Perfluoroctansulfonylfluorid
Perfluoroctansulfonylfluorid (POSF oder PFOSF) ist eine synthetische chemische Verbindung, die zu den per- und polyfluorierten Alkylverbindungen (PFAS) gehört. Sie wird verwendet, um Perfluoroctansulfonsäure (PFOS) und PFOS-basierte Verbindungen herzustellen.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
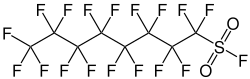 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Perfluoroctansulfonylfluorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8F18O2S | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 502,12 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,824 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
154–155 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Brechungsindex |
1,301 (20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Geschichte
Im Jahr 1949 begann 3M mit der Produktion von POSF durch elektrochemische Fluorierung.[2] Von 1966 bis in die 1990er-Jahre stieg die Produktion von 3M entsprechend der erhöhten Nachfrage nach POSF-basierten Verbindungen.[2] Vor 2000 war 3M der weltweit größte Produzent von POSF (vor allem in den Werken Decatur, Alabama und Antwerpen) und die weltweite Produktion erreichte einen Höchststand von 4500 Tonnen pro Jahr.[2] 3M stellte 2002 die Herstellung und Verwendung von POSF ein, die globale Produktion sank. Die chinesische Produktion wuchs hingegen.[3]
An der 4. Vertragsstaatenkonferenz des Stockholmer Übereinkommens im Mai 2009 wurde entschieden, POSF zusammen mit PFOS und seinen Salzen in die Anlage B der unter dieser Konvention eingeschränkten Substanzen aufzunehmen.[4]
Gewinnung und Darstellung
POSF wird durch elektrochemische Fluorierung von Octansulfonylfluorid in wasserfreiem Hydrogenfluorid hergestellt:[5]
Diese Reaktion führt zu einer 25%igen Ausbeute. Das erhaltene Produkt ist unrein, es handelt sich um eine Mischung von linearen (~70 %) und verzweigten (~30 %) Isomeren handelt. POSF kann auch durch elektrochemische Fluorierung von Octansulfonylchlorid erhalten werden.[5]
Verwendung
POSF wird als Zwischenprodukt zur Herstellung von Monomeren und Tensiden für die Textilbehandlung, Papierchemikalien und inerten Flüssigkeiten verwendet.[6] Zudem ist es das Edukt in der Produktion von Sulfluramid.[7]
Einzelnachweise
- Datenblatt Perfluoro-1-octanesulfonyl fluoride, 95% (sum of isomers) bei Sigma-Aldrich, abgerufen am 10. Mai 2017 (PDF).
- Paul AG, Jones KC, Sweetman AJ: A first global production, emission, and environmental inventory for perfluorooctane sulfonate. In: Environ. Sci. Technol.. 43, Nr. 2, 2009, S. 386–392. doi:10.1021/es802216n. PMID 19238969.
- Wang T, Wang Y, Liao C, Cai Y, Jiang G: Perspectives on the Inclusion of Perfluorooctane Sulfonate into the Stockholm Convention on Persistent Organic Pollutants. In: Environ. Sci. Technol.. 43, Nr. 14, 2009, S. 5171–5175. doi:10.1021/es900464a. PMID 19708337.
- Governments unite to step-up reduction on global DDT reliance and add nine new chemicals under international treaty, Pressecommuniqué, 8. Mai 2009.
- HJ Lehmler: Synthesis of Environmentally Relevant Fluorinated Surfactants – A Review. In: Chemosphere. 58, Nr. 11, 2005, S. 1471–1496. doi:10.1016/j.chemosphere.2004.11.078. PMID 15694468.
- G. W. A. Milne: Gardner's Commercially Important Chemicals Synonyms, Trade Names, and Properties. John Wiley & Sons, 2005, ISBN 0-471-73661-9, S. 480.
- John Löfstedt Gilljam, Juliana Leonel, Ian T. Cousins, Jonathan P. Benskin: Is Ongoing Sulfluramid Use in South America a Significant Source of Perfluorooctanesulfonate (PFOS)? Production Inventories, Environmental Fate, and Local Occurrence. In: Environ. Sci. Technol. 50, 2016, S. 653–659, doi:10.1021/acs.est.5b04544.
