Misoprostol
Misoprostol ist ein synthetisch hergestellter Abkömmling des natürlich vorkommenden Gewebehormons Prostaglandin E1. Es wird als Arzneistoff in der Therapie und Prävention von Magen- und Zwölffingerdarmgeschwüren verwendet sowie in verschiedenen Anwendungsgebieten der Frauenheilkunde und Geburtshilfe.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
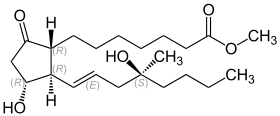 | ||||||||||||||||||||||
| Struktur des wirksamsten Isomers (Eutomers) von Misoprostol | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Misoprostol | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C22H38O5 | |||||||||||||||||||||
| Kurzbeschreibung |
farbloses bis gelbliches Öl, hygroskopisch.[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 382,54 g·mol−1 | |||||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser, löslich in 96%igem Ethanol[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Stereochemische Struktur
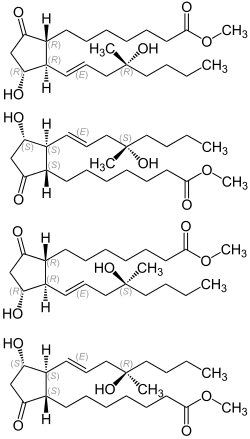
Misoprostol ist ein synthetisch hergestelltes Derivat des Prostaglandins E1 und hat vier chirale Zentren.
Die pharmazeutisch verwendete Substanz ist eine äquimolare Mischung der zwei Enantiomerenpaare
- (8R, 11R, 12R, 13E, 16S) und (8S, 11S, 12S, 13E, 16R) sowie
- (8R, 11R, 12R, 13E, 16R) und (8S, 11S, 12S, 13E, 16S).[2]
Hauptsächlich wirksam ist das (8R, 11R, 12R, 13E, 16S)-Stereoisomer.[1]
Wirkungen
Als Prostaglandin-Analogon wirkt Misoprostol an den Prostaglandin-Rezeptoren der Belegzellen und hemmt die Säure- und Pepsinsekretion im Magen. Es unterstützt ferner die Abwehrmechanismen der Magen- und Darmschleimhaut, indem es die schützende Bikarbonat- und Schleimproduktion fördert. Dadurch können die durch Säureüberproduktion oder durch Schmerzmittel entstandenen Schäden im Magen oder Zwölffingerdarm verringert werden.
Misoprostol bewirkt eine Kontraktion der Gebärmuttermuskulatur.
Misoprostol ist ein Prodrug und wird nach oraler Gabe rasch resorbiert. Der pharmakologisch aktive Metabolit Misoprostolsäure entsteht durch Biotransformation, wobei innerhalb von 15 bis 30 Minuten maximale Plasmakonzentrationen entstehen. Die Plasmaeliminationshalbwertszeit beträgt 20 bis 40 Minuten.[1]
Anwendungsgebiete
Magen- und Zwölffingerdarmgeschwüre
Misoprostol ist als Fertigarzneimittel zugelassen zur Vorbeugung und Behandlung von medikamentenbedingten Schleimhautschädigungen bzw. -geschwüren des Magens und Zwölffingerdarms, die bei der Einnahme von nichtsteroidalen Antirheumatika entstehen können und deren Gabe weder abgesetzt noch die Dosis reduziert werden kann.[4][5]
Wegen der Wirkung auf die Gebärmuttermuskulatur darf eine Anwendung nur erfolgen, wenn eine Schwangerschaft ausgeschlossen ist. Bei Frauen im gebärfähigen Alter darf der Wirkstoff in diesem Anwendungsgebiet nur eingesetzt werden, wenn eine zuverlässige Methode zur Schwangerschaftsverhütung angewendet wird, da unter der Exposition gegenüber Misoprostol im ersten Trimenon ein erhöhtes Risiko für Fehlbildungen des Fetus berichtet wurde.[6] Während der Stillzeit darf Misoprostol nicht eingenommen werden, da es in die Muttermilch übertritt.
Missbrauchsgefahr bestand darin, dass sich schwangere Frauen unter dem Vorwand von Magenbeschwerden aufgrund von Schmerzmittelgebrauch bei ihrem Hausarzt Misoprostol verschreiben lassen konnten, das Mittel dann allerdings zum illegalen Schwangerschaftsabbruch einnahmen.
Gynäkologie, Geburtshilfe
Weitere Anwendungsgebiete liegen in der Gynäkologie und der Geburtshilfe. So findet Misoprostol Anwendung bei nachgeburtlichen Blutungen, Weheneinleitung, verhaltener Fehlgeburt, der Vorbereitung einer Gebärmutterausschabung und beim Schwangerschaftsabbruch.
Wegen dieser wichtigen Indikationen befindet sich der Arzneistoff auf der WHO-Liste der Essential Medicines.[7] Nachdem kritisiert worden war, dass er in dieser Liste nicht für Blutungskomplikationen nach der Geburt eingetragen war,[8] wurde diese Anwendung inzwischen ebenfalls aufgenommen, aber nur für den Fall, dass Oxytocin nicht verfügbar sein sollte. Für gynäkologische bzw. geburtshilfliche Anwendungen sind Misoprostol-haltige Fertigarzneimittel nur in einer beschränkten Anzahl von Ländern zugelassen,[9] daher erfolgt die Anwendung weitgehend im Off-Label-Use. Misoprostol ist das einzige Prostaglandin, das in diesen Anwendungsgebieten oral verabreicht werden kann.
Im April 2021 entschied in Deutschland das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) gemeinsam mit Arzneimittelimporteuren, dass das Mittel Cytotec angesichts vieler Komplikationen im Off-Label-Use in Deutschland nicht mehr vertrieben wird.[10] Der Import des Mittels Cytotec (200μg Misoprostol) wurde gestoppt, da zunehmend über gesundheitliche Schäden bei Schwangeren und Ungeborenen nach unsachgemäßer Anwendung (ungenaue Teilung der Tabletten, nicht etablierte Dosierungsschemata) im Rahmen von zulassungsüberschreitenden Geburtseinleitungen berichtet wurde. Es wird zwar die Zulassung des Mittels Angusta (25μg Misoprostol) erwartet, welches die Aufteilung der Tabletten in kleinere Dosen in einer Klinikapotheke überflüssig macht. Jedoch wird durch den Importstopp eine erschwerte Versorgung von Frauen in den weiteren oben genannten Situationen befürchtet, da hierfür deutlich höhere Dosen erforderlich sind.[11][12]
Seit September 2021 steht mit der Tablette Angusta der Firma Norgine mit 25 μg Misoprostol ein in Deutschland zugelassenes Präparat mit der Indikation Geburtseinleitung zur Verfügung[13][14]
Experimentelle Behandlung der Trigeminusneuralgie
In einer kleinen offenen Studie wurde Misoprostol 2003 als wirksam beschrieben in der Behandlung einer therapierefraktären Trigeminusneuralgie bei Patienten mit Multipler Sklerose.[15]
Nebenwirkungen
Hervorzuheben bei der Therapie von Ulzera ist der in 13 % der Fälle entstehende Durchfall, der insgesamt bei 0,5 % zu einem Abbruch der Therapie führt. Weiterhin können Übelkeit und Bauchschmerzen sowie Kopfschmerzen und Schwindel auftreten.[5] Kardiovaskuläre Wirkungen treten praktisch nicht auf.[1]
Nach Gabe von Misoprostol im zweiten oder dritten Schwangerschaftsdrittel wurde in seltenen Fällen eine Uterusruptur beobachtet, insbesondere bei Frauen, die schon geboren hatten oder mit Narbe nach vorangegangenem Kaiserschnitt.[6]
2020 geriet Cytotec nach Recherchen von report München und der Süddeutschen Zeitung in die Medien, denen zufolge es in Deutschland und Frankreich nach dem nicht zulassungsgemäßen Gebrauch zur Geburtseinleitung (Off Label) zu schwerwiegenden Zwischenfällen gekommen sei. In Deutschland und Frankreich sind daher Klagen vor Gericht anhängig.[16] Einige ausländische Behörden verweisen ausdrücklich auf das potentielle Auftreten von unkontrollierbaren Gebärmutterkontraktionen („Wehensturm“). Der Hersteller Pfizer gibt an, dass es keine ausreichende Studien zur Anwendung von Cytotec gebe. Dem halten die deutschen gynäkologischen Fachverbände über eine Pressemitteilung der Deutschen Gesellschaft für Geburtshilfe und Gynäkologie e. V. (DGGG) entgegen, dass Misoprostol zur Geburtseinleitung in niedrigerer Dosierung – als in Cytotec enthalten – verabreicht werde und in zahlreichen Studien in der vaginalen und oralen Verabreichung untersucht worden sei. Misoprostol werde in fast allen hochrangigen Perinatalzentren eingesetzt und zudem bestünden in anderen Ländern Zulassungen für die Geburtseinleitung mit Misoprostol.[17][18][19] Dagegen warnte im März 2020 die deutsche Arzneimittelbehörde, nachdem ihr neue Berichte über schwere Nebenwirkungen in der off-label Anwendung in der Geburtshilfe eingegangen waren, vor der Anwendung von Cytotec außerhalb des zugelassenen Anwendungsgebiets. Das Mittel sei wegen mangelhafter Teilbarkeit nicht genau genug dosierbar und die neben der oralen Gabe ebenfalls praktizierte sublinguale, buccale oder rektale Verabreichung, mit der der First-Pass-Effekt umgangen werde, sei im Rahmen der Zulassung von Cytotec nicht untersucht worden. Es bestehe die Möglichkeit auf geeignete andere, für eine Geburtseinleitung zugelassene Arzneimittel auszuweichen.[20] Der Import von Cytotec wurde im April 2021 gestoppt.[21]
Handelsnamen
- Frauenheilkunde
- Geburtseinleitung: Angusta (DK, SE, FI, NO, FR), Misodel Vaginalinsert (CH, in D seit 2019 außer Vertrieb[19])
- Schwangerschaftsabbruch (in Übereinstimmung mit den gültigen Gesetzen und Bestimmungen): MisoOne (D, CH), Topogyne (AT, UK)
- Ulkusprohylaxe
- Cytotec (CH), Cyprostol (A). In Deutschland hat der Hersteller Cytotec mit der Begründung der häufigen missbräuchlichen Verwendung zum Schwangerschaftsabbruch 2006 vom Markt genommen, der Import wurde aber erst im April 2021 gestoppt (vgl. oben Nebenwirkungen).[21]
- in Kombination mit Diclofenac: Arthotec (D) Arthrotec (A, CH und andere Länder)
Weblinks
- Eintrag zu Misoprostol bei Vetpharm, abgerufen am 11. August 2012.
Einzelnachweise
- K. Hardtke et al. (Hrsg.): Kommentar zum Europäischen Arzneibuch Ph. Eur. 5.3, Misoprostol. Loseblattsammlung, 25. Lieferung 2006, Wissenschaftliche Verlagsgesellschaft Stuttgart.
- Europäisches Arzneibuch. 6. Auflage, Deutscher Apotheker Verlag, Stuttgart 2008, ISBN 978-3-7692-3962-1, S. 3292–3294.
- Datenblatt Misoprostol ≥ 99 % (TLC) bei Sigma-Aldrich, abgerufen am 10. April 2011 (PDF).
- Fachinformation Cyprostol Tabletten, Stand: März 2009.
- Fachinformation Cytotec 200, Stand: November 2008.
- Beschluss der Koordinierungsgruppe CMDh der HMA, vom 21. Februar 2018.
- WHO Model Lists of Essential Medicines
- Experts seek WHO nod for postpartum haemorrhage drug. IRIN humanitarian news and analysis, 16. März 2011, abgerufen am 21. März 2011.
- Misoprostol Approved. In: misoprostol.org. Abgerufen am 24. September 2017 (englisch).
- Katrin Langhans: Cytotec: Importstopp für umstrittenes Medikament in der Geburtshilfe. In: merkur.de. 6. April 2021, abgerufen am 17. September 2021.
- Katrin Langhans: Cytotec: Importstopp für umstrittenes Medikament in der Geburtshilfe. In: merkur.de. 6. April 2021, abgerufen am 14. April 2021.
- Cytotec ist weg – was bleibt? In: Deutsche Apotheker Zeitung. 19. April 2021, abgerufen am 23. Mai 2021.
- Alexandra Negt: Neu: Misoprostol zur Geburtseinleitung. In: apotheke adhoc. 6. August 2021, abgerufen am 10. August 2021.
- Diana Moll: Misoprostol in Angusta: Orales Arzneimittel zur Geburtseinleitung endlich auf dem deutschen Markt. 2. September 2021, abgerufen am 17. September 2021.
- DMKG study group: Misoprostol in the treatment of trigeminal neuralgia associated with multiple sclerosis. In: Journal of Neurology. Band 250, Nr. 5, 2003, S. 542–545, doi:10.1007/s00415-003-1032-1, PMID 12736732.
- Geburtseinleitung: Kleine Tablette, großes Risiko. In: tagesschau.de. 11. Februar 2020, abgerufen am 11. Februar 2020.
- Stellungnahme zur Berichterstattung über „Cytotec zur Geburtseinleitung“, PM der DGGG vom 13. Februar 2020, abgerufen am 15. Februar 2020.
- Wie gefährlich ist Cytotec bei Geburten; SPON vom 14. Februar 2020, abgerufen am 15. Februar 2020.
- D. Moll: Gefährlich oder Lebensretter für Frauen?Deutsche Apothekerzeitung (DAZonline), 13. Februar 2020.
- Rote-Hand-Brief zu Misoprostol: Risiken im Zusammenhang mit einer Anwendung zur Geburtseinleitung außerhalb der Zulassung („off-label-use“), Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), 16. März 2020.
- tagesschau.de: Importstopp für umstrittenes Medikament Cytotec. Abgerufen am 3. April 2021.