Enalapril
Enalapril ist ein Arzneistoff aus der Gruppe der ACE-Hemmer, der zur Behandlung der arteriellen Hypertonie (Bluthochdruck) und der Herzinsuffizienz eingesetzt wird. Enalapril selbst ist ein inaktives Prodrug. Sein Wirkprinzip beruht nach Aktivierung durch hydrolytische Abspaltung von Ethanol zum Enalaprilat auf der Hemmung des Angiotensin-konvertierenden Enzyms (ACE).
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
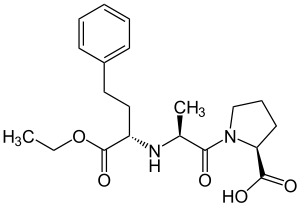 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Enalapril | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C20H28N2O5 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff (Maleat)[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
C09AA02 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 376,45 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
löslich in Wasser: 25 g·l−1[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Chemie
Enalapril wurde den ACE-hemmend wirkenden Peptiden des Giftes der Jararaca-Lanzenotter (Bothrops jararaca), einer brasilianischen Schlangenart, nachempfunden. Enalapril enthält eine stabilisierte Dipeptidstruktur und ist ein Kondensationsprodukt aus den Aminosäuren (S)-Prolin und (S)-Alanin sowie aus 2-Oxo-4-phenylbuttersäureethylester.[3]
In den Forschungslaboratorien der US-amerikanischen Firma Merck Sharp & Dome (MSD) wurden in einem Programm zur Synthese neuer Inhibitoren des Angiotensin-konvertierenden Enzyms (ACE) über 200 Varianten der allgemeinen Formel (Markush-Formel) (I) hergestellt.
.svg.png.webp)
Im Gegensatz zum Vorläufer Captopril enthalten diese kein Schwefelatom. Darunter waren einige Verbindungen, die in Tests eine hohe Aktivität der Hemmung des ACE zeigten.[4][5] Für den Wirkstoff wurde der Internationale Freiname Enalapril vergeben. Die firmeninterne Bezeichnung für die Verbindung war MK-421. Die Ergebnisse der MSD-Forscher wurden im November 1980 in der Zeitschrift Nature veröffentlicht.[6] Enalapril enthält als Strukturteile die Aminosäuren Alanin und am Ende Prolin. Diese Aminosäure war schon im ersten synthetisch erzeugten ACE-Hemmer Captopril verwendet worden. Enalapril war der zweite Inhibitor, dessen Eigenschaften auch besonders gründlich untersucht wurden.[7] Enalapril enthält drei Stereozentren, folglich repräsentiert der Wirkstoff nur ein Diastereomer der möglichen acht verschiedenen Stereoisomeren. Als Arzneistoff wird nur das stereochemisch einheitliche (all-S)-Isomer eingesetzt.
Synthese
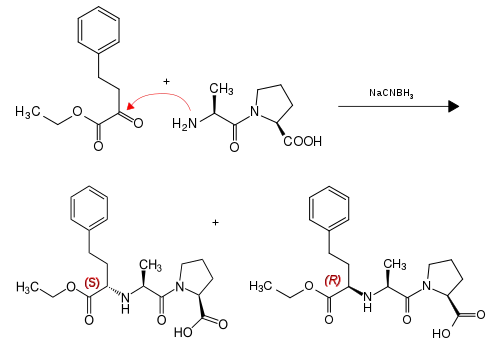
Für die ersten pharmakologischen Untersuchungen wurde die Verbindung durch reduktive Kondensation von 2-Oxo-4-phenylbuttersäure-ethylester mit der Aminogruppe des Dipeptids L-Alanyl-L-prolin [synonym: (S)-Alanyl-(S)-prolin] gewonnen. Dabei erfolgt zuerst eine Reaktion der NH2-Gruppe des Dipeptids mit der Ketogruppe des Reaktionspartners unter Wasserabspaltung. Nach Zugabe eines Reduktionsmittels (hier Natriumcyanoborhydrid, NaCNBH3) in situ eine Hydrierung des Imins.
Da die Ketogruppe und das Imin prochirale Strukturelemente sind, entstehen bei dieser Synthese zwei Diastereomere mit (S,S,S)- bzw. (R,S,S)-Konfiguration, welche durch Chromatographie getrennt wurden. Weitere Synthesen siehe.[8]
Pharmakologie
Enalapril ist ein inaktives Prodrug, was durch Veresterung der freien Carbonsäurefunktion mit Ethanol erreicht wurde. Diese Ethanolgruppe wird im Organismus in der Leber durch Esterasen abgespalten, wodurch das aktive, sogenannte Enalaprilat entsteht. Es sollte besser als ‚Enalaprilsäure‘ (engl. Enalaprilic acid) oder ‚Enalapril-disäure‘ bezeichnet werden, denn es handelt sich um eine Dicarbonsäure bzw. deren Anion.[9]
Anwendungsgebiete
Enalapril wird einzeln (Monotherapie) und in Kombination mit anderen Blutdrucksenkern (Kombinationstherapie, insbesondere mit Diuretika oder Kalziumkanalblockern) überwiegend zur Therapie des Bluthochdrucks eingesetzt. Auch zur Behandlung der Herzinsuffizienz gilt es als Mittel der ersten Wahl. Im Gegensatz zu einigen anderen ACE-Hemmern, wie z. B. Ramipril konnte Enalapril keine Wirksamkeit in der Prophylaxe (Vorbeugung) des Herzinfarkts zeigen.
Wirkmechanismus
Enalapril führt als Inhibitor des Angiotensin Converting Enzyme zu einer verminderten Bildung von Angiotensin II aus Angiotensin I. Diese verminderte Bildung von Angiotensin II bedingt eine Abnahme des Tonus der Blutgefäße und damit eine Abnahme des Blutdrucks. Ebenfalls führt die Abnahme des Angiotensin-II-Spiegels zu einer Verringerung der Aldosteron-Freisetzung aus der Nebennierenrinde und somit zu einer Beeinflussung des Wasserhaushalts (siehe auch Renin-Angiotensin-Aldosteron-System).
Nebenwirkungen
Die meisten Nebenwirkungen von Enalapril werden mit einem durch ACE-Hemmer bedingten verlangsamten Abbau und Kumulation von Bradykinin in Verbindung gebracht. Dazu zählen Hautreaktionen, wie z. B. Exantheme und Nesselsucht, ferner auch Angioödeme. Schwere allergische Hautreaktionen werden hingegen nur sehr selten beobachtet.
Zu den Nebenwirkungen auf die Atemwege zählen trockener Husten, Heiserkeit und Halsschmerz. Asthmaanfälle und Atemnot können ebenfalls, wenn auch selten, auftreten.
Als Folge der Hauptwirkung von Enalapril kann es zu einer zu starken Blutdrucksenkung kommen. Infolgedessen können gelegentlich Schwindel, Kopfschmerz und Benommenheit beobachtet werden. Von schweren Herz-Kreislaufereignissen wie Angina Pectoris, Herzinfarkt und Synkope wurde nur in Einzelfällen berichtet.
Durch den Eingriff in den Wasser- und Elektrolythaushalt können gelegentlich Nierenfunktionsstörungen beobachtet werden. Eine Proteinurie (Ausscheidung von Proteinen im Harn) wird hingegen nur selten beobachtet.
Da Enalapril in der Schwangerschaft u. a. Wachstums- und Knochenbildungsstörungen beim Kind verbunden mit einer erhöhten Sterblichkeit hervorrufen kann, darf Enalapril in dieser Zeit nicht eingenommen werden und sollte durch andere geeignete therapeutische Maßnahmen ersetzt werden.
Wechselwirkungen
Enalapril verstärkt die blutzuckersenkende Wirkung von Insulin und oralen Antidiabetika sowie die blutbildverändernden Wirkungen von Immunsuppressiva.
Durch Eingriff in den Wasser- und Elektrolythaushalt kann die Ausscheidung von Elektrolyten verlangsamt werden, was insbesondere bei der Therapie mit Lithium und kaliumsparenden Diuretika beachtet werden sollte.
Bei Kombination mit anderen blutdrucksenkenden Arzneimitteln sollte eine verstärkte Blutdrucksenkung berücksichtigt werden.
Handelsnamen
Monopräparate
ACEpril (CH), Alapril (A), Elpradil (CH), Epril (CH), Mepril (A), Pres, Renistad (A), Renitec (A), Reniten (CH), Xanef[10] (D), zahlreiche Generika (D, A, CH)
Tiermedizin: Enacard, Enadog, Enalatab, Prilenal
- In Kombination mit Hydrochlorothiazid: Co-Acepril (CH), Co-Renitec (A), Co-Mepril (A), Co-Renistad (A), Coenytyrol (A), Elpradil HCT (CH), Epril plus (CH), Renitec plus (A), Reniten plus (CH), Generika (D, A, CH)
- In Kombination mit Lercanidipin: Carmen ACE (D), Zaneril (D), Zanipress (D), Zanipril (A)
- In Kombination mit Nitrendipin: Baroprine (A), Cenipress (A), Eneas (D)
Literatur
- Wolfgang Blaschek et al. (Hrsg.): Hagers Enzyklopädie der Arzneistoffe und Drogen. Band 6. 6. Auflage. Wiss. Verlagsges. [u. a.], Stuttgart [u. a.] 2007, ISBN 978-3-8047-2384-9, S. 602–605.
Einzelnachweise
- Datenblatt Enalapril bei Sigma-Aldrich, abgerufen am 8. Dezember 2016 (PDF).
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, ISBN 978-0-911910-00-1, S. 607.
- Axel Kleemann, Jürgen Engel, Bernd Kutscher, Dietmar Reichert: Pharmaceutical Substances. 4. Auflage. Thieme-Verlag, Stuttgart 2000, ISBN 978-1-58890-031-9, S. 739–741.
- Europäische Patent Anmeldung 12 401.
- E. E. Harris et al. US-Patent 4374829 (1980, 1983) beide für MSD
- A. A. Patchett et al.: A new class of angiotensin-converting enzyme inhibitors. Nature 288, 280–283 (1980).
- D. Heber, J. Mann: Artikel. In: Hagers Enzyklopädie (siehe Literatur).
- Axel Kleemann, Jürgen Engel, Bernhard Kutscher, Dietmar Reichert: Pharmaceutical Substances. 5. Auflage. Thieme-Verlag, Stuttgart / New York 2009, ISBN 978-1-58890-031-9, S. 469–471.
- W. Forth, D. Henschler, W. Rummel: Allgemeine und spezielle Pharmakologie und Toxikologie. 5. Auflage. Bibliographisches Institut / F. A. Brockhaus, Mannheim / Wien / Zürich 1987, ISBN 3-411-03150-6, S. 158.
- Rote Liste 2017 – Arzneimittelverzeichnis für Deutschland (einschließlich EU-Zulassungen und bestimmter Medizinprodukte). 57. Ausgabe. Rote Liste Service, Frankfurt am Main 2017, ISBN 978-3-946057-10-9, S. 553.