Dischwefeldecafluorid
Dischwefeldecafluorid ist eine chemische Verbindung aus der Gruppe der anorganischen Schwefelverbindungen und Fluoride, die 1934 durch Denbigh und Whytlaw-Gray entdeckt wurde.[5]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
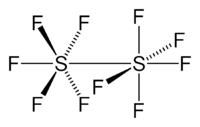 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Dischwefeldecafluorid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | S2F10 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit Geruch nach Schwefeldioxid[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 254,12 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
2,08 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
28,7 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 0,01 ml·m−3 bzw. 0,1 mg·m−3[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Dischwefeldecafluorid bildet sich als Nebenprodukt bei der Reaktion von Schwefel mit Fluor oder auf photochemischem Wege aus Schwefelchloridpentafluorid.[6]
Eigenschaften
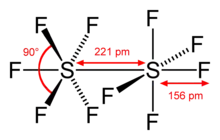
Dischwefeldecafluorid ist eine farblose Flüssigkeit mit Geruch nach Schwefeldioxid und ist durch die Bildung von SF5•-Radikalen sehr reaktionsfreudig. Bei Erhitzung zersetzt es sich zu Schwefelhexafluorid und Schwefeltetrafluorid. Bei Vorhandensein eines Überschusses an Chlor reagiert es zu Schwefelchloridpentafluorid.
Dischwefeldecafluorid ist unlöslich in Wasser und reagiert auch nicht mit diesem.[7] Es wird auch nicht durch wässrige Lösungen im sauren und alkalischen Bereich, jedoch in 10%iger Kaliumhydroxid-Lösung in Methanol hydrolysiert.[2]
In der nebenstehenden Abbildung sind Bindungslängen und -winkel des Dischwefeldecafluorids dargestellt.
Verwendung
Aus Ammoniak und Dischwefeldecafluorid kann Thiazyltrifluorid dargestellt werden.[8]
Sicherheitshinweise
Dischwefeldecafluorid ist sehr giftig. Es wirkt bei Inhalation schon im ppm-Bereich tödlich auf Ratten. Untersuchungen ergaben, dass es mindestens dreimal so giftig ist wie Phosgen.[9] Daher war es im Zweiten Weltkrieg als Lungenkampfstoff angedacht, weil es im Gegensatz zu einigen anderen chemischen Kampfstoffen bei Kontakt mit den Augen keine Tränen- oder Hautreizungen auslöst und damit schwer rechtzeitig erkannt werden kann.[10]
Literatur
Einzelnachweise
- Eintrag zu Dischwefeldecafluorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Februar 2017. (JavaScript erforderlich)
- Kurte: Infrarot-spektrometrische Spurengasbestimmung in für elektrische Schaltanlagen verwendetem Schwefelhexafluorid. Dissertation, TU Dortmund 2002
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 5714-22-7 bzw. Dischwefeldecafluorid), abgerufen am 2. November 2015.
- Kenneth G. Denbigh and Robert Whytlaw-Gray: The preparation and properties of disulphur decafluoride. In: J. Chem. Soc. 1934, S. 1346–1352. doi:10.1039/JR9340001346.
- Hans P. Latscha, Helmut A. Klein; Anorganische Chemie, ISBN 978-3-540-42938-8.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 565.
- Steve Mitchell (1996). Steve Mitchell, ed. Biological interactions of sulfur compounds. CRC Press. p. 14. ISBN 0-7484-0245-4.
- Fritz Ullmann; Ullmanns Encyklopädie der technischen Chemie, ISBN 978-3-527-20000-9.
- Harold Johnston: A bridge not attacked: chemical warfare civilian research during World War II. World Scientific, 2003, ISBN 9812381538, S. 33–36.