Acetylendicarbonsäuredimethylester
Acetylendicarbonsäuredimethylester (DMAD) ist eine organische chemische Verbindung mit der Formel C6H6O4 aus der Gruppe der Carbonsäureester mit einer C≡C-Dreifachbindung.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
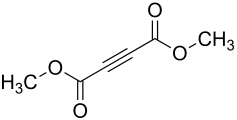 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Acetylendicarbonsäuredimethylester | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H6O4 | ||||||||||||||||||
| Kurzbeschreibung |
schwach gelbliche Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 142,11 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,16 g·cm−3 (20 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
195–198 °C[1] | ||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[1] | ||||||||||||||||||
| Brechungsindex |
1,447[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
Maleinsäure wird bromiert und die resultierende Dibrombernsteinsäure mit Kaliumhydroxid dehydrohalogeniert. Die entstehende Acetylendicarbonsäure wird dann mit Methanol und Schwefelsäure als Katalysator verestert.
Eigenschaften
Acetylendicarbonsäuredimethylester ist eine schwach gelbliche Flüssigkeit, die sich bei starker Erhitzung oder unter Lichteinwirkung zersetzt.[1]
Verwendung
DMAD als bei Raumtemperatur flüssiges Alkin ist stark elektrophil. Daher wird es als Dienophil in Cycloadditionsreaktionen – wie der Diels-Alder-Reaktion – eingesetzt.[2] Es ist auch ein starker Michael-Akzeptor.
Sicherheitshinweise
Acetylendicarbonsäuredimethylester ist ein Reizstoff und ein Ätzstoff. Bei Kontakt mit Metallen kann Wasserstoff entstehen, wodurch Explosionsgefahr besteht.[1]
Einzelnachweise
- Datenblatt Acetylendicarbonsäuredimethylester (PDF) bei Merck, abgerufen am 2. März 2013.
- Datenblatt Dimethyl acetylenedicarboxylate bei Sigma-Aldrich, abgerufen am 20. März 2011 (PDF).
- Datenblatt Dimethyl Acetylenedicarboxylate (PDF) bei Fisher Scientific, abgerufen am 13. Februar 2014.

