Raffinose
Raffinose ist ein in Pflanzen vorkommendes Kohlenhydrat, genauer ein Dreifachzucker (Trisaccharid). Sie setzt sich aus den drei Einfachzuckern Galactose, Glucose und Fructose zusammen. Sie ist ein nichtreduzierender Zucker, da keine Ringöffnung möglich ist.[1]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
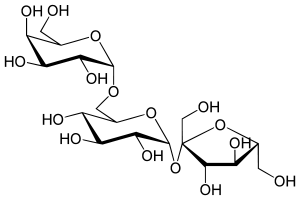 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Raffinose | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C18H32O16 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Prismen[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 504,46 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Vorkommen und Funktion


Raffinose und die Raffinose-Familie ersetzt in manchen Pflanzen die Stärke als Speicherkohlenhydrat. In größeren Mengen ist Raffinose in Hülsenfrüchten enthalten. Bei Erbsen und Bohnen können sie 5 bis 15 % der Trockensubstanz ausmachen. Raffinose ist auch in Zuckerrohr und Zuckerrüben enthalten, sammelt sich bei der Zuckerherstellung aber in der Melasse an. Raffinose dient in einigen Arten (Kürbisgewächse, Linden, Ulmen) auch anstelle der Saccharose als Transportsubstanz in den Siebröhren des Phloems.
Biosynthese
Die Biosynthese in Pflanzen erfolgt, indem von Galactinol ein Galactosylrest auf Saccharose übertragen wird, wobei myo-Inosit frei wird.
- Saccharose + Galactinol → Raffinose + myo-Inosit.
Diese Reaktion wird durch eine myo-Inositol-Galactosyl-Transferase katalysiert. Die Galactose wird dabei in α-1,6-glycosidischer Bindung angehängt und es ergibt sich α-D-Galactopyranosyl-(1→6)-α-D-glucopyranosyl-(1→2)-β-D-fructofuranosid.
Analytik
Die zuverlässige qualitative und quantitative Bestimmung der Raffinose gelingt nach hinreichender Probenvorbereitung und Derivatisierung als Trimethylsilylderivate durch Kopplung der Gaschromatographie[3] oder HPLC mit der Massenspektrometrie.[4]
Raffinose-Familie
Von der Raffinose leiten sich zwei weitere Oligosaccharide ab, bei denen in gleicher Weise ausgehend von der Raffinose in α-1,6-glycosidischer Bindung weitere Galactoseeinheiten angehängt werden:
- Raffinose + Galactinol → Stachyose + myo-Inosit,
- Stachyose + Galactinol → Verbascose + myo-Inosit.
Daher werden Raffinose, Stachyose und Verbascose auch als Raffinose-Familie bezeichnet.
Die Verbindungen haben folgende molare Massen:
- Raffinose: 504,5 g·mol−1
- Stachyose: 666,6 g·mol−1
- Verbascose: 828,7 g·mol−1
Mensch
Raffinose besitzt nur 22 %[5] der Süßkraft von Rübenzucker (Saccharose), da mit zunehmendem Polymerisationsgrad Saccharide zunehmend geschmacksneutral werden.
Im Dünndarm wird sie nur in geringem Umfang gespalten und resorbiert, da die α-Galactosidbindung von menschlichen Verdauungsenzymen nicht gespalten werden kann. Dies hat zur Folge, dass größere Mengen in den Dickdarm gelangen. Die dort vorhandenen anaeroben Mikroorganismen der Darmflora verwerten sie und produzieren dabei unter anderem Gase, die zu Blähungen führen.
Literatur
- Hans W. Heldt, Birgit Piechulla: Pflanzenbiochemie. 4. Auflage. Spektrum Akademischer Verlag, Heidelberg 2008, ISBN 978-3-8274-1961-3, S. 252–253.
Weblinks
Einzelnachweise
- Eintrag zu Raffinose. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Dezember 2014.
- Datenblatt Raffinose bei Sigma-Aldrich, abgerufen am 15. Juni 2011 (PDF).
- Z. Füzfai, I. Boldizsár, I. Molnár-Perl: Characteristic fragmentation patterns of the trimethylsilyl and trimethylsilyl-oxime derivatives of various saccharides as obtained by gas chromatography coupled to ion-trap mass spectrometry. In: J Chromatogr A. 1177(1), 4. Jan 2008, S. 183–189. PMID 18061601
- M. I. Perlné, K. Horváth, Z. Katona: The possibilities of GC/MS and HPLC in the analysis of sugars and acids in natural matrices. In: Acta Pharm Hung. 70(3-6), Jul-Dez 2000, S. 231–238. PMID 11379030
- Hans-Dieter Belitz, Werner Grosch, Peter Schieberle: Lehrbuch der Lebensmittelchemie. 6., vollst. überarb. Auflage. Springer, Berlin 2008, ISBN 978-3-540-73201-3, S. 263.