Poliovirus
Das Poliovirus (genauer Humanes Poliovirus, gelegentlich noch Poliomyelitis-Virus, PV) ist eine Subspezies von Viren der Spezies Enterovirus C (EV-C) aus der Gattung Enterovirus in der Familie der Picornaviridae.[3][4] Das Poliovirus löst beim Menschen die Kinderlähmung (Poliomyelitis, kurz Polio) aus. Es handelt sich um ein sehr einfaches Virus ohne Hülle mit einem Genom aus einzelsträngiger plus-RNA. Es kommt beim Menschen und manchen anderen Primaten vor. Die Ausrottung des Poliovirus durch Impfung ist ein Ziel der Weltgesundheitsorganisation. In Deutschland gilt es bereits als ausgerottet.
| Humanes Poliovirus | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||
| Systematik | ||||||||||||||||||||
| ||||||||||||||||||||
| Taxonomische Merkmale | ||||||||||||||||||||
| ||||||||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||||||||
| Human poliovirus | ||||||||||||||||||||
| Kurzbezeichnung | ||||||||||||||||||||
| PV, EV-C | ||||||||||||||||||||
| Links | ||||||||||||||||||||
|
Entdeckung und Geschichte
Obwohl die Poliomyelitis eine seit langem bekannte Krankheit war, wurde erst nach Studien des schwedischen Arztes Ivar Wickman zu Beginn des 20. Jahrhunderts allgemein anerkannt, dass es sich um eine durch Kontakt übertragene Infektionskrankheit handelt. Als Entdecker des Poliovirus gelten aber Karl Landsteiner und Erwin Popper; 1908 gelang es ihnen, durch Injektion eines bakteriologisch sterilen Rückenmarkextraktes aus einem an Poliomyelitis verstorbenen Jungen den Erreger auf zwei Affen zu übertragen; beide Tiere erkrankten.[5]
Charles Armstrong gelang es in den 1930er Jahren, das Virus auf Baumwollratten zu übertragen. John F. Enders, Frederick Chapman Robbins und Thomas Huckle Weller konnten 1949 das Virus in Zellkulturen vermehren; dafür erhielten sie 1954 gemeinsam den Nobelpreis für Physiologie oder Medizin. 1955 wurde ein von Jonas Salk entwickelter, inaktivierter Polioimpfstoff zugelassen, 1960 eine Schluckimpfung von Albert Sabin.
2010 durchbrach eine mutierte Virusvariante (englisch circulating vaccine-derived poliovirus, cVDPV) den Impfschutz in der Republik Kongo und verursachte einen schweren Ausbruch, in dessen Verlauf mehrere hundert Personen infiziert wurden und fast die Hälfte von ihnen verstarb.[6]
Virusaufbau
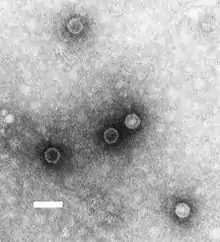
Morphologie
Das annähernd runde unbehüllte Viruspartikel hat einen Durchmesser von 28 bis 30 Nanometer. 1985 gelang es, mittels Kristallstrukturanalyse die dreidimensionale Struktur eines kompletten Polioviruspartikels aufzulösen.[7] Jedes Virion enthält eine Kopie des einzelsträngigen RNA-Genoms, das von einem ikosaedrischen Kapsid umhüllt wird. Das Kapsid setzt sich aus je 60 Kopien der vier Kapsidproteine VP1, VP2, VP3 und VP4 zusammen.
Aufgrund dieser Struktur ist das Poliovirus ein relativ umweltstabiles Virus, das als unbehülltes Virus nur langsam durch Desinfektionsmittel wie 70-prozentiges Ethanol oder Isopropanol inaktiviert wird. Es zählt daher zu jenen Viren, an denen Desinfektionsmittel im Zulassungsverfahren ihre Wirksamkeit erweisen müssen.[8] Auch durch viele Detergenzien,[9] durch quartäre Ammoniumverbindungen oder durch Säuren, beispielsweise Magensäure, wird das Virus nur langsam inaktiviert.
Genom und Virusproteine
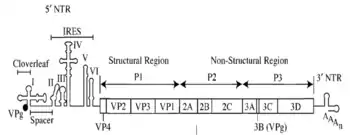
Das virale Genom wurde erstmals 1981 kloniert und sequenziert. Die beim Typ 1 7440 Nukleotide lange RNA, an deren 5'-Ende ein virales Protein (VPg) gebunden ist, besteht aus einem langen 5'-untranslatierten Bereich (5'-NTR), der von einem einzigen offenen Leserahmen gefolgt wird, welcher für ein Polyprotein von 220 kDa codiert, sowie einem kurzen 3'-untranslatierten Bereich (3'-NTR) mit einem Poly(A)-Schwanz. Im 5'-untranslatierten Bereich enthält die RNA eine interne ribosomale Eintrittsstelle (IRES), die für die Translation der RNA in der Wirtszelle entscheidend ist. Mutationen in der IRES sind eine molekulare Ursache für die Attenuierung der Polioviren, die für orale Polioimpfstoffe benutzt werden.
Das 220 kDa-Polyprotein wird durch virale Peptidasen in drei Proteine, P1, P2 und P3 zerteilt; das P1-Protein wird weiter aufgespalten in die strukturellen Proteine VP1–VP4, aus denen das Kapsid der neuen Viruspartikel zusammengesetzt wird. Aus den Proteinen P2 und P3 gehen Nichtstrukturproteine hervor, die eine Funktionen bei der Vermehrung des Virus haben. Die Proteine 2Apro und 3Cpro sowie 3CDpro sind Peptidasen, die das virale Polyprotein zerteilen, während die Proteine 2BC, 2C und 3AB einen Membrankomplex bilden, der für die Virusreplikation benötigt wird. 3BVPg bindet an das 5'-Ende der viralen RNA und ist für die Initiation der Replikation der RNA wichtig, 3Dpol schließlich ist eine RNA-abhängige RNA-Polymerase, die die virale RNA synthetisiert.[10]
Replikation
Das Poliovirus vermehrt sich im Zytoplasma der Wirtszelle. Um in die Zelle eindringen zu können, benötigt das Virus einen spezifischen Rezeptor, das CD155-Protein. Dann kann das Virus seine RNA in die Zelle übertragen, wo diese unmittelbar zum Polyprotein translatiert wird. Das Polyprotein kann sich selbst proteolytisch in einzelne strukturelle und funktionelle Proteine zerlegen. Die RNA wird nicht nur translatiert, sondern auch repliziert. Letzteres geschieht durch die virale RNA-abhängige RNA-Polymerase 3Dpol, die die ursprüngliche plus-RNA in eine minus-RNA umschreibt und von dieser sogleich wieder neue plus-RNA erzeugt. Die RNA wird schließlich mit den Strukturproteinen zu einem neuen Virusteilchen (Virion) verpackt; schließlich stirbt die Wirtszelle und die Viren werden freigesetzt.
Systematik
Das Poliovirus gehört zur Virusgattung Enterovirus; diese ist Teil der Familie der Picornaviridae. Beim Poliovirus werden drei Serotypen unterschieden.
- Ordnung Picornavirales
- Familie Picornaviridae
- Gattung Enterovirus
- Spezies Enterovirus C (EV-C)
- Subspezies Humanes Enterovirus C (HEV-C)
- Subspezies (Humanes) Poliovirus (PV, HPV)
- Serotyp 1 (PV1, Typ „Mahoney“ oder „Brunhilde“): dieser Typ kommt am häufigsten vor und kann auch eine schwere Erkrankung verursachen.
- Serotyp 2 (PV2, Typ „Lansing“): dieser Typ verursacht eher leichte Verläufe (gilt seit 2015 als ausgerottet).
- Serotyp 3 (PV3, Typ „Saukett“ bzw. „Leon“): dieser Typ kommt eher selten vor, verursacht aber in der Regel einen ernsten Verlauf (gilt seit 2019 als ausgerottet).
Die drei Serotypen unterscheiden sich strukturell vor allem in den Kapsidproteinen. Vergleiche der vollständigen Genomsequenzen der Polioviren und des Humanen Enterovirus C (HEV-C) zeigten, dass die Polioviren und die HEV-C-Viren in der Genomstruktur zueinander sehr ähnlich sind. Außerhalb der Kapsidregion sind die Polioviren zu den HEV-C-Viren so ähnlich wie untereinander. Deshalb wurde vorgeschlagen, die Spezies Poliovirus aufzugeben und die drei Serotypen in die Spezies Enterovirus C (heutiger Name, Stand November 2018) einzuordnen.[11]
Verbreitung, Übertragung und Spezifität
Verbreitung und Ausrottung
Ursprünglich war das Virus weltweit verbreitet; in den Tropen traten Epidemien ganzjährig auf, in gemäßigten Breiten vor allem im Sommer. In Endemiegebieten ist das Virus unter anderem auch in Abwässern nachweisbar; in der Umwelt soll es mehrere Wochen vermehrungsfähig bleiben. Der einzige natürliche Wirt und damit das einzige bekannte Reservoir ist der Mensch. Daher scheint eine Ausrottung durch Impfung möglich. Tatsächlich ist das Polio-Wildvirus vom Typ 2 (WPV2) bereits seit 1999 nicht mehr nachgewiesen. 2007 gab es weltweit 1310 Fälle von Poliomyelitis durch Wildviren. Im Jahr 2008 war das Virus nur noch in Nigeria, Indien, Pakistan und Afghanistan endemisch.[12][13] 2012 wurde in Nigeria Polio-Wildvirus 3 (WPV3) das letzte Mal nachgewiesen. 2015 wurde Typ 2 durch die WHO als ausgerottet erklärt. Am Welt-Poliotag 2019 erklärte die WHO auch Typ 3 für ausgerottet.[14]
Übertragung und Spezifität
Das Virus wird durch Schmierinfektion und auch über Gegenstände übertragen. Der Tropismus des Poliovirus beschränkt sich auf den Menschen und manche andere Primaten. Verschiedene Affen können experimentell infiziert werden, indem das Virus direkt in das Rückenmark oder das Gehirn injiziert wird. Lediglich Schimpansen und Altweltaffen können auch wie der Mensch auf oralem Wege infiziert werden. Da das Virus für die Infektion einen spezifischen Rezeptor, das CD155-Protein, auf den Wirtszellen benötigt, hängt die Infektion eines Organismus wesentlich davon ab, ob das Virus an den Rezeptor im Wirt binden kann. Das Poliovirus bindet an CD155 vom Menschen, vom Schimpansen und von Altweltaffen, aber nur teilweise auch an CD155 von Neuweltaffen.[15] Nach Bindung an den CD155-Rezeptor wird das Virus in die Zelle aufgenommen, wo es sich vermehren kann. Die Vermehrungsmechanismen innerhalb der Zelle sind weniger wirtsspezifisch als der Aufnahmemechanismus. Der CD155-Rezeptor befindet sich auf der Zelloberfläche von Monozyten, Makrophagen, T-Lymphozyten und Nervenzellen. Lymphatische Gewebe wie die Peyer-Plaques im Darm sind der Ort der ersten Virusvermehrung.
Erkrankung, Nachweis und Impfstoffe
Erkrankung
Nachdem das Virus über den Mund aufgenommen wurde und sich im Nasopharynx und im Verdauungstrakt vermehrt hat, kommt es zu einer Virämie, bei der das Virus über die Blutbahn verteilt wird. In den meisten Fällen verläuft dies ohne Symptome; lediglich bei 4 bis 8 % der Infizierten kommt es zu grippeähnlichen Beschwerden.
Nur in seltenen Fällen, bei zirka 1 % der Infektionen, befallen die Viren auch Nervenzellen, und zwar vorzugsweise die für die Muskulatur wichtigen Vorderhornzellen im Rückenmark. Dies führt dann zum Krankheitsbild der Kinderlähmung.
Nachweis
Der Nachweis des Virus kann aus Stuhlproben, Rachenabstrichen und gegebenenfalls aus Liquor erfolgen. Beim klassischen virologischen Nachweis wird das aufbereitete Material auf Zellkulturen inkubiert und die Identität des Virus mit einem Neutralisationstest mit spezifischen Antisera bestimmt. Eine Isolierung des Virus aus Stuhlproben soll in den ersten 14 Tagen der Erkrankung zu 80 % erfolgreich sein.[16] Diese Methodik ist aber aufwändig. Deshalb wird heute oft die Reverse Transkriptase-Polymerase-Kettenreaktion eingesetzt, mit der direkt virale RNA in klinischem Material nachgewiesen werden kann. Teilweise werden sogar Teile des Virusgenoms sequenziert, um über Sequenzvergleiche Zusammenhänge zwischen verschiedenen Patienten herzustellen und den Infektionsweg nachzuvollziehen zu können. Auch ein Nachweis von Antikörpern gegen das Virus in Serum des Patienten kann durchgeführt werden.
Meldepflicht
In Deutschland ist der direkte oder indirekte Nachweis des Poliovirus namentlich meldepflichtig nach § 7 des Infektionsschutzgesetzes (IfSG), soweit der Nachweis auf eine akute Infektion hinweist. Diese Meldepflicht für den Erreger betrifft in erster Linie Labore bzw. deren Leitungen (vgl. § 8 IfSG).
In der Schweiz ist der positive laboranalytische Befund zu einem Poliovirus für Laboratorien meldepflichtig und zwar nach dem Epidemiengesetz (EpG) in Verbindung mit der Epidemienverordnung und Anhang 3 der Verordnung des EDI über die Meldung von Beobachtungen übertragbarer Krankheiten des Menschen.
Impfstoffe
Es gibt zwei verschiedene Polioimpfstoffe:
- Die inaktivierte Poliovakzine (IPV) nach Jonas E. Salk (auch: Salk-Vakzine) ist ein Totimpfstoff, der intramuskulär injiziert wird.[17] Der Impfstoff enthält auf Zellkulturen gezüchtete, mit Formaldehyd inaktivierte Viruspartikel der drei Typen („trivalent“). Dieser Impfstoff bietet guten Schutz gegen die Erkrankung; der entscheidende Vorteil dieses Impfstoffes ist, dass eine Impf-Poliomyelitis ausgeschlossen ist. Der inaktivierte Polioimpfstoff wurde 1955 in den USA zugelassen und führte dort zu einem rapiden Rückgang der Erkrankungen. Als Kombinationsimpfstoff ist IPV auch mit anderen Impfstoffen z. B. gegen Tetanus und Diphtherie erhältlich (Td-IPV-Impfstoff).
- Die orale Poliovakzine (OPV) nach Albert Sabin (auch: Sabin-Vakzine) zur Schluckimpfung ist ein eingesetzter Lebendimpfstoff und besteht aus einer Mischung aus den drei Typen sogenannter attenuierter Viren, die zwar noch vermehrungsfähig sind, aber keine Krankheit mehr erregen (fehlende Neurotoxizität).[17] Im Magen-Darm-Trakt erzeugt der Impfstoff eine inapparente Infektion. Der Vorteil dieses Impfstoffes ist neben der einfachen Anwendung, dass er auch eine Immunität im Magen-Darm-Trakt erzeugt (IgA-Schleimhautimmunität), die nicht nur die Erkrankung, sondern auch eine Übertragung des Virus verhindert. Bei Immundefekten und Immunsuppression ist OPV kontraindiziert.[17]
In Deutschland wird der Lebendimpfstoff nicht mehr angewendet, da eine Impf-Poliomyelitis, insbesondere bei Patienten mit Immundefekten (v. a. Agammaglobulinämien), nicht vollkommen ausgeschlossen werden kann.[17] Da das Poliovirus in Deutschland ausgerottet ist, wäre dies ein nicht akzeptables Risiko. Die WHO verwendet dagegen im Zuge des weltweiten Poliomyelitis-Eradikationsprogramm den Lebendimpfstoff.[17]
Einzelnachweise
- ICTV Master Species List 2018b.v2 MSL #34v, März 2019
- ICTV: ICTV Taxonomy history: Enterovirus C, EC 51, Berlin, Germany, July 2019; Email ratification March 2020 (MSL #35)
- International Committee on Taxonomy of Viruses (ICTV): Master Species List 2018a v1, MSL including all taxa updates since the 2017 release. Fall 2018 (MSL #33)
- ViralZone: ICTV 2016 Master Species List #31 with Acronyms, (Excel XLSX), SIB Swiss Institute of Bioinformatics
- Hans J. Eggers: Milestones in early poliomyelitis research (1840 to 1949). In: Journal of Virology. Band 73, Nr. 6, Juni 1999, S. 4533–4535, PMID 10233910.
- Jan Felix Drexler et al.: Robustness against serum neutralization of a poliovirus type 1 from a lethal epidemic of poliomyelitis in the Republic of Congo in 2010. In: Proceedings of the National Academy of Sciences of the United States of America. Band 111, Nr. 35, 2. September 2014, S. 12889–12894, doi:10.1073/pnas.1323502111, PMID 25136105, PMC 4156724 (freier Volltext).
- J. M. Hogle et al.: Three-dimensional structure of poliovirus at 2.9 A resolution. In: Science (New York, N.Y.). Band 229, Nr. 4720, 27. September 1985, S. 1358–1365, doi:10.1126/science.2994218, PMID 2994218.
- Prüfung und Deklaration der Wirksamkeit von Desinfektionsmitteln gegen Viren. In: Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz. 2004, Band 47, S. 62–66. doi:10.1007/s00103-003-0754-7. (PDF) (Memento des Originals vom 21. Oktober 2013 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.. Abgerufen am 24. Mai 2013.
- J. Steinmann et al.: Comparison of virucidal activity of alcohol-based hand sanitizers versus antimicrobial hand soaps in vitro and in vivo. In: The Journal of Hospital Infection. Band 82, Nr. 4, Dezember 2012, S. 277–280, doi:10.1016/j.jhin.2012.08.005, PMID 23009803.
- Nidia H. De Jesus: Epidemics to eradication: the modern history of poliomyelitis. In: Virology Journal. Band 4, 10. Juli 2007, S. 70, doi:10.1186/1743-422X-4-70, PMID 17623069, PMC 1947962 (freier Volltext).
- Betty Brown et al.: Complete genomic sequencing shows that polioviruses and members of human enterovirus species C are closely related in the noncapsid coding region. In: Journal of Virology. Band 77, Nr. 16, August 2003, S. 8973–8984, doi:10.1128/jvi.77.16.8973-8984.2003, PMID 12885914.
- Centers for Disease Control and Prevention (CDC). Progress toward interruption of wild poliovirus transmission--worldwide, January 2007–April 2008. In: MMWR Morb Mortal Wkly Rep. 57(18), 9. Mai 2008, S. 489–494. PMID 18463607
- Verbreitungskarte 2006 (Memento vom 25. September 2006 im Webarchiv archive.today) für das Poliovirus (polioeradication.org)
- Two out of three wild poliovirus strains eradicated: Global eradication of wild poliovirus type 3 declared on World Polio Day, online 24. Oktober 2019, abgerufen 24. Oktober 2019
- Shaukat Khan et al.: Characterization of the New World monkey homologues of human poliovirus receptor CD155. In: Journal of Virology. Band 82, Nr. 14, Juli 2008, S. 7167–7179, doi:10.1128/JVI.02664-07, PMID 18480448, PMC 2446954 (freier Volltext).
- Merkblatt Poliomyelitis. des Robert Koch-Instituts In: Epidemiologisches Bulletin. 1/2010, S. 5–8.
- Albert Heim: Picornaviren. In: Sebastian Suerbaum, Gerd-Dieter Burchard, Stefan H. E. Kaufmann, Thomas F. Schulz (Hrsg.): Medizinische Mikrobiologie und Infektiologie. Springer-Verlag, 2016, ISBN 978-3-662-48678-8, S. 459, doi:10.1007/978-3-662-48678-8_55.
Literatur
- David M. Knipe, Peter M. Howley (Red.): Fields’ Virology. 5. Auflage. 2 Bände. Philadelphia 2007, ISBN 978-0-7817-6060-7, S. 796–884.
- Anonymus: Globale Polioeradikation – zwischen Bangen und Zuversicht. In: Hygiene und Medizin. 29(11), 2004, S. 400–401. ISSN 0172-3790
Weblinks
- Global Polio Eradication Initiative
- Poliovirus in der Datenbank des International Committee on Taxonomy of Viruses (ICTV)
- Poliovirus in der Taxonomie-Datenbank des NCBI
- Genom- und Polyproteinsequenz des Poliovirus Typ 1