Peroxomonoschwefelsäure
Peroxomonoschwefelsäure (auch Peroxoschwefelsäure, Peroxy-Monoschwefelsäure oder Carosche Säure) ist eine Oxosäure des Schwefels. Ihre Salze heißen Peroxomonosulfate, z. B. Kaliumperoxomonosulfat (KHSO5).[3] Die farblosen wässrigen Lösungen der Peroxomonoschwefelsäure werden im Praxisjargon von Chemielaboren auch Knabberwasser, Piranhasäure oder Piranha-Lösung genannt. Der Chemiker Heinrich Caro beschrieb sie erstmals 1898.[4]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
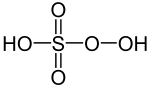 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Peroxomonoschwefelsäure | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | H2SO5 | |||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 114,09 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Darstellung
Eine Synthese kann durch Umsetzung von Chlorsulfonsäure (ClSO3H) mit Wasserstoffperoxid erfolgen:[5]
Bei weiterer Umsetzung mit Chlorsulfonsäure bildet sich Peroxodischwefelsäure (H2S2O8).
Peroxomonoschwefelsäure als wässrige Lösung ist unter Normalbedingungen instabil und wird daher zur Verwendung stets neu hergestellt. Hierfür wird Wasserstoffperoxid zu konzentrierter Schwefelsäure gegeben. (Vorsicht: Hitzeentwicklung):
Dabei entsteht neben Peroxomonoschwefelsäure auch Wasser als Reaktionsprodukt.
Eigenschaften
Peroxomonoschwefelsäure ist ein farbloser, äußerst hygroskopischer, feinkristalliner Feststoff, der nach Ozon riecht. In reinem Zustand ist er mehrere Wochen unter nur geringem Verlust von aktivem Sauerstoff haltbar, in unreiner Form ist er wesentlich unbeständiger. Er ist unzersetzt löslich in Ethanol und wenig löslich in Ether.[6] Beim Lösen in Wasser wird in einer Gleichgewichtsreaktion Wasserstoffperoxid (H2O2) freigesetzt:
Peroxomonoschwefelsäure wirkt stark oxidierend.
Verwendung
Peroxomonoschwefelsäure wird als Reinigungs- und Bleichmittel verwendet. Sie wird zum Beispiel zur Reinigung von Glasfritten verwendet. Dabei dürfen unter keinen Umständen organische Lösungsmittel wie z. B. Aceton zugesetzt werden, da dies zu Explosionen führen kann.
Gefahren
Reine Peroxomonoschwefelsäure ist hochexplosiv.[7] Wie alle starken Oxidationsmittel bildet Peroxomonoschwefelsäure in Kontakt mit organischen Verbindungen, wie z. B. Ethern, Ketonen oder organischen Lösungsmitteln sehr instabile Moleküle, wie z. B. Acetonperoxid.
Einzelnachweise
- Sicherheitsdatenblatt Solvay abgerufen am 18. Februar 2021
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Wiberg, Egon., Wiberg, Nils,: Lehrbuch der anorganischen Chemie. 102., stark umgearbeitete und verb. Auflage. De Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- H. Caro: Zur Kenntniss der Oxydation aromatischer Amine. In: Zeitschrift für angewandte Chemie. Vol. 11, Nr. 36, 1898, S. 845–846, doi:10.1002/ange.18980113602.
- G. Brauer (Hrsg.): Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 388–389.
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 392.
- J.O. Edwards: SAFETY. In: Chem. & Eng. News. Vol. 33, Nr. 32, 1955, S. 3336, doi:10.1021/cen-v033n032.p3336.