Kava
Kava (Piper methysticum), auch Kava-Kava (Kawa-Kawa) oder Rauschpfeffer genannt, ist eine Pflanzenart aus der Gattung Pfeffer in der Familie der Pfeffergewächse (Piperaceae). Aus Pflanzenbestandteilen (meist getrocknet und pulverisiert) wird ein traditionelles Getränk des westpazifischen Raumes hergestellt, das vor allem als Zeremonialgetränk bei religiösen und kulturellen Anlässen konsumiert wird.
| Kava | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|

Kava (Piper methysticum) | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Piper methysticum | ||||||||||||
| G.Forst. |


Pflanzenbeschreibung
Die Kava ist mit dem Schwarzen Pfeffer verwandt und ähnelt diesem sowohl im Habitus als auch im pfefferartigen Geschmack.
Die Kava erreicht als immergrüner Strauch Wuchshöhen bis etwa 2–4 Meter. Sie bildet Rhizome. Die Pflanze ist zweihäusig diözisch.
Sie hat wechselständige, herzförmige, bis 20–30 Zentimeter große, ganzrandige und gestielte, spitze Laubblätter. Die Blätter sind kahl bis leicht behaart. Die Nervatur ist handförmig mit bis zu 13 Hauptadern. Es sind Nebenblätter vorhanden.
Es werden kurze, achsel- oder blattgegenständige und vielblütige, dichte, ährige Blütenstände gebildet. Die sehr kleinen, eingeschlechtlichen und grünlich-weißen bis gelblichen Blüten sind ohne Blütenhülle. Die männlichen Blüten besitzen zwei Staubblätter, die weiblichen einen einkammerigen, oberständigen Fruchtknoten mit sitzenden Narben. Die Pflanze bildet nur selten weibliche Blüten; diese bleiben auch bei Handbestäubung durch den Menschen steril. Die Pflanze wird ungeschlechtlich vermehrt. Selten werden jedoch einsamige Beeren gebildet.
Die Chromosomenzahl beträgt 2n = etwa 130.[1]
Verbreitung und Geschichte
Da die Pflanze seit langem in Kultur ist, ist die ursprüngliche Heimat der Kava nicht gesichert. Überwiegend wird vermutet, dass sie auf den Fidschi-Inseln und weiteren Inseln des südlichen Pazifik heimisch ist, aber möglicherweise stammt die Pflanze auch ursprünglich aus Neuguinea. Die ersten Europäer, die von der Pflanze und auch ihrer Nutzung als Zeremonialgetränk berichteten, waren die niederländischen Entdecker Jacob Le Maire und Willem Cornelisz Schouten. Sie sichteten diese auf den Horn-Inseln, die heute politisch zum französischen Überseeterritorium Wallis und Futuna gehören.
Der Name „Kava(-kava)“ stammt aus dem Tongaischen und Marquesischen;[2] andere Namen sind ʻawa (Hawaiʻi), ʻava (Samoa), yaqona (Fidschi), und sakau (Pohnpei).
Zubereitung und Anwendung
Kava wird traditionell auf verschiedene Arten in vielen Kulturen des westpazifischen Raumes konsumiert, so zum Beispiel in Polynesien, Vanuatu, Melanesien und Teilen von Micronesien und Australien, wird jedoch auch in vielen westlichen Kulturen als Medizin oder als Genussmittel konsumiert.
Traditionelle Anwendung und Zubereitung
Traditionell werden frische oder getrocknete Bestandteile der Kava-Wurzel mit Wasser aufgegossen. Meist wird zur Gewinnung der Wurzelstock des Rauschpfeffers („Piperis methystici rhizoma“) zu einem feinen Pulver zerrieben oder in einem Mörser zerstoßen; manchmal werden auch Pflanzenteile gekaut und in ein Gefäß gespuckt. Wird die ganze Pflanze bei der Herstellung verwendet und geknetet, enthält das Kava-Getränk später auch ein speichelflussförderndes Enzym. In manchen Kulturen wird es hingegen auch frisch gekaut, welches einen stärkeren Effekt hervorruft. Frisches Kava gilt gegenüber getrocknetem, industrieverarbeitetem Kava als potenter. Die Potenz hängt von Sorte und Kultivation ab. Es wird sowohl mit heißem als auch kaltem Wasser konsumiert. Oft wird Kava aus halbierten Kokosnussschalen getrunken. Der Geschmack ist leicht scharf; das eigentliche Aroma hängt stark davon ab, ob zur Herstellung frische oder getrocknete Pflanzen verwendet wurden. Die Farbe ist grau bis grünlich.
In den traditionellen Gesellschaften Polynesiens, Mikronesiens und auch Melanesiens war und ist der Konsum von Kava in der Regel reine Männersache, auch wenn es in touristisch gut erschlossenen Gebieten auf Tahiti, Fidschi oder Guam auch bei rein folkloristischen Anlässen männlichen wie weiblichen Gästen angeboten wird.
Auf Hawaii wurden rund 30 verschiedene Kavasorten für medizinische, religiöse, politische, kulturelle und soziale Zwecke von allen sozialen Klassen genutzt – sowohl von Männern als auch von Frauen. Kava hatte dort eine ähnliche Rolle wie Bier als Feierabendgetränk zum Entspannen und Lockern von Muskeln. Auch unruhigen Kleinkindern wurde Kava verabreicht, um sie zu beruhigen und besser schlafen zu lassen.
Auf vielen austronesischen Inseln war das gemeinschaftliche Kavatrinken eine ursprünglich sehr intime und religiöse Zeremonie.
Auf Nauru wurde sie als Initiationsritual für junge Männer genutzt. Auch heute noch spielt das Kava-Ritual auf Nauru eine wichtige, meist festliche Rolle.
Auf Vanuatu wird Kava nachts an einem Ort namens „Nakamal“ („Ort des Friedens“) getrunken. Männer trinken Kava dort aus Muscheln oder leeren Kokosschalen; Frauen war der Genuss von Kava ursprünglich verboten. In der traditionellen Medizin wird eine andere Kavasorte gegen Fieber, Asthma und Schmerzen aller Art verabreicht.
Auf Pohnpei, einer mikronesischen Insel, wird Kava unter dem Namen Sakau aus Kokosnussschalen konsumiert. Vor allem im zeremoniellen und rituellen Bereich ist die Pflanze bedeutend. Neben der Konsumption stellt auch die Produktion des Extraktes eine wichtige soziale Handlung dar. Davon abgesehen findet man auf Pohnpei zahlreiche öffentliche Sakau-Bars.[3]
Moderne Anwendung
Heutzutage wird es auch über das Ursprungsgebiet von Kava hinaus konsumiert – als Medizin oder als Genussmittel. So finden sich zum Beispiel Kava-Bars in vielen US-Staaten. Hierbei werden üblicherweise weiterhin nur Produkte konsumiert, die aus der Wurzel gewonnen werden – so zum Beispiel Wurzelpulver oder Extrakte. Es wird sowohl mit Wasser aufgegossen oder mit Milch o. Ä. konsumiert. Oft wird Lecithin hinzugefügt, um eine bessere Auflösung der Kavapyrone in Wasser zu erreichen.
Es wird auch als Softdrink vertrieben, so in Rzo in Hawaii (ausgesprochen „rizzo“)[4] oder Bula in den USA.[5] Das mit seiner beruhigenden Wirkung beworbene Getränk „Lava Cola“ (auch genannt Kava Cola) ist seit 2009 im pazifischen Vanuatu und anderen Ländern erhältlich.[6][7][8][9]
Kava ist in vielen Ländern in pharmazeutischen Erzeugnissen erhältlich und wird als Medikament genutzt. In Deutschland wurde Kava-Wurzelstockextrakt bis 2002 zur Behandlung von leichten allgemeinen Angstzuständen eingesetzt. Handelsnamen waren Antares, Neuronika, Kava-ratiopharm, Kavosporal forte oder Kavatino.
Inhaltsstoffe
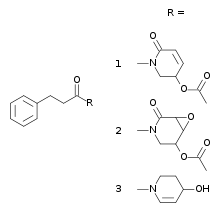
Die 2 bis 10 kg schweren, sehr saftigen Wurzelstöcke der Kava-Pflanze enthalten zwischen 3 und 20 % Kavapyrone. Der Gesamtgehalt schwankt in Abhängigkeit vom Standort und der Unterart. Weitere Bestandteile sind Stärke (43 %), Rohfaser (20 %), Wasser (12 %), Zucker (3,2 %), Proteine (3,6 %) und Mineralstoffe (3,2 %). Außerdem enthalten die Wurzeln Flavokavin A und B sowie geringe Mengen an Sitosterol, Stigmastendion und Cepharadion A nebst geringen Mengen ätherischer Öle, sowie einige organische Säuren (zum Beispiel: Oxo-n-nonansäure, Phenylessigsäure, Zimtsäure, p-Methoxyphenylessigsäure).[10][11]
Die sichtbaren Pflanzenteile (Blätter, Rinde) dagegen enthalten zusätzlich zu den Kavapyronen die Piperidin-Alkaloide Pipermethystin (0,2 bis 0,8 % in der Rinde, 1 bis 2,4 % in den Blättern), 3a,4a-Epoxy-5b-Pipermethystin (nur in cv. 'Isa') und Awain (nur in geschlossenen Blättern, 0,1 bis 2,6 %), welche vermutlich zu Leberschäden beitragen. In kommerziell erhältlichen Zubereitungen der Wurzeln sind diese Alkaloide nicht enthalten.
Wirkung
Die Kavapyrone (Kavain, Methysticin) aus Wurzeln und Rinde der Kava-Pflanze wirken anxiolytisch, mindern also Angst- und Spannungszustände. Bei Sozialphobie zeigte es sich dem Placebo überlegen.[12] Auch hat Kava leichte analgetische (schmerzstillende) und antioxidante Wirkung. Der Genuss von Kava entspannt und mindert Unruhen; er führt zu leichter Euphorie und Gesprächigkeit.[13] Kava löst Muskelverkrampfungen; Konsumenten fühlen sich in der Regel entspannt, wohl und klar denkend. Auf den Konsum schläft man in der Regel erholsam, und es gibt keine Nachwirkungen am Folgetag, solange die Zubereitung keinen Alkohol enthält.
Nebenwirkungen können leichte vorübergehende Taubheitsgefühle in Lippen und Zunge sein, vermindertes Sehvermögen, eingeschränkte Reaktionsfähigkeit, eine Gelbfärbung der Haut und allgemein allergische Hautreaktionen. Kava sollte in der Schwangerschaft und Stillzeit nicht angewandt werden. Bei hohem Konsum und langer Einnahmedauer sowie vorbestehenden Leberschäden kann Kava zu Gewichtsverlust, Unterernährung, Leberschäden, Nierenschäden, Ausschlag, Pulmonale Hypertonie, Makrozytose, Lymphopenie und verminderten Thrombozyten-Volumen führen.[14]
Kontroverse um Leberschäden
In Deutschland wurden kavahaltige Medikamente 2001 vom Markt genommen, nachdem das Auftreten von Leberschäden beobachtet worden war. Es wurde vermutet, dass in der Arzneimittelherstellung eine eventuelle Mitverwendung von „peelings“ (Rinde), welche im Gegensatz zu den in der traditionellen Verwendung benutzten Kava-Wurzel das Alkaloid Pipermethystin enthalten soll, die Ursache für das Auftreten von Leberschäden sei.[15][16][17][18] Mittlerweile gilt diese Hypothese als überholt. Zwar hat sich gezeigt, dass Pipermethystin Leberschäden hervorrufen kann.[16] Jedoch ergab eine Analyse von Rückstellmustern der deutschen Kava-Medikamente, dass Pipermethystin nicht in relevanten Mengen enthalten war.[19] In einer Tierstudie an Ratten mit einem ethanolischen Kava-Extrakt konnte keine lebertoxische Wirkung festgestellt werden.[16] Eine andere Vermutung ist daher, dass die Leberschäden durch vorher bestehende Erkrankungen oder durch mögliche Verunreinigungen der Arzneimittel mit Aflatoxinen oder andere leberschädigenden Mykotoxinen, verursacht durch Schimmel und Bakterien, ausgelöst sein könnten. Studien hierzu stehen jedoch bisher aus.[20]
Eine Vergiftung durch synthetische Enantiomere könnte ebenfalls eine mögliche Ursache sein, wie eine 2011 veröffentlichte Dissertation zeigt. Die in Deutschland hergestellten Medikamente (wie z. B. das Arzneimittel Laitan) enthielten nicht nur natürliche Stoffe, sondern aus Kostengründen auch synthetisiertes Kavain.[21] Künstlich produziertes Kavain ist eine racemische Mischung aus (+)-Kavain und (−)-Kavain (auch als DL-Kavain bezeichnet). Die Kava-Pflanze enthält nur (+)-Kavain. In der Arbeit wurde gezeigt, dass (−)-Kavain zu gesundheitsschädlichen para-Hydroxy-Verbindungen abgebaut wird. Dies würde erklären, warum hepatotoxische Fälle hauptsächlich im deutschsprachigen Raum aufgetreten sind, während die Hepatotoxizität im pazifischen Raum so gut wie unbekannt ist. Auch die bisherigen Unterschiede zur Hepatotoxizität in der wissenschaftlichen Literatur könnten verständlich werden, da die Autoren nicht explizit angeben, ob das untersuchte Kavain synthetisch ist oder aus der Kava-Pflanze stammt.[22]
Rechtliche Lage
Am 14. Juni 2002 widerrief das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) die Zulassung für Kava-Kava- und Kavain-haltige Arzneimittel. Es reagierte damit auf 40 dokumentierte Fälle von schwerwiegenden Leberschädigungen, darunter sechs Fälle mit beträchtlichem Leberversagen mit Erfordernis einer Transplantation und drei Fälle mit tödlichem Verlauf, bei denen die Einnahme von Kava-Präparaten vorlag.
Über diese Entscheidung des BfArMs äußerten die Mitglieder der das BfArM beratenden Kommission E ihr Befremden. Sie bewerteten die therapeutische Wirksamkeit und das Nutzen-Risiko-Verhältnis der aus dem Rhizom gewonnenen Kava-Arzneimittel für den Patienten im Gegensatz zum BfArM positiv und sahen keine Gefahr im Verzug, die eine solche Maßnahme rechtfertigen könne.[23] Die Ursache für die eingetretenen Leberschädigungen in früheren Studien basiere auf Überdosierungen und einer zu langen Einnahmedauer, durch vorher bestehende Erkrankungen oder mögliche Verunreinigungen durch Aflatoxine oder andere leberschädigende Mykotoxine; nur in sehr wenigen Einzelfällen sei bei ordnungsgemäßer Behandlung mit Kava ein kausaler Zusammenhang zu Leberschädigungen als wahrscheinlich einzustufen.[20][24]
Nach einem Widerspruch der Hersteller wurde vom BfArM am 12. Mai 2005 als minderschwere Maßnahme das befristete Ruhen der Zulassung angeordnet, wodurch den Unternehmen die Möglichkeit gegeben werden sollte, durch geeignete Studien die Wirksamkeit und Unbedenklichkeit der Kava-Präparate nachzuweisen. Es gelang den Unternehmen jedoch nicht, die Unbedenklichkeit in geeigneten Tierversuchen hinreichend nachzuweisen, was eine Voraussetzung für die Genehmigung und Durchführung klinischer Studien gewesen wäre. Somit konnte keine neue Nutzen-Risiken-Bewertung vorgenommen werden. Das BfArM kam zum Ergebnis, dass dem Risiko keine ausreichend belegte, angemessene therapeutische Wirksamkeit in den beanspruchten Indikationen gegenüberstehe, und ferner therapeutische Alternativen bestünden, deren Wirksamkeit in den in Frage stehenden Anwendungsgebieten erwiesen sei.
Es widerrief am 21. Dezember 2007 die Zulassung erneut. Davon sind nicht nur Fertigarzneimittel, sondern auch Einzelzubereitungen und der Verkauf der Arzneidroge betroffen. Ausgenommen sind lediglich homöopathische Zubereitungen mit einer Endkonzentration geringer als D4.[25] Auf Klagen der pharmazeutischen Hersteller hob das Verwaltungsgericht Köln im Mai 2014 den Widerrufsbescheid mit der Begründung auf, das Nutzen-Risiko-Verhältnis der streitigen Kava-Kava-haltigen Arzneimittel sei nicht ungünstig.[26]
Das Oberverwaltungsgericht Nordrhein-Westfalen hat im Februar 2015 die Berufung zurückgewiesen und das erstinstanzliche Urteil des VG Köln bestätigt. Die Voraussetzungen für einen Zulassungswiderruf seien nicht erfüllt. Das Nutzen-Risiko-Verhältnis sei nicht ungünstig, wenn bestimmte Änderungen in den Zulassungen vorgenommen würden, um die Risiken bestmöglich einzudämmen. Die therapeutische Wirksamkeit der Arzneimittel sei zu bejahen. Für deren Nutzen spreche auch, dass es sich bei Angststörungen um eine ernsthafte, weitverbreitete und behandlungsbedürftige psychische Erkrankung handele. Es bestünden zwar Anwendungsrisiken in Form hepatotoxischer (leberschädigender) Ereignisse. Die Zahl gemeldeter Fälle im Verhältnis zum Anwendungsvolumen der Arzneimittel sei aber gering und das Ursache-Wirkungs-Verhältnis vielfach fraglich. Entscheidend sei, dass die lebertoxischen Risiken bei Beachtung bestimmter Maßnahmen auf ein vertretbares Maß reduziert werden könnten. Hierzu zählten die seit 2002 bestehende ärztliche Verschreibungspflicht, die Begrenzung der maximalen Tagesdosis und der Anwendungsdauer, die regelmäßige Bestimmung der Leberwerte und die Vermeidung von Alkohol sowie einer begleitenden Medikation insbesondere mit Betablockern, Antidepressiva und Migränemitteln. ("Soweit die bisher umgesetzten Maßnahmen dem nicht genügten, komme kein Widerruf in Betracht, sondern müsse die Zulassung angepasst werden.")[27]
Die Arzneimittelbehörden der Schweiz (Swissmedic),[28] Frankreichs (AFSSAPS), der Niederlande (CBG)[29] und die britische MHRA[30] kamen zur gleichen Bewertung aufgrund des damaligen Verdachts. Diese Einschätzungen decken sich jedoch nicht mit denen anderer Arzneimittelbehörden: In den USA ist Kava frei erhältlich, wie auch in den meisten Teilen Australiens. Die australische Therapeutic Goods Administration hat jedoch eine Empfehlung ausgesprochen, nach der Konsumenten nicht mehr als das Kava-Äquivalent von 250 mg Kavapyronen pro Tag konsumieren sollten.[31]
2019 widerrief das BfArM erneut die Zulassung.[32]
Literatur
- Hermann Mückler: Kava in Ozeanien: Neue Betrachtungen zu einer Kulturpflanze und deren Bedeutung im kulturellen Kontext. In: Mitteilungen der Anthropologischen Gesellschaft Wien. Band CXXV, Wien 1996, S. 207–224.
- Ingrid und Peter Schönfelder: Das neue Buch der Heilpflanzen. Botanik, Arzneidrogen, Wirkstoffe, Anwendungen. Franckh-Kosmos, Stuttgart 2011, ISBN 978-3-440-12932-6.
- Lutz Roth, Max Daunderer, Kurt Kormann: Giftpflanzen Pflanzengifte. 6. Auflage. Nikol, Hamburg 2012, ISBN 978-3-86820-009-6.
- Angelika Prentner: Bewusstseinsverändernde Pflanzen von A-Z. Springer, Wien / New York, NY 2004, ISBN 3-211-23524-8.
Studien
- F. Pantano, R. Tittarelli u. a.: Hepatotoxicity Induced by "the 3Ks": Kava, Kratom and Khat. In: International journal of molecular sciences. Band 17, Nummer 4, 2016, S. , doi:10.3390/ijms17040580, PMID 27092496, PMC 4849036 (freier Volltext) (Review).
- L. R. Olsen, M. P. Grillo, C. Skonberg: Constituents in kava extracts potentially involved in hepatotoxicity: a review. In: Chemical research in toxicology. Band 24, Nummer 7, Juli 2011, S. 992–1002, doi:10.1021/tx100412m, PMID 21506562 (Review).
- R. Teschke: Kava hepatotoxicity–a clinical review. In: Annals of hepatology. Band 9, Nummer 3, 2010 Jul–Sep, S. 251–265, PMID 20720265 (Review).
Weblinks
- Eintrag bei GRIN Taxonomy for Plants (englisch)
- Pharmazeutische Zeitung online: Kava-Kava: Comeback unter strengen Auflagen. In: pharmazeutische-zeitung.de. 31. Dezember 2015, abgerufen am 6. August 2016.
- Bundesinstitut für Arzneimittel und Medizinprodukte: Kava-Kava Patientenheft (PDF, 64 KB). In: bfarm.de. 23. März 2015, abgerufen am 6. August 2016.
- Bundesinstitut für Arzneimittel und Medizinprodukte: Risikobewertungsverfahren: Kava-Kava-haltige Arzneimittel: Risiko für das Auftreten schwerer Leberreaktionen, Änderung der betroffenen Zulassungen. Abgerufen am 9. September 2019.
Einzelnachweise
- Piper methysticum bei Tropicos.org. In: IPCN Chromosome Reports. Missouri Botanical Garden, St. Louis.
- kava. In: Merriam–Webster Online Dictionary (2010).
- Augustine Kohler: Sakau – Pohnpei’s communal narcotic. In: Charting the Pacific. ABC radio Australia, abgerufen am 24. Mai 2008.
- http://rzorzo.com
- Kalm with Kava - Premium Kava and Relaxation Drinks. In: Kalm with Kava.
- Van Beverage releases new kava drink. (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis. In: Vanuatu Daily Post, 4. Oktober 2009.
- Vanuatu has high hopes for new Kava based Lava Kola. ABC Radio Australia, 18. März 2010.
- Kava cola, Vanuatu’s answer to energy drinks (Memento vom 29. Februar 2012 im Internet Archive)
- Advertisement for Lava Cola, focusing on its relaxing effect, on the official YouTube channel of the Vanuatu Kava Store
- Rudolf Hänsel: Kava-Kava in der modernen Arzneimittelforschung. In: Zeitschrift für Phytotherapie, 17, 1996, S. 180–194.
- A. Lopez-Avila, J. Benedicto: Supercritical Fluid Extraction of Kava Lactones from Piper methysticium (Kava) Herb. In: J.High. Resol. Chromatogr., 20, 1997, S. 555–559.
- Pittler MH, Ernst E: Kava extract for treating anxiety. In: Cochrane database of systematic reviews (Online). Nr. 1, 2003, S. CD003383. doi:10.1002/14651858.CD003383. PMID 12535473.
- Kava: Keine Angst vor guter Laune. In: Wechselwirkung
- Fu PP, Xia Q, Guo L, Yu H, Chan PC: Toxicity of kava kava. In: J Environ Sci Health C Environ Carcinog Ecotoxicol Rev. 26, Nr. 1, 2008, S. 89–112. doi:10.1080/10590500801907407. PMID 18322868. (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis.
- Klaus Dragulla, Wesley Y. Yoshidab, Chung-Shih Tang: Piperidine alkaloids from Piper methysticum. In: Phytochemistry, 2003, 63/2, S. 193–198, doi:10.1016/S0031-9422(03)00111-0, PDF (Memento des Originals vom 15. Dezember 2006 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- Sorrentino L, Capasso A, Schmidt M: Safety of ethanolic kava extract: Results of a study of chronic toxicity in rats. In: Phytomedicine. 13, Nr. 8, September 2006, S. 542–9. doi:10.1016/j.phymed.2006.01.006. PMID 16904878.
- Pratibha V. Nerurkar u. a.: In Vitro Toxicity of Kava Alkaloid, Pipermethystine, in HepG2 Cells Compared to Kavalactones. In: Toxicological Sciences, 79/-, 2004, S. 106–111, oxfordjournals.org
- New Evidence Links Kava To Liver Damage.
- M Lechtenberg, B Quandt, M Schmidt, A Nahrstedt: Is the alkaloid pipermethystine connected with the claimed liver toxicity of Kava products? In: Pharmazie, 63 (1), 2008, S. 71–74, PMID 18271308.
- R. Teschke, S.X. Qiu, V. Lebot: Herbal hepatotoxicity by kava: Update on pipermethystine, flavokavain B, and mould hepatotoxins as primarily assumed culprits. In: Digestive and Liver Disease, 2011 [Article in Press]
- Stufenplanverfahren Stufe II zur Abwehr von Arzneimittelrisiken im Zusammenhang mit Kava-Kava- und Kavain-haltigen Arzneimitteln. Bescheid des BfArM vom 14. Juni 2002 (PDF)
- Yann Barguil: Etude de trois plantes psychotropes consommées en Nouvelle-Calédonie: kava, cannabis et datura : Aspects médicaux et médico-légaux, S. 16, 19, 36f., 45f., 51ff. (PDF; 2,9 MB) Nouméa : Université de la Nouvelle-Calédonie, 2011. – Dissertation
- Statement der Kommission E: Zitatauszug (Memento des Originals vom 29. November 2014 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- R. Teschke, W. Gaus, D. Loew: Kava extracts: safety and risks including rare hepatotoxicity. In: Phytomedicine : international journal of phytotherapy and phytopharmacology. Band 10, Nummer 5, 2003, S. 440–446, doi:10.1078/0944-7113-00314, PMID 12834011 (Review).
- Dokumente des BfArM zu Kava-haltigen Arzneimitteln. Archiviert vom Original am 11. Dezember 2012. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Abgerufen am 18. November 2014.
- Verwaltungsgericht Köln, 7 K 2128/12. Abgerufen am 30. Juni 2017.
- Oberverwaltungsgericht Nordrhein-Westfalen, Urteil vom 25. Februar 2015 (13A1371/14)
- Widerruf der Zulassungen von Arzneimitteln mit Kava-Kava und Kavain und Streichung von Kava-Kava und Kavain aus der Stoffliste C (Verfügung). In: Swissmedic Journal. Nr. 6, 2003, S. 492–495 (PDF [abgerufen am 26. Februar 2019]).
- C.I.J.M. Ross-van Dorp: Besluit van 23 april 2003, houdende wijziging van het Warenwetbesluit Kruidenpreparaten (verbod op Kava kava in kruidenpreparaten) (PDF) In: Sdu Uitgevers. Staatsblad van het Koninkrijk der Nederlanden. 2003. Archiviert vom Original am 27. Februar 2008. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Abgerufen am 7. Februar 2007.
- MHRA Expert Working Group on the safety of Kava. Archiviert vom Original am 14. April 2009. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Abgerufen am 18. November 2014.
- Kava fact sheet. Therapeutic Goods Administration, Government of Australia. 22. April 2005. Abgerufen am 26. Februar 2019.
- Celine Müller, Apothekerin, Redakteurin DAZ.online (cel): Endgültiges Aus für Kava-Kava. 27. Dezember 2019, abgerufen am 21. Oktober 2020.