Imidazole
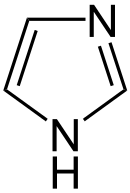
Imidazole sind eine chemische Stoffgruppe aus dem Bereich der heterocyclischen Verbindungen und gehören zur Gruppe der Azole. Ihre Mitglieder sind fünfgliedrige cyclische organische ungesättigte Verbindungen, die genau zwei nicht benachbarte Stickstoffatome im Ringgerüst tragen. Sie gehören zur Gruppe der Heteroaromaten und sind isomer zu den Pyrazolen. Das Stammsystem der Gruppe bildet das Imidazol.[1][2]
Vorkommen
Imidazole kommen vielfältig in der Natur vor. So enthält die Aminosäure Histidin und das davon abgeleitete Histamin einen Imidazolring, ebenso die Purine, die Xanthine und deren Derivate. Imidazolalkaloide kommen in Rautengewächsen vor.
Darstellung
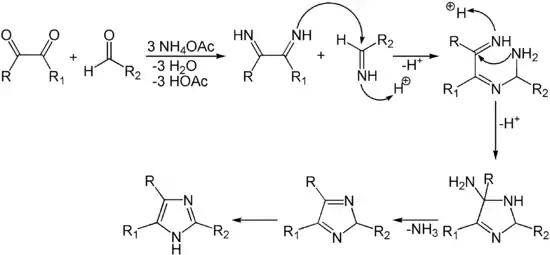
Die Synthese von Imidazolen kann ausgehend von α,β-Diketonen und Aldehyden geschehen. Hierzu werden alle Carbonylfunktionen zunächst mit Ammoniumacetat (NH4OAc) zu Iminen umgesetzt. Säurekatalysiert läuft nun die Kupplung eines Diiminstickstoffs an den Iminkohlenstoff unter Bildung eines Diiminoamins. Ebenfalls säurekatalysiert folgt nun der nucleophile Angriff des Aminstickstoffs am zweiten Iminkohlenstoff, wobei der Ring geschlossen wird. Die entstandene Aminofunktion wird nun als Ammoniak abgespalten, wodurch ein Diimin entsteht, welches dann zum Imidazol tautomerisiert.[1]
Eigenschaften
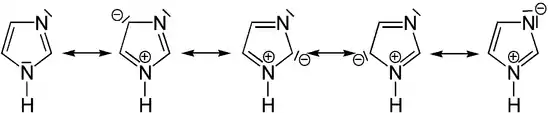
Imidazole besitzen sechs π-Elektronen, die ein mesomeres System bilden. Neben den zwei Doppelbindungen im Ring wird hierzu noch das freie Elektronenpaar des Aminstickstoffs hinzugenommen. Das freie Elektronenpaar des Iminstickstoffs kann nicht an der Mesomerie teilnehmen, da es sich in der Ringebene befindet und aus geometrischen Gründen nicht mit dem π-System ober- und unterhalb der Ringebene überlappen kann. Der Imidazolring ist planar, so dass Imidazole die Hückel-Kriterien erfüllen und aromatischen Charakter besitzen.[1][2]
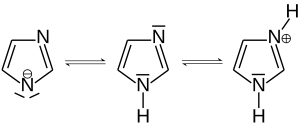
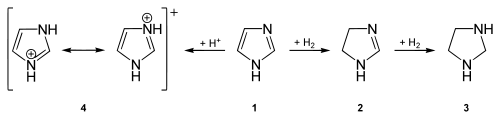
Imidazole besitzen wie alle Azole basischen Charakter. Der pKS-Wert von protoniertem Imidazol (Imidazolium-Ion) liegt bei 7,0.[1] Die im Vergleich zu Pyrazolen relativ hohe Basizität erklärt sich durch die cyclische Amidinstruktur. Zusätzlich können sie jedoch auch als Säuren auftreten, wobei das stickstoffgebundene Proton abgespalten werden kann, so dass sie zu den Ampholyten gehören.
Aus der teilweisen Hydrierung von Imidazolen entstehen Imidazoline (siehe auch Imidazolin-Rezeptor). Werden Imidazole vollständig hydriert, so entstehen Imidazolidine.[3]
Verwendung
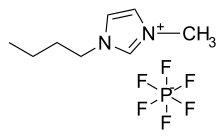
Aus Imidazol wird leicht das Imidazoliumkation gebildet. Derivate dieses Kations mit verschiedenen organischen Resten werden als ionische Flüssigkeiten eingesetzt. Bekannte Derivate sind z. B. Xylometazolin oder Clotrimazol.
Weblinks
Einzelnachweise
- D. T. Davies: Basistexte Chemie: Aromatische Heterocyclen, 1. Auflage, Wiley-VCH, Weinheim 1995, ISBN 3-527-29289-6.
- H. Beyer, W. Walter: Lehrbuch der Organischen Chemie, 23. Auflage, S. Hirzel Verlag, Stuttgart 1998, S. 753–876, ISBN 3-7776-0808-4.
- J. Falbe, M. Regitz (Hrsg.): Römpp Lexikon Chemie. 10. Aufl., Thieme, Stuttgart u. New York, 1996–1999. S. 1882.