Ergolin
Ergolin ist eine polycyclische, stickstoffhaltige organische chemische Verbindung. Diese Substanz wurde zuerst 1937 von Walter A. Jacobs und R. Gordon Gould Jr. beschrieben.[1] Sie ist das Grundgerüst des Großteils der Mutterkornalkaloide und zahlreicher weiterer voll- oder teilsynthetisch hergestellter Substanzen. Vom Ergolin strukturell abgeleitete Substanzen werden Ergoline bezeichnet und in der Medizin zur Behandlung der Migräne, der Parkinson-Krankheit sowie von Herz-Kreislauferkrankungen eingesetzt. Der Name wurde von der – vorwiegend im englischen Sprachraum verbreiteten – Bezeichnung Ergot für Sklerotien des Mutterkornpilzes Claviceps abgeleitet.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
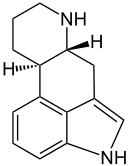 | ||||||||||
| Allgemeines | ||||||||||
| Name | Ergolin | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C14H16N2 | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 212,29 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
| |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Darstellung
Die Synthese von Ergolin basiert auf dem Aufbau eines tetrazyklischen Ringsystems ausgehend von Naphthalsäure.[1] In einem ersten Reaktionsschritt wird Naphthalsäure nach Leuck, Perkins und Whitmore zu 3-Nitro-1-naphthoesäure umgesetzt, welche in Gegenwart von Eisen(II)-sulfat und Ammoniak zu 3-Amino-1-naphthoesäure reduziert wird. In einer Skraup-Synthese wird die bicyclische 3-Amino-1-naphthoesäure durch säurekatalysierte Addition von Acrolein aus Glycerol um einen Ring zur 5,6-Benzochinolin-7-carbonsäure erweitert. Unter Zusatz von rauchender Salpetersäure wird die 5,6-Benzochinolin-7-carbonsäure zu 3′-Nitro-5,6-benzochinolin-7-carbonsäure nitriert. Das Reaktionsprodukt wird in Gegenwart von Eisen(II)-sulfat im alkalischen Milieu zum Amin reduziert. Nach Zusatz von Salzsäure erfolgt der Ringschluss zum entsprechenden Lactam, dem tetrazyklischen 3′-Amino-5,6-benzochinolin-7-carbonsäurelactam. Abschließend wird das Lactam mit elementarem Natrium in Butanol zum Endprodukt Ergolin reduziert.
Eigenschaften
Chemische Eigenschaften
Ergolin ist eine weiße pulvrig-kristalline Substanz, die sich leicht in Ethanol, Chloroform und Benzol löst. In Gegenwart von Ehrlichs Reagenz oder Van-Urk-Reagenz gibt Ergolin eine intensive Farbreaktion. Eine tiefe blau-violette Färbung kann in Gegenwart von Kellers Reagenz beobachtet werden.[1]
Stereochemie
Ergolin besitzt zwei Stereozentren. Somit existieren rechnerisch 4 Stereoisomere des Ergolins. Alle natürlich vorkommenden und alle therapeutisch genutzten Derivate des Ergolins besitzen eine 5R-Konfiguration.
Einzelnachweise
- Jacobs WA, Gould Jr. RG: The ergot alkaloids: XII. The synthesis of substances related to lyseric acid. In: J. Biol. Chem. 120, Nr. 1, 1937, S. 141–150.
- W. A. Jacobs, R. G. Gould: THE SYNTHESIS OF SUBSTANCES RELATED TO LYSERGIC ACID. In: Science. Band 85, Nummer 2201, März 1937, S. 248–249, doi:10.1126/science.85.2201.248, PMID 17841382.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.