Skraup-Synthese
Die Skraup-Synthese wurde nach dem tschechisch-österreichischen Chemiker Zdenko Hans Skraup (1850–1910) benannt, und beschreibt die Synthese von Chinolin und dessen Derivaten aus Anilin, Schwefelsäure, Eisen(II)-sulfat und Glycerin. Die Dehydrierung der Zwischenstufe 1,2-Dihydrochinolin erfolgt durch Nitrobenzol.
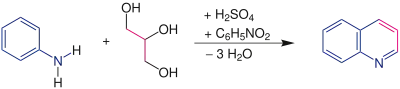
Reaktionsmechanismus
α,β-ungesättigte Carbonylverbindungen (Aldehyde, Ketone) reagieren durch eine säurekatalysierte Addition mit aromatischen Aminen zu Chinolin. Die zur Synthese benötigten α,β-ungesättigten Carbonylverbindungen werden häufig erst in einem separaten Syntheseschritt dargestellt (z. B. Crotonaldehyd aus Paraldehyd oder Acrolein aus Glycerin).
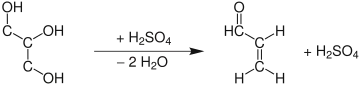
Erst im nächsten Schritt wird das Amin addiert. Anschließend erfolgt die säurekatalysierte Aldehydkondensation mit dem aromatischen Kern und bildet das Dihydrochinolin.
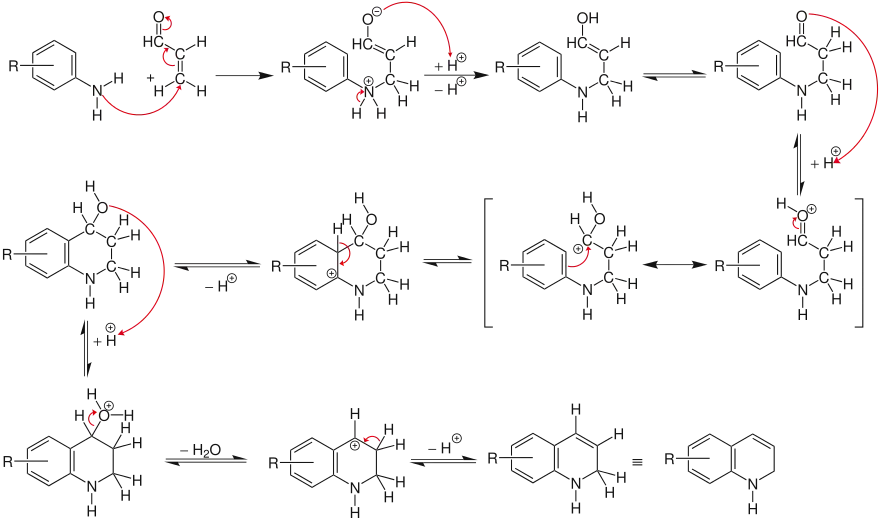
Anschließend wird das Dihydrochinolin durch Nitrobenzol zum aromatischen Chinolin dehydriert, wobei das Nitrobenzol reduziert wird.
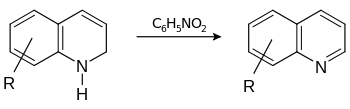
Variante
Wird das gebildete Dihydrochinolin zum Tetrahydrochinolin und Chinolinderivat disproportioniert, so handelt es sich um eine Doebner-Miller-Synthese.
Quellen
- Organikum, VEB Deutscher Verlag der Wissenschaften, Berlin 1976
- Adalbert Wollrab: Organische Chemie: Eine Einführung für Lehramts- und Nebenfachstudenten. Springer, 2002, S. 984.