Enfluran
Enfluran (Handelsname auch Ethrane) ist ein dem Halothan ähnliches volatiles Anästhetikum aus der Gruppe der Flurane. Es hat eine gute hypnotische und muskelrelaxierende, jedoch nur schwache analgetische Wirkung. Es wird, unter anderem wegen seiner geringen kardiovaskulären[4] Sicherheitsbreite, weltweit nicht mehr verwendet.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
-1%252C1%252C2-trifluoroethane_200.svg.png.webp) | ||||||||||||||||||||||
| Vereinfachte Strukturformel ohne Stereochemie 1:1-Gemisch von (S)-Form und (R)-Form | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Enfluran | |||||||||||||||||||||
| Andere Namen |
(RS)-2-Chlor-1-difluormethoxy-1,1,2-trifluorethan | |||||||||||||||||||||
| Summenformel | C3H2ClF5O | |||||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit mildem, süßlichen Geruch[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
N01AB04 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 184,49 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||||||||
| Dichte |
1,5167 g·cm−3 (25 °C)[1] | |||||||||||||||||||||
| Siedepunkt |
56,5 °C[1] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Brechungsindex |
1,3025 (20 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
150 mg·m−3 [1] | |||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Treibhauspotential |
705 (bezogen auf 100 Jahre)[3] | |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Pharmakologie
Der Blut-Gas-Verteilungskoeffizient von Enfluran ist 1,9, das heißt bei einer Konzentration von 1 Volumenprozent (Vol.-%) in den Lungenbläschen beträgt die Konzentration im Blut 1,9 Vol.-%. Daraus resultiert eine mittelschnelle Einschlaf- und Aufwachphase. Die minimale alveoläre Konzentration ist 1,68 %, Enfluran ist damit etwa so potent wie Isofluran. Enfluran ist nur wenig schleimhautreizend.
Die Metabolisierungsrate von Enfluran beträgt 2–3 %, wodurch die Wahrscheinlichkeit einer Leberschädigung gering ist. Die Bedeutung der dabei entstehenden Fluoridverbindungen ist noch nicht geklärt. Enfluran erhöht die Krampfbereitschaft, Muskelzuckungen bis Myoklonien sowie epileptiforme Anfälle, insbesondere im Zusammenhang mit einer Hyperventilation, sind beschrieben. Die blutdrucksenkende Wirkung von Enfluran ist im Vergleich zu den anderen Inhalationsanästhetika stärker ausgeprägt. Wie die anderen Inhalationsanästhetika erhöht Enfluran den Hirndruck und ist Trigger einer malignen Hyperthermie sowie der Porphyrie.
Chemie
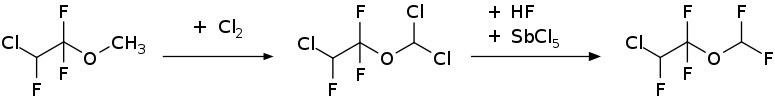
Enfluran ist chiral, es wird als Racemat [1:1-Gemisch aus (S)-Enfluran und (R)-Enfluran] eingesetzt. Es handelt sich um eine farblose Flüssigkeit, die bei Normaldruck bei 56,8 °C siedet. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend ln(P) = A−(B/(T+C)) (P in kPa, T in K) mit A = 14.10102, B = 2573.403 und C = −58,600 im Temperaturbereich von 274,04 bis 351,76 K.[5] Die molare Verdampfungsenthalpie beträgt am Siedepunkt 30,2 kJ·mol−1.[6] Die kritische Temperatur liegt bei 201,9 °C, der kritische Druck bei 29,80 bar.[5] Die Synthese von Enfluran geht vom 2-Chlor-1,1,2-trifluorethylmethylether aus. Mittels einer photochemischen Chlorierung wird im ersten Schritt der 2-Chlor-1,1,2-trifluorethyldichlormethylether erhalten. Ein anschließender Halogenaustausch mittels Fluorwasserstoff oder Antimontrifluorid in Gegenwart von Antimonpentachlorid ergibt die Zielverbindung. Aus der Synthesesequenz resultiert das Racemat.[7]
Einzelnachweise
- Eintrag zu Enfluran in der GESTIS-Stoffdatenbank des IFA, abgerufen am 11. April 2020. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-228.
- G. Myhre, D. Shindell et al.: Climate Change 2013: The Physical Science Basis. Working Group I contribution to the IPCC Fifth Assessment Report. Hrsg.: Intergovernmental Panel on Climate Change. 2013, Chapter 8: Anthropogenic and Natural Radiative Forcing, S. 24–39; Table 8.SM.16 (PDF).
- Reinhard Larsen: Anästhesie und Intensivmedizin in Herz-, Thorax- und Gefäßchirurgie. (1. Auflage 1986) 5. Auflage. Springer, Berlin/ Heidelberg/ New York u. a. 1999, ISBN 3-540-65024-5, S. 6–8.
- Ambrose, D.; Ghiassee, N.B.: Vapour pressures, critical temperatures, and critical pressures of 2-chloro-1,1,2-trifluoroethyl difluoromethyl ether (enflurane) and of 1-chloro-2,2,2-trifluoroethyl difluoromethyl ether (isoflurane) in J. Chem. Thermodyn. 20 (1988) 765–766.
- Uchytilová, V.; Majer, V.; Svoboda, V.; Hemer, I.: Enthalpies of vaporization and cohesive energies of 2-chloro-1,1,2-trifluoroethyl ethyl ether, 2-chloro-1,1,2-trifluoroethyl propyl ether, 2-chloro-1,1,2-trifluoroethyl chloromethyl ether, and 2-chloro-1,1,2-trifluoroethyl difluoromethyl ether in J. Chem. Thermodyn. 16 (1984) 475–479, doi:10.1016/0021-9614(84)90205-2.
- Axel Kleemann, Jürgen Engel, Bernd Kutscher, Dietmar Reichert: Pharmaceutical Substances. Syntheses, Patents, Applications. 2 Bände. 4. Auflage. Thieme, Stuttgart u. a. 2001, ISBN 1-58890-031-2; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.