Conrad-Limpach-Chinolinsynthese
Die Conrad-Limpach-Chinolinsysnthese ist eine Namensreaktion aus dem Bereich der organischen Chemie und wurde 1887 von Max Conrad (1848–1920) und Leonhard Limpach (1852–1933) beschrieben.[1] Dabei findet unter Abspaltung von Wasser und Alkohol eine Kondensation von Anilin mit einem β-Ketoester zu einem 4-Hydroxychinolin[2] statt.[3]
Übersichtsreaktion
Die Conrad-Limpach-Chinolinsynthese wird in saurer, wässriger Lösung ausgeführt.
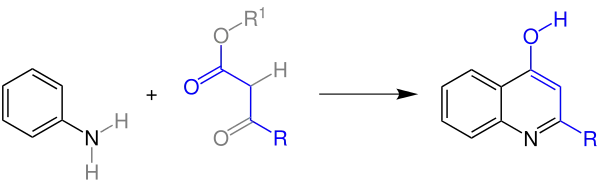
Die grau eingezeichneten Atome verlassen bei der Reaktion das Molekül und die blau eingezeichnete Verbindung steht für die neu geknüpfte Bindung des Anilins mit dem β-Ketoester zu einem Heteroaromaten, einem Chinolinderivat. Der Rest R kann dabei für einen organischen Rest stehen.
Möglicher Mechanismus
Der folgende Mechanismus der Conrad-Limpach-Chinolinsynthese wird anhand von Anilin und β-Propanoethylester und Chlorwasserstoff (HCl) erklärt.[3]
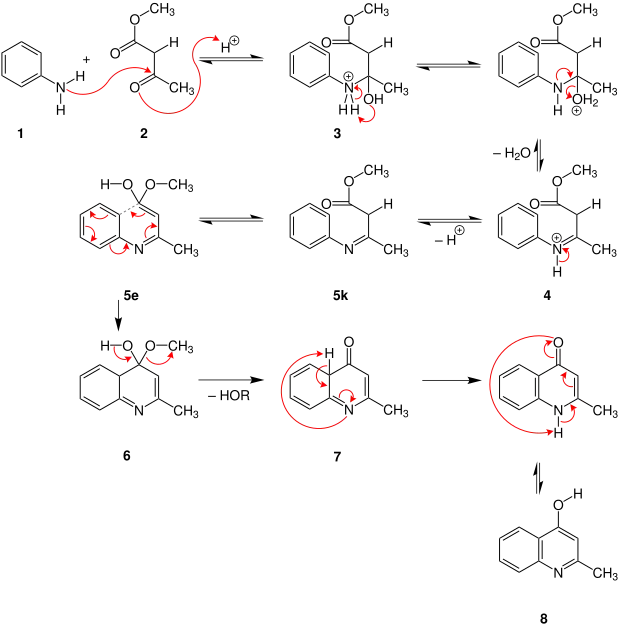
Das Anilin (1) greift an der Ketogruppe von Methylacetoacetat (2) nukleophil an, während die Ketogruppe protoniert wird. Dadurch entsteht das Kation 3. Durch interne Umlagerung des Protons und anschließender Wasserabspaltung entsteht das Kation 4. Durch Deprotonierung am Stickstoff entsteht das Zwischenprodukt 5k.Die Carbonylgruppe tautomerisiert durch die Keto-Enol-Tautomerie zur Alkoholgruppe und das Molekül somit zum Enol 5e. Elektronenwanderungen erzeugen einen Ringschluss zum Intermediat 6. Nach Abspaltung von Methanol entsteht das Zwischenprodukt 7, welches durch erneute interne Umlagerung des Protons aromatisiert wird und somit das Endprodukt 4-Hydroxy-2-methyl-chinolin (8) gebildet wird.
Literatur
- Bradford P. Mundy, Michael G. Ellerd, Frang G. Favaloro Jr.: Name Reactions and Reagents in Organic Synthesis. 2. Auflage. John Wiley & Sons, New York 2005, ISBN 0-471-22854-0, S. 134–135.
- Martha Windholz: The Merck Index. 9. Auflage. Merck & Co., New Jersey 1976, ISBN 0-911910-26-3, S. 19.
Einzelnachweise
- M. Conrad, L. Limpach: Ueber das γ-Oxychinaldin und dessen Derivate. In: Berichte der deutschen chemischen Gesellschaft. Band 20, Nr. 1, 1887, S. 948–959, doi:10.1002/cber.188702001216.
- Externe Identifikatoren von bzw. Datenbank-Links zu 4-Hydroxychinolin: CAS-Nummer: 611-36-9, EG-Nummer: 210-268-2, ECHA-InfoCard: 100.009.336, PubChem: 69141, ChemSpider: 62357, Wikidata: Q27098240.
- Bradford P. Mundy, Michael G. Ellerd, Frank G. Favaloro Jr.: Name Reactions and Reagents in Organic Synthesis. 2. Auflage. John Wiley & Sons, Hoboken 2005, ISBN 0-471-22854-0, S. 166 f. (eingeschränkte Vorschau in der Google-Buchsuche).