Blei(II)-chromat
Blei(II)-chromat, PbCrO4, (umgangssprachlich auch bekannt als Bleichromat, Chromgelb, Parisergelb oder Königsgelb) ist ein Bleisalz der Chromsäure. Blei(II)-chromat ist im Colour Index unter C.I. Pigment Yellow 34 gelistet.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
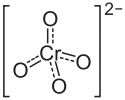 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Blei(II)-chromat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | PbCrO4 | |||||||||||||||
| Kurzbeschreibung |
gelber Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 323,18 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
6,3 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
fast unlöslich in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend, fortpflanzungsgefährdend (CMR)[4]; zulassungspflichtig[5] | |||||||||||||||
| MAK |
Schweiz: 5 μg·m−3 (berechnet als Chrom)[6] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Geschichte
Blei(II)-chromat wurde 1797 von Vauquelin in Paris entdeckt und heißt deswegen Pariser Gelb. Ab 1818 wird es als Pigment hergestellt und wird aufgrund seiner außerordentlich hohen Chrominanz bald zur Modefarbe (Neugelb), insbesondere als Postgelb.
Seit der Entwicklung der ersten gelben Azopigmente (C.I. Pigment Yellow 1 und 3) 1909 durch Hoechst kam das giftige Pigment im Künstlerfarbenbereich schnell außer Gebrauch.[7] Für die Anwendung im Lackbereich sind diese Ersatzpigmente jedoch ungeeignet, da sie ein geringes Deckvermögen und eine sehr niedrige Wetterechtheit besitzen.
In der industriellen Anwendung hielt sich Blei(II)-chromat in Europa bis in die 1980er Jahre, gemeinsam mit den heute ebenfalls geächteten Pigmenten Cadmiumsulfid (C.I. Pigment Yellow 35 und 37) und Molybdatrot (C.I. Pigment Red 104). Diese zählten zu den Standardpigmenten in diesem Farbtonbereich, wurden dann aber aufgrund der toxikologischen Eigenschaften von der europäischen Lackindustrie geächtet. Dies begründete unter anderem die starke Umsatzzunahme bei Bismutvanadatpigmenten (C.I. Pigment Yellow 184) und die Entwicklung von modifizierten organischen Pigmenten mit höherem Deckvermögen. Heute ist Blei(II)-chromat aus der industriellen Anwendung in Europa nahezu verschwunden, wird aber in den anderen Erdteilen weiter verwendet.[8][9][10]
Häufig verwendete es zum Beispiel Vincent van Gogh, der sich die teuren Cadmiumgelbe nicht leisten konnte.[7]
Vorkommen
In der Natur kommt Bleichromat als Mineral Krokoit, mit massiver monokliner Kristallstruktur, vor. Dieses Erz diente lange Zeit zur Chrom- und Bleigewinnung.
Gewinnung und Eigenschaften
Blei(II)-chromat ist ein orangegelbes, in Wasser unlösliches Pulver, das sich aus einer Lösung einer wasserlöslichen Bleiverbindung (z. B. Bleiacetat oder Bleinitrat), die mit Kaliumchromat oder Ammoniumchromat versetzt wurde, abscheidet.
Industriell wird die Darstellung aus Bleiacetat auf Natriumdichromat verwendet. Verwendet man zur Fällung der Bleisalzlösung nicht saure, sondern neutrale oder schwach alkalische Chromatlösungen, so entsteht basisches Bleichromat, Chromrot, als Mineral Phönikochroit.
In der Anwendung als Pigment für Lacke und Dispersionsfarben zeigt Blei(II)-chromat ein gutes Deckvermögen, Ergiebigkeit, Brillanz und hohe Chrominanz (Buntheit, auch Chroma).[8] Blei(II)-chromat wandelt sich aber dennoch langsam zu anderen Verbindungen um, wobei dreiwertiges Chrom entsteht. Dadurch ändert sich das Aussehen von Gelb zu mattem Braun. Dies führt dazu, dass alte Gemälde (zum Beispiel von Vincent van Gogh) im Laufe der Zeit immer dunkler werden.[11] Diese Reaktion wird vor allem durch ultraviolettes Licht und damit durch Sonnenstrahlung in Gang gesetzt. Selbst bei dem diffusen Licht in Museen lässt sich dieser Vorgang nicht völlig stoppen. Eine wichtige Rolle spielt dabei auch die verwendete Firnis, da dort Verbindungen enthalten sind, die die Elemente Barium und Schwefel enthalten und diese den Farbzerfall unterstützen.[12]
Chromgelb neigt zu Farbabweichungen und -verschiebungen und kann im Außenbereich auf Dauer empfindlich gegenüber dem Sonnenlicht und schwefeliger Säure als Luftschadstoff sein. Auch reagiert es mit Schwefelwasserstoff. In relativ dichten Bindemitteln wie Öl und Kunstharzen ist es lichtechter als bei der Verwendung als Aquarellfarbe.[13]

Bleichromat kristallisiert in der Monazit-Struktur, also im monoklinen Kristallsystem in der Raumgruppe P21/n (Raumgruppen-Nr. 14, Stellung 2) mit den Gitterparametern a = 712,7 pm, b = 743,8 pm, c = 679,9 pm und β = 102,43°. In der Elementarzelle befinden sich 4 Formeleinheiten.[14] Auch eine orthorhombische Modifikation (Raumgruppe Pnma (Nr. 62), a = 867 pm, b = 559 pm, c = 713 pm) wurde beschrieben.[15][16]
Verwendung
Blei(II)-chromat wurde im Künstlerfarbenbereich lange Zeit als Pigment verwendet, da es gleichermaßen günstig wie brillant und hochecht war. Auf Grund seiner Giftigkeit wurde es aber durch andere Substanzen wie Bismutvanadat ersetzt. In Europa besitzt die Verbindung in diesem Bereich nur noch Bedeutung als Pigment zur Restaurierung historischer Kunst- oder Bauwerke.
Im Gegensatz zu den meisten Chromorangetönen ist Chromgelb jedoch in der Regel nicht kalkecht.[17][18]
In der industriellen Anwendung als Pigment in Lacken und Dispersionsfarben wird Blei(II)-chromat nach wie vor in großen Mengen verwendet, allerdings nicht mehr in Europa. Es wird dabei auch als Mischkristall in Kombination mit Bleisulfat und/oder Bleimolybdat (z. B. von C.I. Pigment Red 104) eingesetzt.[19] Die außergewöhnliche Kombination von niedrigem Preis, hoher Buntheit, gutem Deckvermögen und hoher Wetterechtheit (sie wurde deshalb häufig auch als Rostschutzfarbe verwendet) bedeutet, dass Blei(II)-chromat in Regionen mit weniger hohem Sicherheitsbewusstsein als in Europa weiterhin eingesetzt wird. In Europa ist der Ersatz von Blei(II)-chromat zwar weitgehend abgeschlossen, dies aber zu Lasten des Preises und/oder der koloristischen Eigenschaften.[8][9]

Andere anorganische Pigmente wie Eisenoxidgelb (C.I. Pigment Yellow 42) sind zwar preisgünstig, aber deutlich trüber im Farbton. Hochwertige anorganische Pigmente wie Bismutvanadat zeigen einen reinen Farbton und gute Wetterechtheit, sind aber deutlich teurer als Blei(II)-chromat. Organische Pigmente wie Brillantgelb (z. B. C.I. Pigment Yellow 74, 151) zeigen sehr reine Farbtöne, sind aber ebenfalls teurer und besitzen selbst in optimierten Varianten ein wesentlich schlechteres Deckvermögen. Bezüglich der Wetterechtheit gibt es abhängig von der chemischen Struktur Typen mit höherem und niedrigerem Niveau. Alle weisen jedoch ein schlechteres Niveau als das anorganische Blei(II)-chromat auf.[8][9]
Sicherheitshinweise und gesetzliche Regelungen
Blei(II)-chromat wurde im Januar 2010 aufgrund seiner Einstufung als Krebserzeugend (Kategorie 1B) und Fortpflanzungsgefährdend (Kategorie 1A) in die Kandidatenliste der besonders besorgniserregenden Stoffe (Substance of very high concern, SVHC) aufgenommen.[4] Im Februar 2012 wurde Blei(II)-chromat zudem in das Verzeichnis der zulassungspflichtigen Stoffe mit dem Ablauftermin für die Verwendung in der EU zum 21. Mai 2015 aufgenommen.[5] Als Bleiverbindung unterliegt Blei(II)-chromat außerdem den Beschränkungen im Anhang XVII, Nummer 47, 63 und 72 der REACH-Verordnung.[20]
Trivia
- Die Farbbezeichnung Chromgelb ist die frühere Bezeichnung des heute als Narzissengelb bezeichneten Farbtons RAL 1007 im RAL-Farbsystem.
- Die oben beschriebene Reaktion mit Kaliumchromat dient unter anderem als Nachweis für Blei.
Literatur
- H. Kühn, M. Curran: Chrome yellow and Other Chromate Pigments. In: L. Feller (Hrsg.): Artists’ Pigments. A Handbook of Their History and Characteristics. Cambridge University Press, London 1986, S. 187–204 (Digitalisat).
Weblinks
- Chrome yellow, ColourLex
Einzelnachweise
- Datenblatt Blei(II)-chromat (PDF) bei Merck, abgerufen am 15. Dezember 2010.
- Eintrag zu Lead chromate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Blei(II)-chromat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 16. Juli 2014.
- Eintrag im Verzeichnis der zulassungspflichtigen Stoffe der Europäischen Chemikalienagentur, abgerufen am 16. Juli 2014.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach Chrom(VI)-Verbindungen), abgerufen am 27. Oktober 2015.
- Kurt Wehlte: Werkstoffe und Techniken der Malerei. Otto Maier, Ravensburg 1967. ISBN 3-473-48359-1 (früher: ISBN 3-473-61157-3), S. 102–103.
- G. Buxbaum, G. Pfaff; Industrial inorganic pigments; Wiley-VCH; 2006.
- W. Herbst, K.Hunger; Industrielle organische Pigmente; 3. Auflage; Wiley-VCH; 2004.
- Pigments for industrial paint mixing systems; Clariant; 2004.
- H. Tan, H. Tian, J. Verbeeck, L. Monico, K. Janssens, G. van Tendeloo: Nanoscale Investigation of the Degradation Mechanism of a Historical Chrome Yellow Paint by Quantitative Electron Energy Loss spectroscopy Mapping of Chromium Species. In: Angewandte Chemie. Band 125, Nr. 43, 2013, S. 11570–11573, doi:10.1002/ange.201305753.
- Wissenschaft aktuell: Vom Gelb zum Braun – Warum van Goghs Gemälde immer dunkler werden, abgerufen am 15. Februar 2011.
- Dr. A. Eibner: Malmaterialienkunde als Grundlage der Maltechnik. Für Kunststudierende, Künstler, Maler, Lackierer, Fabrikanten und Händler, 1909, Verlag Julius Springer, Berlin
- H. Effenberger, F. Pertlik: "Four monazite type structures: comparison of SrCrO4, SrSeO4, PbCrO4 (crocoite), and PbSeO4" in Zeitschrift für Kristallographie 1986, 176, S. 75–83. Volltext (PDF-Datei; 718 kB)
- G. Collotti, L. Conti, M. Zocchi: "The structure of the orthorhombic modification of lead chromate PbCrO4" in Acta Cryst 1959, 12, S. 416. doi:10.1107/S0365110X59001220
- F. Quittner, J. Sapgir, N. Rassudowa: "Die rhombische Modifikation des Bleichromates" in Zeitschrift für anorganische und allgemeine Chemie 1932, 204(3), S. 315–317. doi:10.1002/zaac.19322040309
- Beschreibung von Chromgelb (Memento vom 8. März 2017 im Internet Archive) bei Kremer Pigmente
- Michael Stahr, Joachim du Puits, Karl-Heinz Pfestorf: Praxiswissen Bausanierung: Erkennen und Beheben von Bauschäden, S. 481, Auflage von 2013 bzw. S. 808 in der 6. Auflage von 2015, Springer Verlag
- Leitfaden zur Anwendung umweltverträglicher Stoffe (PDF; 959 kB)
- ECHA: Liste der beschränkten Stoffe – Anhang XVII der REACH-Verordnung, abgerufen am 12. August 2020.

