2-Chlorpropan
2-Chlorpropan ist eine organisch-chemische Verbindung aus der Gruppe der Chlorkohlenwasserstoffe (CKW).
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
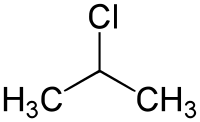 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2-Chlorpropan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C3H7Cl | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit chloroformartigem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 78,54 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
0,86 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
35 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
schwer in Wasser (3,1 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,378[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−172,3 kJ/mol[4] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
2-Chlorpropan kann durch Chlorierung von Propan erhalten werden, wobei abhängig von der Temperatur zu großen Teilen auch 1-Chlorpropan entsteht (siehe auch Markownikow-Regel).[5][6]
Eigenschaften
2-Chlorpropan ist eine sehr leicht flüchtige, farblose Flüssigkeit mit chloroformartigem Geruch. Im Gegensatz zu vielen Halogenalkanen besitzt es eine geringere Dichte als Wasser.
Thermodynamische Eigenschaften
Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 3,81944, B = 1022,222 und C = −41,619 im Temperaturbereich von 194,3 bis 309,7 K.[7]
| Eigenschaft | Typ | Wert [Einheit] | Bemerkungen |
|---|---|---|---|
| Verbrennungsenthalpie | ΔfH0liquid ΔfH0gas |
−2028,4 kJ·mol−1[8] −2059,6 kJ·mol−1[9] |
|
| Standardbildungsenthalpie | ΔcH0liquid | −145,0 kJ·mol−1[9] | |
| Kritische Temperatur | Tc | 489 K[10] | |
| Kritischer Druck | pc | 45,4 bar[10] | |
| Kritisches Volumen | Vc | 0,247 l·mol−1[10] | |
| Kritische Dichte | ρc | 0,318 g·ml−1[10] | |
| Azentrischer Faktor | ωc | 0,199[10] | |
| Schmelzenthalpie | ΔfusH | 7,39 J·mol−1·[11] | am Schmelzpunkt |
| Verdampfungsenthalpie | ΔVH | 27,2 kJ·mol−1[12][13] | beim Normaldrucksiedepunkt |
Die Temperaturabhängigkeit der Verdampfungsenthalpie lässt sich entsprechend der vereinfachten Watsongleichung ΔVH=A·(1−Tr)n (ΔVH in kJ/mol, Tr =(T/Tc) reduzierte Temperatur) mit A = 40,56 kJ/mol, n = 0,419 und Tc = 489,0 K im Temperaturbereich zwischen 156 K und 489 K beschreiben.[14]
Sicherheitstechnische Kenngrößen
2-Chlorpropan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt unterhalb von −36 °C.[1] Der Explosionsbereich liegt zwischen 2,8 Vol.‑% (90 g/m3) als untere Explosionsgrenze (UEG) und 10,7 Vol.‑% (350 g/m3) als obere Explosionsgrenze (OEG).[1][15] Die Grenzspaltweite wurde mit 1,32 mm (50 °C) bestimmt.[15] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA.[15] Die Zündtemperatur beträgt 590 °C.[1][15] Der Stoff fällt somit in die Temperaturklasse T1.
Einzelnachweise
- Eintrag zu 2-Chlorpropan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Datenblatt 2-Chlorpropan bei Sigma-Aldrich, abgerufen am 2. April 2010 (PDF).
- Eintrag zu 2-chloropropane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-24.
- J. Clayden, N. Greeves, S. Warren, P. Wothers: Organic Chemistry. 1. Auflage. Oxford University Press, 2000, ISBN 0-19-850346-6, S. 1036.
- Chemgapedia: Chlorierung höherer Alkane
- D. R. Stull: Vapor Pressure of Pure Substances Organic Compounds. In: Ind. Eng. Chem. 39, 1947, S. 517–540, doi:10.1021/ie50448a022.
- L. Smith, L. Bjellerup, S. Krook, H. Westermark: Heats of combustion of organic chloro compounds determined by the "quartz wool" method. In: Acta Chem. Scand. 7, 1953, S. 65–86, doi:10.3891/acta.chem.scand.07-0065, (PDF)
- R. A. Fletcher, G. Pilcher: Measurements of heats of combustion by flame calorimetry. Part 7.-Chloromethane, chloroethane, 1-chloropropane, 2-chloropropane. In: Trans. Faraday Soc. 67, 1971, S. 3191–3201, doi:10.1039/TF9716703191.
- Carl L. Yaws, Prasad K. Narasimhan: Thermophysical Properties of Chemicals and Hydrocarbons - Chapter 1: Critical Properties and Acentric Factor, Organic Compounds. 1. Auflage. Elsevier 2008, ISBN 978-0-8155-1596-8, S. 8, doi:10.1016/B978-081551596-8.50006-7.
- W. E. Acree: Thermodynamic properties of organic compounds: enthalpy of fusion and melting point temperature compilation. In: Thermochim. Acta. 189, 1991, S. 37–56, doi:10.1016/0040-6031(91)87098-H.
- J. H. Mathews, P. R. Fehlandt: The heats of vaporization of some organic compounds. In: J. Am. Chem. Soc. 53, 1931, S. 3212–3217, doi:10.1021/ja01360a002.
- J. B. Pedley, R. D. Naylor, S. P. Kirby: Thermochemical Data of Organic Compounds. Chapman and Hall, New York 1986.
- Carl L. Yaws, Marco A. Satyro: Thermophysical Properties of Chemicals and Hydrocarbons - Chapter 7: Enthalpy of Vaporation, Organic Compounds. 1. Auflage. Elsevier 2008, ISBN 978-0-8155-1596-8, S. 315, doi:10.1016/B978-081551596-8.50012-2.
- E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.

