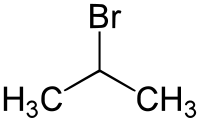
2-Brompropan
2-Brompropan ist eine organisch-chemische Verbindung aus der Gruppe der Bromkohlenwasserstoffe.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2-Brompropan | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C3H7Br | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit chloroformartigem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 122,99 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,31 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
59 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
3,18 g·l−1 (20 °C)[1] | |||||||||||||||
| Brechungsindex |
1,425[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−130,5 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Darstellung
2-Brompropan erhält man aus 2-Propanol durch Umsetzung mit Bromwasserstoffsäure (HBr).[5][6]
Auch die elektrophile Addition von Bromwasserstoff an Propen ergibt nach Markownikow 2-Brompropan.
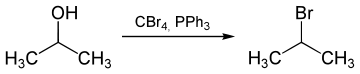
Ebenso kann 2-Brompropan durch eine Appel-Reaktion aus 2-Propanol, Tetrabromkohlenstoff (CBr4) und Triphenylphosphin (PPh3) erhalten werden.
Eigenschaften
2-Brompropan ist eine leicht flüchtige, farblose Flüssigkeit mit chloroformartigem Geruch, welche schwer löslich in Wasser ist.[6] Die Verbindung schmilzt bei −89 °C mit einer Schmelzenthalpie von 6,53 kJ·mol−1.[7] Sie bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei −20 °C. Die untere Explosionsgrenze (UEG) liegt bei 3,3 Vol.‑% (165 g/m3).[1]
Verwendung
In der organischen Synthese wird 2-Brompropan als Alkylierungsmittel für Amine, Phosphine, Alkohole und Thiole verwendet. Es ist ein Edukt bei Friedel-Crafts-Alkylierungen, Grignard-Reaktionen und anderen metallorganischen Reaktionen.[6]
Einzelnachweise
- Eintrag zu 2-Brompropan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 21. Oktober 2021. (JavaScript erforderlich)
- Datenblatt 2-Brompropan bei Sigma-Aldrich, abgerufen am 9. Oktober 2016 (PDF).
- Eintrag zu 2-bromopropane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-24.
- Autorengemeinschaft: Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, S. 200.
- Eintrag zu Brompropane. In: Römpp Online. Georg Thieme Verlag, abgerufen am 30. November 2020.
- Kushner, L.M.; Crowe, R.W.; Smyth, C.P.: The heat capacities and dielectric constants of some alkyl halides in the solid state in J. Am. Chem. Soc. 72 (1950) 1091–1098, doi:10.1021/ja01159a010.
- Ichihara, G.: Neuro-reproductive toxicities of 1-bromopropane and 2-bromopropane in Int. Arch. Occup. Environ. Health 78 (2005) 79–96, doi:10.1007/s00420-004-0547-9, pdf.