2,4′-Bipyridin
2,4′-Bipyridin ist eine heterocyclische chemische Verbindung mit der Summenformel C10H8N2. Sie besteht aus zwei Pyridinringen, bei der die 2-Position des einen Rings mit der 4-Position des zweiten Rings verknüpft ist und gehört zur Gruppe der Bipyridine.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
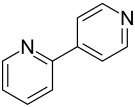 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2,4′-Bipyridin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C10H8N2 | |||||||||||||||
| Kurzbeschreibung |
hellgelbes bis hellbraunes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 156,19 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
280–282 °C[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Darstellung
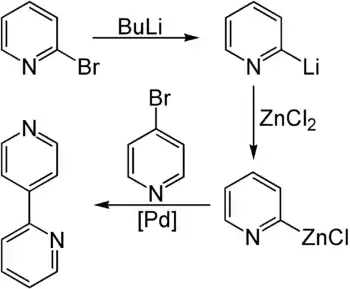
2,4′-Bipyridin kann durch eine Negishi-Kupplung aus 2-Brompyridin und 4-Brompyridin hergestellt werden. Hierzu wird 2-Brompyridin zunächst mit n-Butyllithium lithiiert und unter Zugabe von Zinkchlorid zum Zinkorganyl transmetalliert. Als Katalysator zur Kupplung dient ein Palladiumkomplex mit Triphenylphosphanliganden.[2]
Des Weiteren fällt es in geringen Mengen als Nebenprodukt bei der Synthese anderer Bipyridine an, beispielsweise bei der Herstellung von 4,4′-Bipyridin aus Pyridin mit Lithiumdiisopropylamid und HMPT.[3]
Eigenschaften
2,4′-Bipyridin ist bei Raumtemperatur ein gelblicher Feststoff, der bei 58–62 °C schmilzt und bei 280–282 °C siedet.
Verwendung
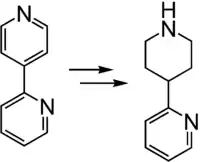
Durch Reduktion kann 2,4′-Bipyridin zur Herstellung von 4-(2-Pyridyl)piperidin genutzt werden, das als Ausgangsstoff für weitere Synthese eingesetzt kann.[4] Hierzu wird zunächst das N-Oxid gebildet und anschließend an Palladium mit molekularem Wasserstoff reduziert.
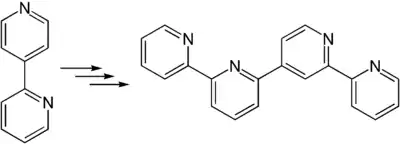
Auch zur Synthese von 2,2′:4′,2′′:6′′,2′′′-Quaterpyridin kann es verwendet werden.[5]
Einzelnachweise
- Datenblatt 2,4′-Bipyridin bei Acros, abgerufen am 21. Februar 2013.
- D. R. Sidler, N. Barta, W. Li, E. Hu, L. Matty, N. Ikemoto, J. S. Campbell, M. Chartrain, K. Gbewonyo, R. Boyd, E. G. Corley, R. G. Ball, R. D. Larsen, P. J. Reider, Paul J: Efficient synthesis of the optically active dihydropyrimidinone of a potent α1A-selective adrenoceptor antagonist. In: Canadian Journal of Chemistry. 80 (6), 2002, S. 646–652, doi:10.1139/v02-079.
- G. R. Newkome, D. C. Hager: Interconversion of cembranolide δ- and γ-lactones: synthesis of the C-1 epimer of isolobophytolide, in: J. Org. Chem., 1982, 47, S. 599–601 (doi:10.1021/jo00342a054).
- J.-C. Plaquevant, I. Chichaoui: Réduction régiospécifique des bipyridines, in: Tetrahedron Letters, 1993, 34, S. 5287–5288.
- J. A. Zoltewicz, M. P. Cruskie Jr., C. D. Dill: Use of pyridine N-oxide and pyridinium ion synthons in the preparation of oligopyridines. Two new unsymmetrical quaterpyridines with 2,2′-bipyridine units, in: Tetrahedron, 1996, 52, S. 4239–4244 (doi:10.1016/0040-4020(96)00100-7).