1,1,1-Trimethylolpropan
1,1,1-Trimethylolpropan ist eine organische Verbindung aus der Gruppe der Alkohole, die in Form eines weißen, brennbaren Pulvers vorliegt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
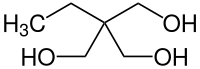 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1,1,1-Trimethylolpropan | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C6H14O3 | ||||||||||||||||||
| Kurzbeschreibung |
weißer, kristalliner Feststoff mit schwachem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 134,18 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,084 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
295 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
leicht löslich in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Die technische Herstellung von 1,1,1-Trimethylolpropan erfolgt durch eine doppelte Aldoladdition von n-Butyraldehyd (1) mit Formaldehyd (2), wobei zunächst 2,2-Bis-hydroxymethylbutanal (3) als Zwischenprodukt entsteht. Dieses reagiert anschließend mit überschüssigem Formaldehyd und Einsatz stöchiometrischer Mengen Base in einer gekreuzten Cannizzaro-Reaktion, wobei die Aldehydgruppe zum Alkohol reduziert wird und Trimethylolpropan (4) sowie das entsprechende Formiat (5) gebildet wird.[3]
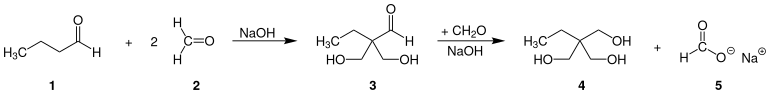
Als Base wird vorwiegend Natrium- oder Calciumhydroxid verwendet. Gelegentlich werden auch verschiedene Carbonate eingesetzt. Die Ausbeute beträgt in allen Fällen etwa 90 %. Um den großen Anfall an Formiat-Nebenprodukt zu vermeiden, wird die Reduktion der Carbonylgruppe in einigen Prozessen (z. B. BASF) mittels katalytischer Hydrierung realisiert. Als Basen werden tertiäre Amine und Cobalt-Hydrierkatalysatoren eingesetzt.[3]
Eigenschaften
1,1,1-Trimethylolpropan besitzt drei Hydroxygruppen und ermöglicht es dadurch, Polymere dreidimensional zu vernetzen. Der Flammpunkt liegt bei 179 °C, die Zündtemperatur bei 375 °C.[2]
Verwendung
1,1,1-Trimethylolpropan wird als Zwischenprodukt bei der Synthese anderer organischer Verbindungen eingesetzt (zum Beispiel Trimethylolpropan-trimethacrylat (TMPTMA), für Polyurethane, Polyesterpolyole und Polyetherpolyole, für Tenside, Bindemittel und Klebstoffe, synthetische Schmierstoffe, Polyester- und Alkydharzlacke). Diese werden in der Möbel-, Bau- und Automobilindustrie genutzt.[4]
Weblinks
- OECD: Screening Information Dataset (SIDS) Initial Assessment Report (SIAR) für 1,3-Propanediol, 2-ethyl-2-(hydroxymethyl)-
Einzelnachweise
- Eintrag zu TRIMETHYLOLPROPANE in der CosIng-Datenbank der EU-Kommission, abgerufen am 16. April 2020.
- Eintrag zu 1,1,1-Trimethylolpropan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 7. Oktober 2020. (JavaScript erforderlich)
- Peter Werle, Marcus Morawietz, Stefan Lundmark, Kent Sörensen, Esko Karvinen,Juha Lehtonen: Alcohols, Polyhydric. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley‐VCH Verlag GmbH & Co. KGaA., 15. Juli 2008, S. 14; doi:10.1002/14356007.a01_305.pub2.
- Nachrichten aus der Chemie, 03/2011, S. 219 doi:10.1002/nadc.201179640.
