Ytterbium(II)-chlorid
Ytterbium(II)-chlorid ist eine anorganische chemische Verbindung des Ytterbiums aus der Gruppe der Chloride.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
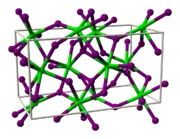 | ||||||||||||||||
| _ Yb2+ _ Cl− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Ytterbium(II)-chlorid | |||||||||||||||
| Andere Namen |
Ytterbiumdichlorid | |||||||||||||||
| Verhältnisformel | YbCl2 | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 243,95 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
5,27 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
1300 °C[1] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Ytterbium(II)-chlorid kann durch Reduktion von Ytterbium(III)-chlorid mit Wasserstoff bei 500 °C bis 600 °C oder mit Zink in Zinkchlorid bei 500 °C gewonnen werden,[1] wobei erstere Reaktion zuerst 1929 von Wilhelm Klemm und Wilhelm Schüth berichtet wurde.[5][6]
Die Verbindung lässt sich auch durch Reduktion mit Lithium-Naphthalin gewinnen.[7]
Eigenschaften
Ytterbium(II)-chlorid ist ein farbloser[1] oder grüner[2] Feststoff. Die Verbindung ist äußerst hygroskopisch und kann nur unter sorgfältig getrocknetem Schutzgas oder im Hochvakuum aufbewahrt und gehandhabt werden. An Luft oder bei Kontakt mit Wasser geht er unter Feuchtigkeitsaufnahme in Hydrate über, die aber instabil sind und sich mehr oder weniger rasch unter Wasserstoff-Entwicklung in Oxidchloride verwandeln. Die Verbindung besitzt eine Kristallstruktur vom Strontiumiodid-Typ[1][8] und kristallisiert rhombisch mit den Gitterkonstanten a = 13,18 Å, b = 6,96 Å, c = 6,70 Å mit der Raumgruppe Pbca (Raumgruppen-Nr. 61).[9] Klemm und Schüth beschrieben die Verbindung als nahezu farblosen, diamagnetischen Feststoff, der sich in Wasser mit gelber Farbe löst, wesentlich bestandiger ist als Samarium(II)-chlorid und Europium(II)-chlorid nahesteht. Die Verbindung reagiert mit flüssigem Ammoniak und färbt sich dabei rot. Durch Abbau wurden Ammoniakate mit acht (rotgelb), zwei und einem Mol (gelb) Ammoniak nachgewiesen. Nach Zahl und Beständigkeit der Ammoniakate steht die Verbindung zwischen Calciumchlorid und Strontiumchlorid. Beim isothermen Abbau der Ammoniakate tritt eine geringere Ammonolyse auf als bei Samarium(II)-chlorid.[10]
Verwendung
Ytterbium(II)-chlorid kann in der organischen Chemie zur reduktiven Dimerisierung von ungesättigten Ketonen verwendet werden.[3]
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1081.
- William M. Haynes: CRC Handbook of Chemistry and Physics, 93rd Edition. CRC Press, 2012, ISBN 1-4398-8049-2, S. 4–99 (eingeschränkte Vorschau in der Google-Buchsuche).
- David Crich: Handbook of Reagents for Organic Synthesis, Reagents for Radical and Radical ... John Wiley & Sons, 2013, ISBN 978-1-118-63487-5, S. 651 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- H.J. Emeléus, A.G. Sharpe: ADVANCES IN INORGANIC CHEMISTRY AND RADIOCHEMISTRY. Academic Press, 1977, ISBN 0-08-057869-1, S. 17 (eingeschränkte Vorschau in der Google-Buchsuche).
- Wilhelm Klemm, Wilhelm Schüth: Messungen an zwei- und vierwertigen Verbindungen der seltenen Erden. III. Ytterbiumdichlorid. In: Zeitschrift für anorganische und allgemeine Chemie. 184, 1929, S. 352–358, doi:10.1002/zaac.19291840128.
- Kurt Rossmanith: Herstellung der klassischen Seltenerd(II)-chloride in Lösung. In: Monatshefte für Chemie. 110, 1979, S. 109–114, doi:10.1007/BF00903752.
- H. Bärnighausen, H. Pätow, H. P. Beck: Kristallchemische Studien an Seltenerd-Dihalogeniden. Die Kristallstruktur von Ytterbium(II)-chlorid, YbCl2. In: Zeitschrift für anorganische und allgemeine Chemie. 403, 1974, S. 45–55, doi:10.1002/zaac.19744030106.
- Horst. P. Beck, H. Bärnighausen: Zur Kristallchemie der Ytterbium(II)-Halogenide YbCl2 und YbBr2. In: Zeitschrift für anorganische und allgemeine Chemie. 386, 1971, S. 221, doi:10.1002/zaac.19713860214.
- Wilhelm Klemm und Wilhelm Schüth, Messungen an zwei- und merwertigen Verbindungen der seltenen Erden: III. Ytterbiumdichlorid, aus Chemisches Zentralblatt. 30. April 1930 Band I. Nr. 18.