Silberiodid
Silberiodid (auch: Silberjodid) ist eine chemische Verbindung aus Silber und Iod. Es ist ein gelbliches, in Wasser unlösliches Salz.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
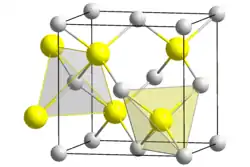 | ||||||||||||||||
| _ Ag+ _ I− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Silberiodid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | AgI | |||||||||||||||
| Kurzbeschreibung |
gelbliches, geruchloses Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 234,77 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
5,67 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (0,03 mg·l−1)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
0,01 mg·m−3 (bezogen auf die einatembare Fraktion)[1] | |||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−61,8 kJ/mol[2] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vorkommen
Natürlich kommt Silberiodid als Mineral Jodargyrit vor.
Gewinnung und Darstellung

ohne und mit Ammoniakwasser
Silberiodid wird durch Ausfällen aus einer Silbernitrat-Lösung mit Hilfe von Kaliumiodid gewonnen.
Diese Reaktion wird auch in der chemischen Analytik als Nachweis für Iodid-Ionen benutzt, weil das entstehende AgI einen schwerlöslichen gelblichen Niederschlag bildet. Im Gegensatz zum Silberiodid lassen sich das ebenfalls schwer lösliche Silberchlorid (AgCl) und Silberbromid (AgBr) in Ammoniak lösen (Komplexbildungsreaktion). Mit Natriumthiosulfat lässt sich auch Silberiodid komplexieren bzw. lösen. Chlorid-, Bromid- und Iodid-Ionen können so mit Hilfe von Natriumthiosulfat und Ammoniaklösung voneinander unterschieden werden.[3][4]
Eigenschaften
Physikalische Eigenschaften
Von Silberiodid sind mehrere Modifikationen bekannt.[5] Bei Raumtemperatur ist das β-AgI thermodynamisch stabil, das in der Wurtzit-Struktur kristallisiert. Daneben existiert eine metastabile Modifikation, das γ-AgI, das eine Zinkblende-Struktur hat.
Oberhalb von etwa 147 °C ist das α-AgI stabil, das aufgrund seiner hohen Silberionen-Leitfähigkeit zu den festen Ionenleitern gehört. Seine ionische Leitfähigkeit liegt in der Größenordnung von 1 bis 2 S/cm[6] und ist vergleichbar mit der von Flüssigelektrolyten. Das α-AgI hat ein kubisch-innenzentriertes Iodid-Untergitter und ein strukturell fehlgeordnetes Silberionen-Untergitter. Die Silberionen können sich also zwischen den größeren Iodidionen frei bewegen. Durch Einlagerung von Rubidium-Ionen zum Rubidiumsilberiodid (Ag4RbI5) kann die Temperatur des α/β-Phasenüberganges auf unter Raumtemperatur gesenkt werden. Dadurch wird auch der Bereich der Ionenleitung bis auf Raumtemperatur ausgedehnt.
Die elektronische Leitfähigkeit von α-AgI beruht auf Elektronen-Lochleitung und ist proportional zum I2-Partialdruck. Sie ist gegenüber der auf den Silberionen beruhenden Leitfähigkeit um ungefähr den Faktor 1010 kleiner.[7] Dies macht Silberiodid als festen Elektrolyten besonders gut geeignet.
Chemische Eigenschaften

Silberiodid ist lichtempfindlich und zerfällt dabei langsam in seine Elemente. An Sonnenlicht verfärbt es sich grün-grau. AgI löst sich in starken Komplexbildnern, wie Cyaniden oder Thiocyanaten.
Verwendung
Silberiodid wird mit Aceton gemischt aus Hagelfliegern versprüht, um in der Atmosphäre kleinste Kondensationskerne zur gezielten Regen- oder Hagelbildung zu erzeugen.
Einerseits dient es dazu, schädliche Unwetter zu verhindern oder abzuschwächen. Es kann damit die Bildung von zu großen Hagelkörnern verhindert werden. In den USA wurde in den 1940er und 1950er Jahren versucht, mit Silberiodid Hurrikane vorzeitig abzuschwächen; die Wirkung war allerdings begrenzt.[8] In Deutschland wurde 1958 im Landkreis Rosenheim eine organisierte Hagelabwehr eingerichtet, die das Silberiodid aus über 100 Abschussstellen durch Raketen in die Wolken schoss.[8] Seit 1975 wird diese Aufgabe von zwei Anti-Hagel-Flugzeugen erledigt.[8] In Süddeutschland, Österreich und der Schweiz gibt es noch weitere als Verein organisierte Hagelwehren.
Andererseits wird dadurch versucht, bestimmte Gebiete gezielt mit Niederschlag zu versorgen: Durch Impfen der Wolken mit Silberiodid-Feinstaub im Aufwindkanal einer Wolkenfront aus einem Flugzeug wird seit den 1980er Jahren (laut einer unbestätigten Behauptung des russischen Majors Alexei Gruschin auch 1986 bei Tschernobyl zur Verhinderung von radioaktiv belasteten Wolken über russischen Großstädten[9]) im mittleren Westen der USA und Russlands, aber auch testweise in Bayern[10] versucht, die Wolken gezielt an einem definierten Ort abregnen zu lassen.[11] Die Wirksamkeit dieser Methode ist statistisch zwar untersucht, aber der Erfolg ist gering (ca. 10 % mehr Niederschlag). Das Silberiodid ist im dadurch gefallenen Schnee in geringsten Mengen analytisch nachweisbar. Diese Mengen sind für den Menschen ungefährlich.
Mit dem konträren Ziel wird zu einzelnen Terminen ein bestimmtes Gebiet regenfrei gehalten, indem man die Schauer davor niedergehen lässt. So herrscht in Moskau am 9. Mai, dem Tag des Sieges, und am 12. Juni, dem Tag Russlands, Sonnenschein.[12] Bei den Olympischen Sommerspielen in Peking 2008 wurde Silberiodid mit Hilfe von Raketen in Regenwolken eingebracht, um einer Störung der Eröffnungsfeierlichkeiten vorzubeugen.[13]
In den Anfangszeiten der Fotografie im 19. Jahrhundert wurde Silberiodid wegen seiner Lichtempfindlichkeit für verschiedene Edeldruckverfahren wie Kalotypie oder Argyrotypie verwendet. Später wurde es durch besser geeignete Substanzen wie Silberbromid ersetzt.
Einzelnachweise
- Eintrag zu Silberiodid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 11. März 2020. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-4.
- James Huheey, Ellen Keiter, Richard Keiter: Anorganische Chemie: Prinzipien von Struktur und Reaktivität. Gruyter, Germany 2003, ISBN 978-3110179033, S. 150.
- Halogenidtrennung
- J. G. P. Binner, G. Dimitrakis, D. M. Price, M. Reading, B. Vaidhyanathan: "Hysteresis in the β–α Phase Transition in Silver Iodide", Journal of Thermal Analysis and Calorimetry, 2006, 84, S. 409–412 (PDF)
- W. Biermann, W. Jost: Z. Phys. Chem. N. F., 1960, 25, S. 139.
- B. Ilschner: J. Chem. Phys., 1958, 28, S. 1109.
- Mara Schneider: Das Wetter lässt sich nur bedingt kontrollieren. (Nachrichtenartikel) (Nicht mehr online verfügbar.) news.de, 19. Februar 2009, ehemals im Original; abgerufen am 21. Februar 2009 (deutsch). (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis.
- Telepolis: Warum es nach Tschernobyl über Weißrussland regnete | Telepolis, abgerufen am 18. August 2018
- BR.de: Wettermanipulation: Die Hagelflieger von Rosenheim | Wissen | Themen | BR.de, abgerufen am 18. August 2018
- WELT: Regen auf Knopfdruck - WELT, abgerufen am 18. August 2018
- Anne Gellinek, Janin Renner, Kay Siering: Die Wolkenschieber (Memento vom 5. März 2011 im Internet Archive).
- SPIEGEL ONLINE: Olympia-Wetter: China schießt auf Regenwolken
