Malonsäuredinitril
Malonsäuredinitril, auch Propandinitril, ist eine chemische Verbindung aus der Stoffklasse der Nitrile mit der Formel CH2(CN)2. Malonsäuredinitril ist relativ sauer mit einem pKs-Wert von 11 in Wasser.[7] Daher kann Malonsäuredinitril in einer Knoevenagel-Kondensation reagieren, zum Beispiel zur Herstellung von 2-Chlorbenzyliden-malonsäuredinitril.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
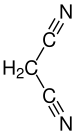 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Malonsäuredinitril | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C3H2N2 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 66,06 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,049 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
220 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Brechungsindex |
1,4146 (34 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
186,4 kJ/mol[6] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
Malonsäuredinitril kann aus Chlorcyanoacetylen und Ammoniak hergestellt werden.[8] Im großtechnischen Maßstab wird Malonsäuredinitril bei der Umsetzung von Acetonitril mit Chlorcyan bei über 700 °C hergestellt. Andere Möglichkeiten zur Herstellung gehen von (2-Cyano-N-alkoxy)-acetimidoylhalogeniden aus, wobei ebenfalls Temperaturen zwischen 500 und 1000 °C benötigt werden.[9]
Eigenschaften
Malonitril ist ein brennbarer farbloser Feststoff, der leicht löslich in Wasser ist. Er zersetzt sich ab einer Temperatur von 130 °C, wobei Cyanwasserstoff, Stickstoffoxide, Kohlenmonoxid und Kohlendioxid entstehen und eine Explosion möglich ist.[2] Die mittels DSC bestimmte Zersetzungswärme beträgt −108 kJ·mol−1 bzw. −1650 kJ·kg−1.[10] Bei niedrigeren Temperaturen kann es bei Kontakt mit starken Basen zu einer heftigen Polymerisation kommen, die ebenfalls explosionsartig verlaufen kann.[11]
Verwendung
In der Chemie ist Malonsäuredinitril ein Ausgangsmaterial für die Gewald-Reaktion, in welcher das Nitril mit einem Keton oder Aldehyd in Gegenwart von elementarem Schwefel und einer Base zu 2-Aminothiophenen kondensiert. Weiterhin spielt Malonsäuredinitril eine wichtige Rolle bei der Synthese einer Vielfalt von pharmazeutischen und agrochemischen Wirkstoffen.[12] Malonsäuredinitril ist ein Edukt für die Gewinnung von CS-Gas.
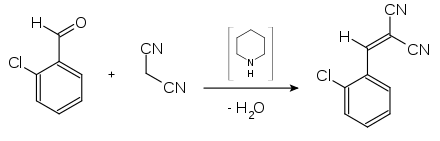
- Synthese von 2-Chlorbenzyliden-malonsäuredinitril (CS-Gas)
Einzelnachweise
- Eintrag zu Malononitril. In: Römpp Online. Georg Thieme Verlag, abgerufen am 5. Juli 2016.
- Eintrag zu Malonitril in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-322.
- Eintrag zu Malononitrile im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Datenblatt Malonsäuredinitril (PDF) bei Merck, abgerufen am 19. Januar 2011.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-23.
- Evans pKa table (PDF; 245 kB)
- Peter B. Sargeant: Fluorocyclopropanes. I. Preparation and nuclear magnetic resonance spectra. In: Journal of Organic Chemistry. 35(3), 1970, S. 678–682.
- Process for the preparation of malononitrile
- T. Grewer, O. Klais: Exotherme Zersetzung - Untersuchungen der charakteristischen Stoffeigenschaften. (= Humanisierung des Arbeitslebens. Band 84). VDI-Verlag, Düsseldorf 1988, ISBN 3-18-400855-X, S. 8.
- Bretherick's Handbook of Reactive Chemical Hazards. 6. Auflage. Vol. 1, Butherworth-Heinemann, 1999, ISBN 0-7506-3605-X, S. 386.
- Ullmanns Encyklopädie der technischen Chemie. 4., neubearbeitete und erweiterte Auflage. Band 16, Verlag Chemie, Weinheim 1978, ISBN 3-527-20016-9, S. 419–423.

