Gewald-Reaktion
Bei der Gewald-Reaktion handelt es sich um eine Namensreaktion in der Organischen Chemie, die nach ihrem Entdecker Karl Gewald (1930–2017) benannt wurde.[1][2][3] Dabei wird ein Keton (oder ein Aldehyd, falls R2 = H) mit einem α-Cyanoester in Gegenwart von elementarem Schwefel und einer Base zu einem substituierten 2-Amino-thiophen umgesetzt.[4][5]
Übersichtsreaktion
Ein Keton und ein α-Cyanoester reagieren mit der Base Morpholin in einer Knoevenagel-Kondensation zu einem α-Alkyliden-nitril, das mit elementarem Schwefel zu einem 2-Amino-thiophen reagiert.
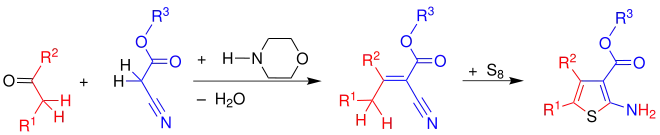
Mechanismus
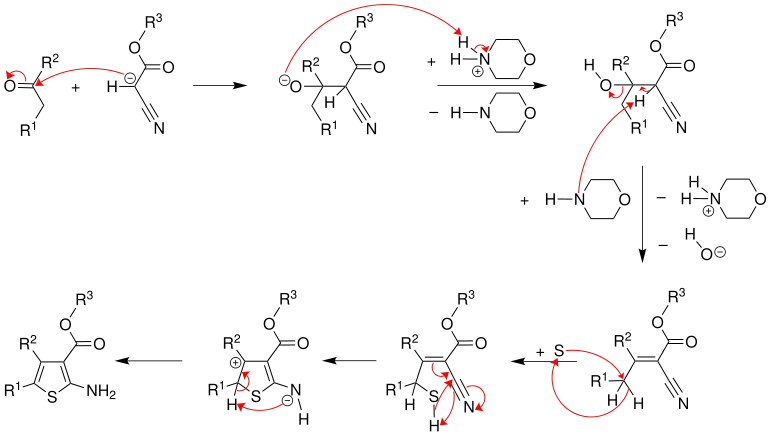
Der Reaktionsmechanismus konnte erst mehrere Jahre nach der Entdeckung der Reaktion teilweise aufgeklärt werden.[6] Im ersten Reaktionsschritt wird der α-Cyanoester durch die Base Morpholin deprotoniert.[7]

Das entstandene Anion und das Keton addieren sich zu einem Alkoholat, das im weiteren Schritt durch die protonierte Base zu einem Alkohol protoniert wird. Dieser wird zu dem stabilen Zwischenprodukt α-Alkylidennitril deprotoniert.
Der Mechanismus der Addition von elementarem Schwefel ist unbekannt. Es wird angenommen, dass dabei das zu addierende Intermediat eine Rolle spielt. Cyclisierung und Tautomerisierung liefern dann das 2-Aminothiophen.
Energiezufuhr mit Mikrowellen verkürzt bisweilen die Reaktionszeiten bei zugleich erhöhter Ausbeute.[8]
Varianten
In einer Abwandlung der Gewald-Reaktion wird 3-Acetyl-2-aminothiophen erhalten, wenn man Dithian [ein Addukt aus Schwefel und Aceton (R = CH3)] mit frisch hergestelltem Cyanoaceton umsetzt:[9]
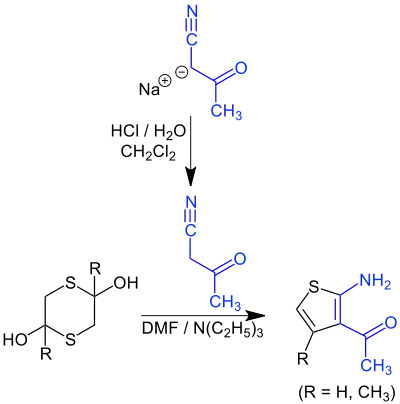
Einzelnachweise
- John A. Joule, Keith Mills: Heterocyclic Chemistry, John Wiley & Sons, 5. Auflage (2010), S. 340, ISBN 978-1-4051-3300-5.
- Bradford P. Mundy, Michael G. Ellerd, Frank G. Favaloro, Jr.: Name Reactions and Reagents in Organic Synthesis, John Wiley & Sons, 2. Auflage (2005) S. 306, ISBN 0-471-22854-0.
- Christopher Hume: Applications of Multicomponent Reactions in Drug Discovery – Lead Generation to Process Development, S. 311–341, dort S. 332–334, In Jieping Zhu, Huges Bienaymé: Multicomponent Reactions, Wiles-VCH Verlag, 2005, ISBN 978-3-527-30806-4.
- Gewald, K.; Schinke, E.; Böttcher, H. Chemische Berichte 1966, 99, 94–100.
- Sabnis, R. W. Sulfur Reports 1994, 16, 1–17.
- Sabnis, R. W.; Rangnekar, D. W.; Sonawane, N. D. J. Heterocyclic Chem. 1999, 36, 333.
- K. Schwetlick: Organikum. 23. Auflage. Wiley-VCH Verlag, Weinheim 2009, ISBN 978-3-527-32292-3, S. 434.
- Sridhar, M.; Raoa, R. M.; Babaa, N. H. K.; Kumbhare, R. M. Tetrahedron Lett. 2007, 48, 3171–3172, (doi:10.1016/j.tetlet.2007.03.052).
- Gernot A. Eller, Wolfgang Holzer Molecules 2006, 11, 371–376 Online-Artikel (PDF; 59 kB).