Liquid Biopsy
Unter einer Liquid Biopsy (LB, deutsch Flüssigbiopsie) versteht man die Probeentnahme und Analyse von nicht festem, biologischen Gewebe, hauptsächlich Blut. Ein Vorteil besteht darin, dass sie weitgehend nichtinvasiv erfolgt. Wie die herkömmliche Biopsie, wird diese Untersuchungsart hauptsächlich zur Diagnose und Überwachung von Krankheiten wie Krebs eingesetzt. Das Verfahren wurde durch Fortschritte bei der DNA-Sequenzierung des menschlichen Genoms ermöglicht, wodurch genetische Mutationen von Krebszellen erkannt werden können.[1]
Tumordiagnostik
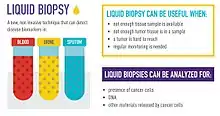
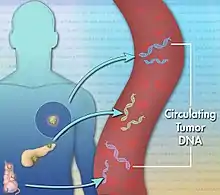
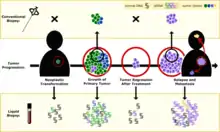
Nach einer Blutentnahme werden zirkulierende Tumorzellen oder Tumor-Erbgut im Blut nachgewiesen.
Zirkulierende Tumorzellen (englisch Circulating tumor cells, CTCs) sind einzelne Krebszellen, die vom Tumor in die Blutbahn gelangen. Sie können durch bestimmte Eigenschaften von normalen Blutzellen unterschieden werden. Inzwischen gibt es mehrere Verfahren, mit denen CTCs gezählt und zum Teil auch angereichert werden können. Hat man die Zellen isoliert, kann man ihr Erbgut oder ihre Eiweiß-Zusammensetzung untersuchen.
Bei zirkulierender Tumor-DNA (englisch Circulating free DNA, cfDNA) handelt es sich um kurze Erbgut-Abschnitte, die als Abbaureste von Tumorzellen im Blut freigesetzt wurden. Im Blut treibt allerdings auch DNA, die von gesunden Zellen stammt. Die Tumor-DNA weist man nach, indem man die DNA aus gesunden Zellen vollständig aus der Blutprobe entfernt.
Der Tumormarker cell free microRNA-375 (cf miR-375) wird u. a. von Merkelzell-Tumorzellen übermäßig ins Blut freigesetzt. Mit einer Blutuntersuchung kann das Ansprechen auf eine Therapie überprüft und ein eventueller Krankheitsrückfall frühzeitig erkannt werden.[2][3]
Mit der Liquid Biopsy des Urins konnte aufgezeigt werden, dass Immunzellen, die im Urin gefunden wurden, repräsentativer für die Diagnostik eines Blasenkarzinoms waren, als Immunzellen aus dem Blut, was darauf schließen lässt, dass das Verfahren mittels Urin anstelle des Blutes dazu beitragen kann, die Reaktion auf eine Immuntherapie genauer zu überprüfen. T-Lymphozyten kommen im Urin normalerweise bei gesunden Personen nicht vor. Entscheidend ist, dass die T-Zellen mit denen in der Tumorumgebung des Blasenkarzinoms übereinstimmen, unabhängig vom Krebsstadium und dem Behandlungsverlauf. Die Immuntherapie ist für Krebsarten, die schwer zu behandeln sind, vielversprechend, jedoch sprechen nur 30–40 Prozent der Patienten auf eine Immuntherapie an. Diese können damit identifiziert werden.[4][5]
Beim malignen Melanom kann eine Immuntherapie mit Anti‐CTLA-4‐ und Anti‐PD-1‐Antikörpern sowie Therapien, die gegen bestimmte Mutationen gerichtet sind, wie BRAF, NRAS und c‐KIT durchgeführt werden. Im Fall von Melanompatienten können die Ergebnisse der Liquid Biopsy als neuartige prädiktive Biomarker bei therapeutischen Entscheidungen hilfreich sein, insbesondere im Zusammenhang mit mutationsbasierten, zielgerichteten Therapien.[6]
Beim Adenokarzinom der Bauchspeicheldrüse (englisch Pancreatic ductal adenocarcinoma, PDAC) kann durch die Untersuchung von DNA-basierten Biomarkern in exosomaler Speichel-DNA (exoDNA) mittels Liquid Biopsy die Früherkennung, Tumorstratifizierung, Therapiestratifizierung und das Monitoring bei Patienten mit PDAC durchgeführt werden.[7][8]
Anfang 2019 gaben Forscher des Universitätsklinikums Heidelberg bekannt, dass die ersten marktfähigen Bluttests für Brustkrebs entwickelt worden seien. Das neue Verfahren mittels Liquid Biopsy erkenne eine Krebserkrankung anhand von Biomarkern und könne somit das Diagnosespektrum bildgebender Diagnoseverfahren wie Mammographie, Ultraschall oder Magnetresonanztomographie (MRT) erweitern. Im Blut von an Brustkrebs erkrankten Frauen konnten bis zu 15 verschiedene Biomarker (microRNA und Methylierungsmarker) identifiziert werden, mit deren Hilfe auch kleine Tumore (< 5 mm) nachweisbar seien. Die Biomarker könnten ebenso Auskunft darüber geben, ob eine Behandlung anspricht oder eine Therapieresistenz eintritt.[9][10] In einer gemeinsamen Stellungnahme der Deutschen Krebsgesellschaft (DKG), Deutschen Gesellschaft für Gynäkologie und Geburtshilfe (DGGG), DGS, AGO, AGO Mamma, AGO TraFo, Deutschen Gesellschaft für Hämatologie und Medizinische Onkologie (DGHO) wird ausdrücklich die Forschung zur Liquid-Biopsy-Technologie begrüßt, aber gleichzeitig vor einer verfrühten Anwendung des Tests gewarnt. Eine wissenschaftliche Publikation liege noch nicht vor. Die klinischen Konsequenzen des Testes im Zusammenhang mit den Ergebnissen andere diagnostischer Verfahren, beispielsweise Mammographie und Sonografie, müssten zunächst in Studien überprüft werden.[11] Dies bestätigte nunmehr die Uni Heidelberg, Das Diagnoseverfahren könne zwar Ende des Jahres zu Testzwecken im Labor eingesetzt werden, damit sei der Test, der in Blutproben Botenstoffe von Tumorzellen detektieren kann, aber noch nicht auf dem Markt. Gerade bei Frauen über 50 läge die Trefferquote der Tests gerade einmal bei 60 Prozent. Bei jüngeren Patientinnengruppen waren die Ergebnisse zwar besser, aber gerade Frauen über 50 haben eben das größte Brustkrebsrisiko.[12]
Inzwischen hat die Staatsanwaltschaft Heidelberg hierzu Vorermittlungen aufgenommen. Uniklinikum und Spin-Off Heiscreen hatten den Test trotz fehlender Daten als „Meilenstein“ in der Brustkrebs-Frühdiagnostik bezeichnet. Finanzielle Verstrickungen von Ärzten, aber auch von Prominenten sollen die PR-Kampagne begünstigt haben.[13]
Weitere Diagnostikmöglichkeiten
Bei der Herzinfarktdiagnose wird nach im Blut zirkulierenden Endothelzellen (englisch Circulating endothel cells, CECs) gesucht.[14]
In der Pränataldiagnostik wird aus dem mütterlichen Blut oder Fruchtwasser zellfreie fetale DNA (englisch Cell-free fetal DNA, cffDNA) extrahiert. Pränatale Abstammungsgutachten (Vaterschaftstests) basieren auf dieser Methode, bei der die genetischen Marker Einzelnukleotid-Polymorphismus (englisch Single Nucleotide Polymorphism, SNP) des angenommenen Vaters und des Embryos verglichen werden.[15] Gemäß Gendiagnostikgesetz dürfen diese in Deutschland nur vorgenommen werden, wenn eine Straftat nach § 176 bis § 178 StGB (Sexueller Missbrauch von Kindern) vorliegt.
Es kann die Isolierung von Protoporphyrin IX aus Blutproben als Diagnosewerkzeug für Atherosklerose verwendet werden.[16]
Bei der Untersuchung des Zentralnervensystems kann anstelle von Blut Zerebrospinalflüssigkeit entnommen werden.[17]
Blutentnahme
Für die Blutentnahme (etwa 10 ml) müssen spezielle Röhrchen eingesetzt werden. Die meisten Standardröhrchen für die Blutentnahme bestehen aus positiv geladenen Kunststoffen, so dass die negativ geladene cfDNA adsorbiert wird und bei der Analyse nicht mehr nachgewiesen werden kann. Zudem beginnt der Zerfall der Blutzellen nach der Entnahme, wodurch genomische DNA freigesetzt und jede Analyse der tatsächlichen cfDNA verzerrt wird. Beide Prozesse beeinflussen die Sensitivität und das Ergebnis der Analyse der Liquid Biopsy. Daher sollen bewährte Blutentnahmeröhrchen aus der Pränataldiagnostik oder solche, die speziell für tumorgenetische Untersuchungen entwickelt wurden, eingesetzt werden. Sie bestehen aus negativ geladenen Werkstoffen und enthalten Stabilisatoren, die den Blutzellenzerfall etwa fünf Tage lang verhindern.[18][19] Ferner sollten für die Blutentnahme Kanülen in ausreichender Größe (≥ 21 Gauge) eingesetzt werden, damit kernhaltige Blutzellen intakt bleiben, beispielsweise Entnahmesysteme, die für Blutkulturen eingesetzt werden und darauf ausgerichtet sind, Blutzellen intakt und vital zu erhalten.[20] Aufgrund der geringen Konzentration von < 0,001 % im Plasma muss die cfDNA mithilfe spezieller Amplifikationsmethoden angereichert werden, damit anschließend nach bestimmten Mutationen gesucht werden kann.
Analyse
Das Fraunhofer-Institut für Mikrotechnik und Mikrosysteme (IMM) hat ein vollautomatisiertes System für die Liquid Biopsy zur Isolierung einzelner Tumorzellen (CTCs) aus Patientenblut entwickelt. Zunächst werden die Tumorzellen mittels immunomagnetischer Separation (IMS) aus der Probe isoliert und in ein kleineres Probenvolumen überführt. Anschließend wird der Extrakt zur Entfernung des unspezifischen Zellhintergrundes in eine mikrofluidische Kartusche überführt, in der die Krebszellen durchflusszytometrisch erkannt werden. Nach Erkennen einer Tumorzelle im Mikrokanal werden die einzelnen Zielzellen mittels eines Druckstoßes direkt in Kavitäten einer Mikrotiterplatte dispensiert.[21]
Klinische Bewertung
Die Deutsche Gesellschaft für Pathologie (DGP) sieht den Einsatz der Liquid Biopsy unter Vorbehalt. Es gäbe derzeit bei dem Verfahren zu große Unsicherheiten, um damit verlässliche Aussagen zur Früherkennung, Diagnostik, Therapie, Verlauf oder Prognose von Krebserkrankungen treffen zu können. Zellfreie, zirkulierende Tumor-DNA ist nicht bei allen, sondern nur bei etwa 70 Prozent der metastasierten Tumorerkrankungen nachzuweisen. Es kann daher in einzelnen Fällen zu falsch-negativen Ergebnissen kommen. Es seien große Unterschiede zwischen unterschiedlichen Tumortypen und in Abhängigkeit vom Tumorstadium feststellbar. Für Hirntumoren sei der cfDNA-Nachweis wegen der Blut-Hirn-Schranke ungeeignet, da nur extrem wenige DNA-Fragmente im Blut aufgefunden werden konnten. Noch mangele es an einer Standardisierung bestehender cfDNA-Isolations- und Analysetechnologien sowie am Qualitätsmanagement der Probenbearbeitung.[22]
Die Liquid Biopsy kann unter bestimmten Bedingungen die Tumordiagnostik ergänzen, beispielsweise wenn kein Primärtumor gefunden wird, so beim nichtkleinzelligen Bronchialkarzinom (englisch non small cell lung cancer, NSCLC). Hier erfolgt die Liquid Biopsy zum Nachweis einer EGFR-T790M-Mutation. Die Mutation des epidermalen Wachstumsfaktor-Rezeptors (englisch Epidermal Growth Factor Receptor, EGFR) ersetzt ein Threonin (T) durch ein Methionin (M) an Position 790 von Exon 20.[23] Zu den aktivierenden Mutationen des EGFR zählen ferner die Mutation vom Exon 21 und Exon 19. Die aktivierenden Mutationen des EGFR können dauerhaft Wachstumssignale aussenden und so zum unkontrollierten Wachstum des Tumors beitragen. Osimertinib wurde 2017 sowohl von der FDA als auch der Europäischen Kommission für die Therapie des NSCLC zugelassen.[24]
Weiterführende Literatur
- Andreas Jung, Thomas Kirchner: Liquid Biopsy in der tumorgenetischen Diagnostik, (Review). In: Deutsches Aerzteblatt Online. 2018, doi:10.3238/arztebl.2018.0169 – (deutsche Fassung).
- Daniela Zimmermann, Walter Depner, Circulating biomarkers – the great white hope of liquid biopsy, Health care in Europe, 20. März 2017. Abgerufen am 4. März 2019.
Einzelnachweise
- Liquid Biopsy: Flüssige Biopsie, Krebsinformationsdienst, 15. Januar 2018. Abgerufen am 22. Februar 2019.
- Merkelzell-Karzinom: Neuer Biomarker entdeckt, Universität Duisburg-Essen, Health Care in Europe, 28. Januar 2019.
- Alessia Finotti, Matteo Allegretti u. a.: Liquid biopsy and PCR-free ultrasensitive detection systems in oncology (Review). In: International Journal of Oncology. 2018, doi:10.3892/ijo.2018.4516.
- Urine liquid biopsies could help monitor bladder cancer treatment, 26. September 2018. Abgerufen am 23. Februar 2019.
- A. Di Meo, J. Bartlett u. a.: Liquid biopsy: a step forward towards precision medicine in urologic malignancies. In: Molecular cancer. Band 16, Nummer 1, 04 2017, S. 80, doi:10.1186/s12943-017-0644-5, PMID 28410618, PMC 5391592 (freier Volltext) (Review).
- Maria Rita Gaiser, Nikolas von Bubnoff, Christoffer Gebhardt, Jochen Sven Utikal: Liquid Biopsy zur Überwachung von Melanompatienten. In: JDDG: Journal der Deutschen Dermatologischen Gesellschaft. 16, 2018, S. 405, doi:10.1111/ddg.13461_g.
- Bedeutung exosomaler DNA aus Speichel beim duktalen Pankreaskarzinom, Deutsche Forschungsgemeinschaft. Abgerufen am 23. Februar 2019.
- Dipesh Kumar Yadav, Xueli Bai u. a.: Liquid biopsy in pancreatic cancer: the beginning of a new era. In: Oncotarget. 9, 2018, doi:10.18632/oncotarget.24809.
- Pressemitteilung Universitätsklinikum Heidelberg, 21. Februar 2019.
- J. Cheng, K. Cuk, J. Heil, M. Golatta, S. Schott, C. Sohn, A. Schneeweiss, B. Burwinkel, H. Surowy: Cell-free circulating DNA integrity is an independent predictor of impending breast cancer recurrence. In: Oncotarget. Band 8, Nummer 33, August 2017, S. 54537–54547, doi:10.18632/oncotarget.17384, PMID 28903362, PMC 5589601 (freier Volltext).
- Jens-Uwe Blohmer, Annette Hasenburg, Wolfgang Janni: Gemeinsame Stellungnahme zur Berichterstattung über neuen Bluttest zur Früherkennung bei Brustkrebs. Arbeitsgemeinschaft Gynäkologische Onkologie e.V., 27. Februar 2019, abgerufen am 8. März 2019.
- Krebstest als "Meilenstein" beworben - Uniklinik entschuldigt sich, Spiegel online, 22. März 2019. Abgerufen am 24. März 2019.
- Universität erstattet Anzeige nach Bluttest-PR, Süddeutsche Zeitung, 8. April 2019. Abgerufen am 14. April 2019.
- K. Bethel, M. S. Luttgen u. a.: Fluid phase biopsy for detection and characterization of circulating endothelial cells in myocardial infarction. In: Physical biology. Band 11, Nummer 1, Februar 2014, S. 016002, doi:10.1088/1478-3975/11/1/016002, PMID 24406475, PMC 4143170 (freier Volltext).
- M. Allyse, M. A. Minear, E. Berson, S. Sridhar, M. Rote, A. Hung, S. Chandrasekharan: Non-invasive prenatal testing: a review of international implementation and challenges. In: International journal of women's health. Band 7, 2015, ISSN 1179-1411, S. 113–126, doi:10.2147/IJWH.S67124, PMID 25653560, PMC 4303457 (freier Volltext).
- M. Nascimento da Silva, L. B. Sicchieri u. a.: Liquid biopsy of atherosclerosis using protoporphyrin IX as a biomarker. In: The Analyst. Band 139, Nummer 6, März 2014, S. 1383–1388, doi:10.1039/c3an01945d, PMID 24432352.
- O. T. Pyykkö, M. Lumela u. a.: Cerebrospinal fluid biomarker and brain biopsy findings in idiopathic normal pressure hydrocephalus. In: PLOS ONE. Band 9, Nummer 3, 2014, S. e91974, doi:10.1371/journal.pone.0091974, PMID 24638077, PMC 3956805 (freier Volltext).
- S. E. Norton, J. M. Lechner u. a.: A stabilizing reagent prevents cell-free DNA contamination by cellular DNA in plasma during blood sample storage and shipping as determined by digital PCR. In: Clinical biochemistry. Band 46, Nummer 15, Oktober 2013, S. 1561–1565, doi:10.1016/j.clinbiochem.2013.06.002, PMID 23769817.
- Informationen zur Blutabnahme für die T790M-Testung an Liquid Biopsies, Institut für Pathologie Charité – Universitätsmedizin Berlin. Abgerufen am 24. Februar 2019.
- Andreas Jung, Thomas Kirchner: Liquid Biopsy in Tumor Genetic Diagnosis. In: Deutsches Aerzteblatt Online. 2018, doi:10.3238/arztebl.2018.0169.
- Liquid Biopsy, Fraunhofer-Institut für Mikrotechnik und Mikrosysteme, 2019. Abgerufen am 5. März 2019.
- E. Dahl, A. Jung, u. a.: Chancen und Risiken der blutbasierten molekularpathologischen Analytik zirkulierender Tumorzellen (CTC) und zellfreier DNA (cfDNA) in der personalisierten Krebstherapie. In: Der Pathologe. 36, 2015, S. 92, doi:10.1007/s00292-014-2069-x.
- D. Ayeni, K. Politi, S. B. Goldberg: Emerging Agents and New Mutations in EGFR-Mutant Lung Cancer. In: Clinical Cancer Research. Band 21, Nummer 17, September 2015, S. 3818–3820, doi:10.1158/1078-0432.CCR-15-1211, PMID 26169963, PMC 4720502 (freier Volltext).
- European Tagrisso information, Europäische Arzneimittelkommission, Abgerufen am 24. Februar 2019.