CTLA-4
CTLA-4 oder CTLA4 (engl. für cytotoxic T-lymphocyte-associated Protein 4), auch benannt als CD152 (engl. für cluster of differentiation 152) ist ein Protein, das in der Regulierung des Immunsystems eine wichtige Rolle spielt. Dieses Protein CTLA-4 wird speziell an der Zelloberfläche von T-Zellen exprimiert, welche die Immunantwort auf Antigene anführen. T-Zellen werden dabei durch bestimmte Rezeptoren (wie z. B. CD28) stimuliert, wobei eine Überreaktion des Immunsystems durch CTLA-4 herunterreguliert und so verhindert wird. Dieses Protein wird beim Menschen am Chromosom 2 kodiert.[1]
| CTLA-4 | ||
|---|---|---|
| ||
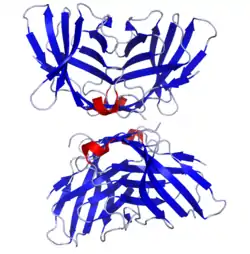
| Struktur des murinen CTLA4 Rezeptors (CD152) | ||
|
Vorhandene Strukturdaten: 1AH1, 1H6E, 1I85, 1I8L, 2X44, 3BX7, 3OSK | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 223 Aminosäuren | |
| Bezeichner | ||
| Gen-Namen | CTLA4 CD; CD152; CELIAC3; CTLA-4; GRD4; GSE; IDDM12 | |
| Externe IDs | ||
| Orthologe | ||
| Mensch | Maus | |
| Entrez | 1493 | 12477 |
| Ensembl | ENSG00000163599 | ENSMUSG00000026011 |
| UniProt | P16410 | P09793 |
| Refseq (mRNA) | NM_001037631 | NM_009843 |
| Refseq (Protein) | NP_001032720 | NP_033973 |
| Genlocus | Chr 2: 204.73 – 204.74 Mb | Chr 1: 60.89 – 60.92 Mb |
| PubMed-Suche | 1493 | 12477 |
Funktion und Wirkungsweise
CTLA-4 ist ein wichtiges Mitglied der Immunglobulin-Superfamilie, das auf der Oberfläche von T-Helferzellen, zytotoxischen T-Zellen, aber auch regulatorischen T-Zellen exprimiert wird.[2] T-Zellen an sich benötigen zwei Signale, damit sie aktiv werden, um sich zu teilen und sich zu differenzieren. Das erste Signal ist Antigen-abhängig, während das zweite Signal co-stimulierend wirkt und alleine keine Reaktion durch die T-Zelle hervorruft.[1] Gleichzeitig jedoch veranlasst eine Aktivierung von T-Lymphozyten durch den T-Zell-Rezeptor eine gesteigerte Produktion des CTLA-4 Rezeptors an der Oberfläche der T-Zelle.[3] Dieser Rezeptor CTLA-4 vermittelt ein hemmendes Signal, um eine Überreaktion des Immunsystems zu vermeiden.[2]
CTLA-4 wirkt dabei antagonistisch zum Komplex der immunologischen Synapse (CD80-CD86-CD28) und bindet an CD80/CD86, sodass CD28 ungebunden bleibt. Über den CTLA-4-Komplex wird eine Proteinkinase aktiviert, die anschließend die Downregulation des Proliferationssignals bewirkt. Folglich werden antigenpräsentierende Zellen weniger stimuliert und die Intensität einer möglichen Immunantwort sinkt.
Struktur
Das Protein CTLA-4 weist eine extrazelluläre V-förmige Domäne sowie eine transmembrane Domäne auf.[2] CTLA-4 ist von der Struktur her auch ähnlich zu dem co-stimulierenden Rezeptor CD28, wobei beide Rezeptoren auch an CD80 und CD86 (auch benannt als B7-1 und B7-2) binden.[1] CD80 und CD86 sind zwei Proteinen an den Antigen-präsentierenden Zellen. Dabei kommt es bei der Bindung an CD80 oder CD86 zu einem Wettstreit zwischen einem hemmenden Signal (durch CTLA-4) sowie einem co-stimulierenden Signal (durch CD28).[4]
Klinische Bedeutung
Das Protein CTLA-4 stellt ein mögliches klinisches Ziel dar, um entweder die Wirkung von CTLA-4 zu verstärken (Agonist), oder aber dessen Wirkung abzuschwächen (Antagonist). Der monoklonale Antikörper Ipilimumab zum Beispiel ist ein Antagonist, der an CTLA-4 bindet und dessen Wirkung abschwächt. Auf diese Weise löst er antitumorale Effekte in der frühen Phase der T-Zellaktivierung aus und verstärkt die Bekämpfung von malignen Melanomen durch das Immunsystem. Ipilimumab wurde als erster Checkpointinhibitor in den USA 2011 für die Immuntherapie des metastasierten Melanoms zugelassen. Dies basierte auf den Daten einer klinischen Studie beim metastasierten Melanom, die mit einer anhaltenden Tumoransprechrate von 10–15 % einen signifikanten Überlebensvorteil gegenüber einer Standardtherapie belegte.[5][6] Im Gegensatz dazu versucht das Fusionsprotein Abatacept die Wirkung von CTLA4 zu verstärken und so Autoimmunerkrankungen erfolgreich zu therapieren.
CTLA-4-Defizienz
Bei der CTLA-4-Defizienz kann es durch eine seltene angeborene Mutation im CTLA4 Gen zu einem Immundefekt- und Immundysregulationssyndrom kommen. Die Vererbung erfolgt autosomal-dominant, die Veranlagung wird also mit einer Wahrscheinlichkeit von 50 % vererbt. Es besteht allerdings eine reduzierte Penetranz und Expressivität, was bedeutet, dass nicht alle Mutationsträger erkranken und das klinische Bild der symptomatischen Mutationsträger unterschiedlich stark ausgeprägt sein kann. Diese Variabilität wirft die Frage der Existenz möglicher modifizierender Faktoren auf, die genetisch oder durch Umweltfaktoren bedingt sein können.
Klinisches Bild
Das klinische Bild der CTLA-4-Defizienz ist sehr variabel und besteht häufig aus einem Symptomkomplex aus Antikörpermangel, rezidivierenden respiratorischen Infekten, sowie Autoimmunität, lymphozytären Organinfiltrationen und Enteropathien mit Durchfall.
Therapie
Die Therapie richtet sich stark nach den Symptomen der einzelnen Patienten. Häufig ist eine Substitution der fehlenden Antikörper durch regelmäßige Infusionen notwendig, außerdem kommen verschiedene immunsuppressive Medikamente zur Stabilisierung des Immunsystems zum Einsatz. Eine weitere Möglichkeit ist der Einsatz des Medikamentes Abatacept, das zumindest teilweise die Funktion des fehlenden körpereigenen CTLA-4 ersetzen kann.
Einzelnachweise
- McCoy Kathy: The role of CTLA-4 in the regulation of T cell immune responses. In: Immunology and Cell Biology. 77, 1999, S. 1–10. doi:10.1046/j.1440-1711.1999.00795.x.
- Sansom D.: CD28, CTLA-4 and their ligands: who does what and to whom?. In: Immunology. 101, 2000, S. 169–177. doi:10.1046/j.1365-2567.2000.00121.x.
- M. L. Baroja, L. Vijayakrishnan, E. Bettelli, P. J. Darlington, T. A. Chau, V. Ling, M. Collins, B. M. Carreno, J. Madrenas, V. K. Kuchroo: Inhibition of CTLA-4 function by the regulatory subunit of serine/threonine phosphatase 2A. In: Journal of Immunology (Baltimore, Md.: 1950). Band 168, Nummer 10, Mai 2002, S. 5070–5078, ISSN 0022-1767. PMID 11994459, doi:10.4049/jimmunol.168.10.5070.
- Krummel M.F.: CD28 and CTLA-4 have opposing effects on the response of T cells to stimulation. In: J Exp Med.. 182, 1995, S. 459–465. PMID 7543139.
- Hodi FS, O’Day SJ, McDermott DF et al. (2010) Improved survival with ipilimumab in patients with metastatic melanoma. N Engl J Med 363:711–723
- Zusammenfassung der Merkmale des Arzneimittels. (PDF) EMA, abgerufen am 4. August 2014 (englisch).