Geflügelpest
Die Geflügelpest wird auch als aviäre Influenza (von lateinisch avis, Vogel[1]), als Vogelgrippe und seit 1981 überwiegend als hochpathogene Influenza-Virus-Infektion (HPAI, Highly Pathogenic Avian Influenza) bezeichnet. Sie ist eine durch Viren hervorgerufene anzeigepflichtige Tierseuche, von der Hühner, Puten, Gänse, Enten, wildlebende Wasservögel und andere Vögel im Freiland und in menschlicher Obhut betroffen sein können. Bei einer Infektion mit den aggressiveren Virusstämmen führt sie meist zum Tod der infizierten Vögel, sofern sie nicht zu den Reservoirwirten gehören. Einige Varianten der Geflügelpest-Viren, insbesondere die Variante A/H5N1, sind in Einzelfällen auf Menschen, Zootiere wie Leoparden sowie auf Hauskatzen übertragen worden. HPAIV und LPAIV der Subtypen A/H5 und A/H7 bei Wildvögeln und Hausgeflügel unterliegen dem Tierseuchenrecht und sind daher anzeigepflichtig.
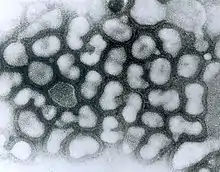
Die Geflügelpest wurde erstmals 1878 in Italien beobachtet.[2] In den 1930er Jahren gab es in Europa, Amerika und Asien mehrere Ausbrüche. Als die Vogelgrippe sich 1983 in Irland und den USA ausbreitete, wurden dort zur Eindämmung der Ausbrüche Millionen Vögel getötet. Je einen weiteren großen Ausbruch gab es u. a. 1992 in Mexiko, 1997 in Hongkong, 2015 in den USA, 2016/2017 sowie 2020/2021 in Deutschland, besonders in den putendichten Regionen Niedersachsens.[3][4]
Als Folge der Ereignisse im Zusammenhang mit der Vogelgrippe H5N1, der Vogelgrippe H7N9 und der Vogelgrippe H5N8 erfuhren die Influenza-Subtypen A/H5N1, A/H7N9 und A/H5N8 besondere Aufmerksamkeit in den Medien.
Ob es sich beim sogenannten Englischen Schweiß, der im 15. und 16. Jahrhundert mit einem Vogelsterben einherging, ebenfalls um eine Erkrankung durch Influenzaviren handelte, ist ungesichert.
Erreger
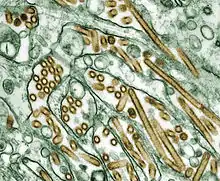
Der Erreger der klassischen Geflügelpest (KP) ist ein als hoch pathogenes aviäres Influenzavirus (HPAIV) bezeichnetes Influenza-A-Virus (also Grippevirus) und damit ein behülltes Einzel(-)-Strang-RNA-Virus [ss(-)RNA] aus der Familie der Orthomyxoviren.
Generell werden nach dem OIE Manual 3 Typen unterschieden.
- LPAIV (Low pathogenic Avian Influenza Virus): gering pathogenes Virus, nicht Subtyp H5, H7
- LPNAIV (Low pathogenic notifiable Influenza Virus): gering pathogenes Virus (IVPI < 1.2 bzw. entsprechende Hämagglutinin Sequenz) des Typs H5 oder H7
- HPNAIV (Highly pathogenic notifiable Influenza Virus): hoch pathogenes Virus (IVPI > 1.2 bzw. typische Hämagglutinin-Sequenz mit basischen Aminosäuren an der Spaltstelle) des Typs H5 oder H7
Die korrekte Bezeichnung eines Influenzavirus würde wie folgt lauten: A/goose/Guangdong/1/96 (H5N1): "A" für den Influenza-Subtyp (A, B oder C); "goose" für die englische Bezeichnung des Wirts, aus welchem das Virus erstmals isoliert wurde; "Guangdong" für die Ortsbezeichnung des ersten Auftretens, die erste Zahl steht für die Nummer der Probe und die zweite Zahl bezeichnet das Jahr.
Erst 1954 wurde durch den damals in Tübingen am Max-Planck-Institut für Virusforschung tätigen deutschen Virologen Werner Schäfer endgültig nachgewiesen, dass die Viren der Influenza des Menschen und der klassischen Geflügelpest der gleichen Gruppe zuzuordnen sind.[5]
Subtypen und Pathogenität
Als Folge von Genveränderungen entstehen ständig neue Varianten der Grippeviren. Diese Varianten werden anhand bestimmter Oberflächeneigenschaften in Subtypen eingeteilt (zur genauen Erläuterung der Variabilität der Erreger siehe unter Influenza). Man unterscheidet 18 H-Untertypen und 11 N-Untertypen. Der Typ A/H5N1 etwa hat auf seiner Oberfläche die 5. Variante des Hämagglutinins (H5) sowie die 1. Variante der Neuraminidase (N1). Diese Untertypen befallen üblicherweise jeweils nur bestimmte Wirte, während sie von einer weiteren Anzahl an Infektionsvektoren verbreitet werden können, ohne dass diese Tiere erkranken.
Durch Mutationen können sich aber sowohl die Wirtsarten als auch die krankmachenden Eigenschaften erheblich verändern. Hierbei spielt das Oberflächenprotein Hämagglutinin eine wichtige Rolle, welches für die Erkennung und Anheftung des Virions an die Wirtszelle verantwortlich ist. Dieses Hämagglutinin wird als Precursor HA0 gebildet und muss anschließend durch bestimmte Enzyme des Wirtes, sogenannte Proteasen, in zwei Untereinheiten (HA1 & HA2) gespalten werden, damit die Viren neue Zellen infizieren können.
Das Hämagglutinin der gering pathogenen Virusstämme (sie werden auch als minder pathogen bezeichnet bzw. auf Englisch abgekürzt als LPAI) kann nur von extrazellulären Trypsin-ähnlichen Proteasen gespalten werden, welche nur im Atem- und Verdauungstrakt vorhanden sind und somit die Infektion lokal begrenzen.
Die Spaltstelle von hoch pathogenen Virusstämmen (HPAI) enthält basische Aminosäuren, so dass sie von ubiquitär vorhandenen, intrazellulären, sogenannten Furin-ähnlichen Proteasen gespalten wird und somit eine Infektion des ganzen Wirtes erlaubt.
Hoch pathogene Varianten sind bisher nur von den HA-Subtypen H5 und H7 bekannt.[6]
Bei Wasservögeln wie Enten und Gänsen wurden viele der möglichen Kombinationen von H und N nachgewiesen, auch minder pathogene Varianten von A/H5N1. Da bisher kein natürliches Reservoir für hoch pathogene Varianten der Geflügelpest-Viren nachweisbar war, gehen die Virologen derzeit davon aus, dass der Übergang von einem minder pathogenen in einen hoch pathogenen Zustand die Folge einer Mutation war, die es zugleich erlaubt, die Artenbarriere von Entenvögeln (Anatidae) zu Hühnervögeln (Galliformes) zu überwinden. Laut Science vom Oktober 2005[7] fanden solche Übergänge seit 1959 mindestens 19 mal statt und hatten jeweils eine Epidemie unter Zuchtgeflügel zur Folge. In einigen dieser Fälle konnte sogar der Weg von minder pathogenem Zustand bei Wasservögeln über minder pathogenen Zustand bei Hühnervögeln zu hoch pathogenem Zustand bei Hühnervögeln nachvollzogen werden. In Bezug auf die Ausbreitung der Vogelgrippe H5N1 hieß es im Juni 2006 jedoch ergänzend, dass der kommerzielle Geflügelhandel den Hauptübertragungsweg darstelle.[8]
Das Risiko eines Übergangs aus infizierten Intensivtierhaltungen auf Wildvögel stellt ein bislang nur wenig beachtetes Problem dar. In Intensivhaltungsställen können wegen der großen Haltungsdichte Krankheitserreger rasch übertragen werden, und aus Kot entsteht in Verbindung mit Einstreu, Hautschuppen und Federbruchstücken ein potenziell hoch infektiöser Feinstaub, der mit der zumeist ungefilterten Abluft weiträumig auf die umliegenden Ackerflächen verteilt werden kann, so dass Erreger von äsenden Gänsen oder anderen Wildvögeln aufgenommen werden können. Die Düngung mit Geflügelmist stellt einen weiteren möglichen Übertragungsweg auf Wildvögel dar. Insgesamt sind Bestände von Wildvögeln und Betriebe mit freilaufendem Geflügel daher als biosicherer zu beurteilen als Geflügel-Großbetriebe, die weltweit miteinander vernetzt sind: So lassen sich verinselte Vorkommen bestimmter Erregertypen nur mit Handelswegen, nicht aber mit Vogelzugwegen erklären.[9]
Besonders großen Schaden in Geflügelhaltungen verursacht haben insbesondere folgende Subtypen:
A/H5N1
Der Subtyp A/H5N1 gilt als besonders aggressiv (HPAI, Highly Pathogenic Avian Influenza). Ein verändertes Nichtstruktur-Gen führt bei ihm dazu, dass bestimmte Botenstoffe des Immunsystems, welche normalerweise Viren abwehren, keine Wirkung mehr gegenüber dem A/H5N1-Subtyp erzielen. Deshalb tötet er befallene Vögel, die nicht zu seinem Virusreservoir gehören, sehr schnell und wird von Wissenschaftlern wegen seiner pathogenen Eigenschaften auf Interdependenzen mit anderen Stämmen und Überschreitungen der Artengrenze aufmerksam beobachtet; laut Weltgesundheitsorganisation ist A/H5N1 der einzige Subtyp der H5-Gruppe, der auf Menschen übertragbar ist. Weitere Einzelheiten zu den aktuellen Ausbrüchen von A/H5N1 unter Geflügel und Menschen siehe unter Vogelgrippe H5N1 und Verbreitung von H5N1.
Erstmals trat ein hoch pathogenes aviäres A/H5N1-Virus 1959 in Hühnervögeln in Schottland auf: A/chicken/Scotland/59 (H5N1).[10]
A/H5N2
Der Subtyp A/H5N2 trat u. a. im Sommer 2005 in Japan auf, weswegen Presseberichten zufolge mehr als 1,5 Millionen Hühner und anderes Geflügel getötet wurden. Bereits in den Jahren 1983 und 1984 hatte es mehrere Ausbrüche in Geflügelfarmen der USA gegeben, in deren Folge 17 Millionen Tiere getötet wurden. Zwischen 1992 und 1995 gab es zudem mehrere Ausbrüche in Mexiko. Im Dezember 2008 wurde ein niedrig pathogenes H5N2 Virus in Belgien und Deutschland festgestellt. Dies führte zur Keulung von drei Geflügelbeständen in Niedersachsen.
A/H5N3
Der Subtyp A/H5N3 verursachte im Jahr 1961 in Südafrika ein großes Sterben unter frei lebenden Seeschwalben. Dies war zugleich der erste Nachweis von Influenzaviren in einer Wildvogelpopulation.[11] Im Oktober 2008 wurde ein niedrig pathogenes H5N3-Virus im Rahmen einer Routinekontrolle in einer Gans des Leipziger Zoos nachgewiesen. Im gleichen Jahr kam es zu Ausbrüchen in mehreren Nutzgeflügelbetrieben im Landkreis Cloppenburg, Niedersachsen.[12] Daraufhin wurden in dieser Region bis Ende Januar 2009 über 560.000 Stück Geflügel getötet.[13]
A/H7N1
Ab März 1999 kam es in Italien zu einer massiven Epidemie des Subtyps A/H7N1, in deren Folge bis Anfang 2000 mehr als 13 Millionen Tiere betroffen waren. Eine Übertragung auf den Menschen war nicht nachweisbar.[14]
A/H7N3
In Nordamerika wurde die Ausbreitung des Subtyps A/H7N3 mehrmals bestätigt. Zuletzt im April 2004 wurden 18 Farmen in British Columbia unter Quarantäne gestellt und zwei Fälle von Übertragung auch auf Menschen dokumentiert.[15]
A/H7N7
In den Niederlanden wurden 2003 89 Infektionen von Menschen mit dem (HPAI, Highly Pathogenic Avian Influenza) Subtyp A/H7N7 bestätigt. Ein Fall verlief tödlich. Dabei handelte es sich um einen Tierarzt, bei dem dieser Virussubtyp im Lungengewebe nachgewiesen werden konnte. Außerdem mussten 30.000 Nutzvögel getötet werden.[15] 1996 kam es zu einer Infektion im Vereinigten Königreich.[16] 2013 wurde in China beim Versuch, die dem Ausbruch der Vogelgrippe H7N9 vorhergehende Reassortierung von Influenza-A-Viren zu rekonstruieren, eine bis dahin unbekannte Variante von A/H7N7 aus frei verkäuflichen Hühnern isoliert, die im Labor auch auf Frettchen übertragbar war;[17] Frettchen gelten bezüglich Influenza als Modellorganismus für den Menschen.
A/H7N9
Vermutlich nach Kontakt mit infiziertem Geflügel kam es im Februar 2013 erstmals auch zu Infektionen von Menschen durch die sogenannte Vogelgrippe H7N9 und als deren Folgen zu Todesfällen bei Menschen durch das Influenza-A-Virus H7N9 in der Volksrepublik China.[18]
Übertragung
Die Geflügelpest kann alle Vogelarten infizieren. Als natürliches Reservoir für das Virus gelten wild lebende Enten und andere Wasservögel, die jedoch in der Regel nicht schwer erkranken, denn das Virus hat sich ihnen angepasst. Es benötigt diese Reservoirwirte für seine Vermehrung. Stärker gefährdet sind vor allem Hühner und Puten, aber auch Fasane, Wachteln, Perlhühner und Wildvögel. Wanderwasservögel, See- und Küstenvögel sind weniger anfällig zu erkranken. Sie sind jedoch Vektoren und ihr Wanderverhalten trägt zur weiten geografischen Verbreitung bei. Tauben sollen zwar selbst nicht sehr empfänglich für Vogelgrippeviren sein, es wird jedoch befürchtet, dass sie die Erreger als mechanische Vektoren im Gefieder verbreiten. So wurde vom nordrheinwestfälischen Landesumweltministerium während einer grassierenden Geflügelpest im Jahre 2003 ein Taubenflugverbot ausgerufen.
Säugetiere sind weniger empfänglich für das Virus, werden aber – wie zum Beispiel Hausschweine – gelegentlich infiziert. Aus Thailand wurde berichtet, dass in zwei Zoos Tiger und Leoparden nach dem Verzehr von infiziertem Geflügel an A/H5N1 starben.
Grundsätzlich beobachtet man die gleichen Infektionswege wie bei anderen Influenzaviren. Die Viren verbreiten sich durch Tröpfcheninfektion über die eingeatmete Luft oder über Kotpartikel an der Kleidung und Geräten. Außerhalb ihrer Wirte sind die Erreger der Vogelgrippe meistens nur wenige Tage, unter günstigsten Bedingungen viele Monate lang funktionsfähig. Aviäre Influenzaviren bleiben im Allgemeinen 105 Tage in Flüssigmist, 30 bis 35 Tage in Kot und Geflügelfleisch oder Eiern bei 4 °C und sieben Tage lang bei 20 °C intakt. Nach bisherigen Erkenntnissen ist eine Übertragung über durchgegarte Geflügel- und andere Fleischprodukte ausgeschlossen.
Symptome
Die akute Form der Geflügelpest äußert sich in Zeichen allgemeiner Schwäche (Apathie, Inappetenz, stumpfes, struppiges Federkleid), hohem Fieber, erschwerter Atmung mit geöffnetem Schnabel, Ödemen an Kopf, Hals, Kamm, Kehllappen, Beinen und Füßen, Blauverfärbung der Haut und der Schleimhäute, wässerig-schleimigem und grünlichem Durchfall und neurologischen Störungen (sonderbare Haltung des Kopfes, Störungen der Motorik).
Bei chronischem Verlauf sinkt die Legeleistung, die Eier sind dünnwandig oder schalenlos.
Die Mortalität ist abhängig vom Alter der Tiere und der Virulenz des Erregers. Bei hochvirulenten Erregern endet die Krankheit bei nahezu allen Tieren tödlich. Mehr als 15 % einer Geflügelherde können sterben, bevor Symptome auftreten (perakuter Verlauf).
Bekämpfung
Bei Ausbrüchen der Geflügelpest in der Tierhaltung wird regelmäßig der gesamte Tierbestand der betroffenen Halter getötet. Die Kadaver werden verbrannt oder auf andere Weise unschädlich gemacht, um eine Übertragung auf andere Tierbestände zu verhindern. Daher ist die Anzahl der getöteten Tiere regelmäßig sehr viel größer als die Zahl der nachweislich infizierten Tiere.
Grundsätzlich können die Tiere auch durch eine vorbeugende Impfung wirksam gegen Geflügelpest geschützt werden. Ein Lebendimpfstoff auf Basis gering pathogener Erreger scheidet jedoch nach heutigem Stand des Wissens wegen des Mutationsrisikos aus. Eine Immunisierung mit inaktivierten Influenzaviren ist unter den Fachleuten aber ebenfalls umstritten, da kein bisher verfügbarer Impfstoff eine spätere Infektion, die nachfolgende Virusvermehrung und das Ausscheiden pathogener Viren verhindert; verhindert wird vielmehr nur die klinische Erkrankung der geimpften Tiere. So können geimpfte Tiere zu Virusträgern werden und pathogene Viren weiterverbreiten. Ein weiteres Problem ist die sichere (mikrobiologische/serologische) Unterscheidung der geimpften Tiere von erkrankten oder ansteckenden Tieren.
Als Ausweg aus diesem Dilemma wurden in Mittelamerika und Ostasien daher bereits Impfstoffe entwickelt und – speziell gegen A/H5N1 – bereits eingesetzt, die aus abgeschwächten Geflügelpocken-Viren bestehen, denen das Hämagglutinin H5 eingefügt wurde. Eine deutsche Forschergruppe des Friedrich-Loeffler-Instituts versucht u. a., einen gebräuchlichen Impfstamm gegen die Newcastle-Krankheit gentechnisch so zu verändern, dass er zur Impfung gegen H5 bzw. H7 verfügbar wird. Bei derart geimpften Tieren könnte später durch geeignete Antikörper-Nachweistests unterschieden werden, ob sie nur eine Immunantwort gegen den Impfstoff zeigen oder – im Falle einer Virusinfektion – gegen die pathogenen Viren.[19] Arbeiten an der Tierärztlichen Hochschule Hannover deuten darauf hin, dass der Einsatz von Markerimpfstoffen auf der Basis eines nicht-übertragbaren Virus der vesikulären Stomatitis (VSV) Erfolge bei der Unterscheidung von infizierten und vakzinierten Tieren und der Sicherheit bringen könnten.[20]

In Deutschland erfolgt die Bekämpfung der Geflügelpest auf Rechtsgrundlage des Tierseuchengesetzes und der Geflügelpest-Verordnung, in der im Oktober 2007 mehrere andere Verordnungen zusammengefasst wurden, die nach dem erstmaligen massiven Auftreten von A/H5N1 erlassen worden waren.
Zur Bekämpfung der sich 2016 auch in Deutschland wieder ausbreitenden Vogelgrippe wurden bestehende Regelungen per Rechtsverordnung[21] temporär auch auf kleinere Haltungen ausgedehnt.
Wegen der bei vielen Vögeln vorhandenen Übertragungsmöglichkeiten des Krankheitserregers (Vektoreigenschaften) muss der Handel oder die Zucht von beispielsweise Papageien und Sittichen behördlich genehmigt werden. Diese nichtheimischen Vogelspezies neigen trotz Käfighaltung zu gelegentlichem Entweichen und können daher auch zu einer unkontrollierten Ausbreitung der Geflügelpest beitragen, wie zuletzt 2004/2005 in Köln geschehen.
Gentechnik
Britische Wissenschaftler von der Universität Cambridge, Universität Edinburgh und der Veterinary Laboratories Agency haben transgene Hühner entwickelt, welche die Geflügelpest nicht übertragen können. Die Hühner wurden mit einer Expressionskassette ausgestattet, welche ein Stück RNA produziert, die als Köder für Polymerase dient. Anstatt an das Virusgenom zu binden und dem Virus damit zur Replikation zu verhelfen, hängt sich die Polymerase dann an diesen Köder. Die transgenen Hühner starben zwar noch an der Geflügelpest, infizierten aber keine anderen Hühner mehr. Ziel ist die komplette Immunisierung von Hühnern gegen A/H5N1.[22] Noch 2019 sollen am Roslin-Institut an der Universität Edinburgh die ersten genetisch veränderten Tiere mit einer vollständigen Immunität ausgebrütet werden.[23]
Siehe auch
Literatur
- David E. Swayne (Hrsg.): Avian Influenza. Blackwell Publishing, 2008, ISBN 978-0-8138-2047-7.
Weblinks
- Was versteht man unter „Vogelgrippe“ und Geflügelpest? Antworten des deutschen Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz.
- Vogelgrippe beim Tier – Informationen des Schweizer Bundesamts für Lebensmittelsicherheit und Veterinärwesen
- Österreichischer Influenza Pandemieplan. (PDF) (Memento vom 27. Juni 2016 im Internet Archive) (Stand: 2006)
- Merkblatt Klassische Geflügelpest (PDF; 765 kB) Friedrich-Loeffler-Institut
- RKI-Ratgeber: Influenza (Teil 2): Erkrankungen durch zoonotische Influenzaviren. Robert Koch-Institut
- deutsche Verordnung zum Schutz gegen die Geflügelpest, Fassung vom 5. Oktober 2018. Bundesministerium der Justiz
- deutsches Tiergesundheitsgesetz
- Avian and other zoonotic influenza. Weltgesundheitsorganisation (WHO)
- Foreign animal diseases, the grey book. (PDF; 4,6 MB) Studie des Committee on Foreign Animal Diseases of the U.S. Animal Health Association aus dem Jahr 2008 (englisch)
- Internationale Gesellschaft für Infektionskrankheiten: The Program for Monitoring Emerging Diseases. (englisch)
Belege
- Adjektiv aviär „auf Vögel bezogen“, „von Vögeln stammend“ von lateinisch avis, „Vogel“
- Jacqueline P. Jacob et al.: Avian Influenza in Poultry. Quelle: The Institute of Food and Agricultural Sciences (IFAS) der University of Florida, Stand: April 2014; abgerufen am 5. Juni 2015.
- Geflügelwirtschaft: Bundesweit bislang 1,4 Millionen Tiere wegen Vogelgrippe getötet. In: animal-health-online.de, 23. März 2021, abgerufen am 25. März 2021.
- Aviäre Influenza. Niedersächsisches Landesamt für Verbraucherschutz und Lebensmittelsicherheit. Abgerufen am 25. März 2021.
- Werner Schäfer: Vergleichende sero-immunologische Untersuchungen über die Viren der Influenza und klassischen Geflügelpest. In: Zeitschrift für Naturforschung B. 10, 1955, S. 80–91 (online).
- ForschungsReport, 1/2006, des Senats der Bundesforschungsanstalten, S. 5.
- Dennis Normile: Are Wild Birds to Blame? In: Science, Band 310, Nr. 5747, 2005, S. 426, doi:10.1126/science.310.5747.426
- Dennis Normile: Wild Birds Only Partly to Blame in Spreading H5N1. In: Science., Band 312, Nr. 5779, 2006, S. 1451, doi:10.1126/science.312.5779.1451.
- Sievert Lorenzen: Evolution und Ausbreitung des Vogelgrippe-Virus H5N1 Asia sowie Aspekte der Biosicherheit In: Tierärztliche Umschau, Band 63, 2008, S. 333–339.
- Dennis J. Alexander: A review of avian influenza in different bird species. In: Veterinary Microbiology. Band 74, 2000, S. 3–13, Volltext (PDF)
- W. B. Becker: The isolation and classification of tern virus influenza virus A/Tern/South Africa/1961. Journal of Hygiene, Band 64, S. 309 (1966)
- Geflügelpest im Landkreis Cloppenburg weitet sich aus. Auf: aerztezeitung.de vom 15. Dezember 2008
- Sperrzone um Straußenfarm ist aufgehoben. Rückblick auf: suedkurier.de vom 15. Januar 2014
- Ilaria Capua et al.: The 1999–2000 avian influenza (H7N1) epidemic in Italy: veterinary and human health implications. In: Acta Tropica. Band 83, Nr. 1, 2002, S. 7–11, doi:10.1016/S0001-706X(02)00057-8
- Zu zahlreichen Verweisen siehe: Scott Krauss, Robert G. Webster: Predicting the Next Influenza Virus. In: Science, Band 337, Nr. 6095, 2012, S. 644, doi:10.1126/science.337.6095.644-a
- Avian Influenza A Virus Infections of Humans / Instances of Avian Influenza A Virus Infections of Humans. Auf: cdc.gov vom 23. Mai 2008
- Tommy Tsan-Yuk Lam: The genesis and source of the H7N9 influenza viruses causing human infections in China. In: Nature. Band 502, 2013, S. 241–244, doi:10.1038/nature12515
H7N7-Viren: Die neue Vogelgrippe hat einen potenziell gefährlichen Verwandten. Auf: zeit.de vom 21. August 2013 - H7N9 avian influenza human infections in China. Auf: who.int vom 1. April 2013
Süddeutsche Zeitung vom 2. April 2013: Neuer Vogelgrippe-Typ ruft WHO auf den Plan.
straitstimes.com: Man dies of H7N9 bird flu in China, third fatality from lesser-known strain. (Memento vom 4. April 2013 im Internet Archive) - ForschungsReport, 1/2006, des Senats der Bundesforschungsanstalten, S. 7
- Nazeer Hussain Kalhoro: Generation and Evaluation of a DIVA (Differentiating Infected from Vaccinated Animals) Vector Vaccines for Protection of Poultry against Avian Influenza virus infections: Deutscher Titel: Herstellung und Evaluierung von DIVA (Unterscheidung von infizierten und vakzinierten Tieren) Vektor-Impfstoffen zum Schutz des Geflügels vor Infektionen mit aviären Influenzaviren, Hannover, Tierärztliche Hochschule, Dissertation, 2008. Volltext (PDF, englischsprachig; 18,9 MB) und Zusammenfassung (HTML, Abstract, deutschsprachig und englischsprachig)
- Verordnung über besondere Schutzmaßregeln in kleinen Geflügelhaltungen
- Martin Enserink: Transgenic Chickens Could Thwart Bird Flu, Curb Pandemic Risk. In: Science. Band 331, Nr. 6014, 2011, S. 132–133, doi:10.1126/science.331.6014.132-a
Jon Lyall et al.: Suppression of Avian Influenza Transmission in Genetically Modified Chickens. In: Science. Band 331, Nr. 6014, 2011. S. 223–226, doi:10.1126/science.1198020 - Hühner bald gripperesistent? In: schweizerbauer.ch. 29. Januar 2019, abgerufen am 30. Januar 2019.