g-Strophanthin
g-Strophanthin (von griech. στροφή, „Strophe“, hier im Sinne von „Wendung, Schlängelung“ bezogen auf die Strophanthin enthaltenden Schlinggewächse, und ἄνϑος, „Anthos“ = Blüte) auch Ouabain oder kurz Strophanthin, ist ein Cardenolid-Glykosid, welches als Herzglykosid früher zur Behandlung von Herzkrankheiten eingesetzt wurde.[6][7] Das Aglykon ist g-Strophanthidin (Ouabagenin). Strophanthin wirkt auf Rezeptoren am Enzym Na+/K+-ATPase (Natrium-Kalium-Pumpe) und kann in höheren Dosen tödlich wirken. In Teilen Afrikas wurde es deshalb als Pfeilgift eingesetzt.[8]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
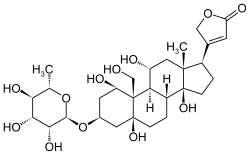 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | g-Strophanthin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C29H44O12 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose, glänzende Kristalle mit bitterem Geschmack[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
C01AC01 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus |
Hemmung bzw. Aktivierung der Na+/K+-ATPase | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 584,65 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
10 g·l−1 in Wasser bei 20 °C[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen und Nomenklatur

g-Strophanthin ist eines der Strophanthine, die im Samen diverser afrikanischer Schlingpflanzen der Gattung Strophanthus aus der Familie der Hundsgiftgewächse vorkommen. Der Buchstabe g steht für das Vorkommen in der Art Strophanthus gratus. Auch in der Pflanze Acokanthera (Acokanthera oblongifolia, Acokanthera ouabaio und Acokanthera schimperi), die bisweilen bei uns auch als Topfpflanze zu finden ist, ist das g-Strophanthin zu finden. Die Bezeichnung Ouabain leitet sich vom afrikanischen Ouabaio-Baum (der wissenschaftliche Name Acokanthera ouabaio ist jedoch ein veraltetes Synonym; heute heißt die Art Acokanthera oppositifolia), dessen Samen gleichfalls g-Strophanthin enthält. Ouabaio ist die englische Schreibung des ostafrikanischen Wortes Wabayo.
g-Strophanthin zählt zusammen mit dem in Strophanthus kombe vorkommenden k-Strophanthin zu den herzwirksamen Glycosiden (vgl. Herzglykoside). Die beiden Substanzen sind von den aus dem Fingerhut (Digitalis) stammenden Digitalisglykosiden zu unterscheiden. Das Aglykon des k-Strophanthins, das ebenfalls sehr giftige k-Strophanthidin, ist in dem auch im europäischen Raum heimischen Sommer-Adonisröschen (Adonis aestivalis) enthalten.
Strophanthin wurde früher zu den endogenen Glykosiden gezählt, die als Hormone in Säugetieren fungieren; der Mensch produziere Strophanthin in der Nebennierenrinde.[9] Inzwischen existieren Hinweise, dass es nicht endogen vorkommt.[10][11] Bei körperlicher Anstrengung sollte die Synthese des endogenen Strophanthins angestiegen sein, was die Verengung von Blutgefäßen (Vasokonstriktion) auslösen sollte und so den arteriellen Blutdruck steigen lassen würde.[12] Bei Säugetieren mit Ausnahme des Menschen wird Strophanthin in der Milz gespeichert.
Wirkungen
Höhere Konzentrationen von Strophanthin, die im Labor auf einfache Weise und klinisch nur durch hohe Dosierungen intravenös verabreichten g-Strophanthins zu erreichen sind, hemmen die in der Zellmembran lokalisierte Natrium-Kalium-Pumpe. Die Natrium-Kalium-Pumpe (Natrium-Kalium-ATPase), die besonders zahlreich in Nerven- und Herzmuskelzellen vorkommt, regelt die Elektrolytkonzentration, indem sie Natriumionen aus der Zelle hinaus pumpt und Kaliumionen hinein. Diese Hemmung wird als die klassische Wirkung der Herzglykoside angesehen, die über den erhöhten zellulären Gehalt an Natrium und somit auch Calcium (via Natrium-Calcium-Austauscher) zu einer Steigerung der Kontraktionskraft der Herzmuskelzelle führt (positiv inotroper Effekt).
In geringen, physiologischen Konzentrationen, wie sie als Hormon, nach oraler Gabe sowie auch nach langsamer intravenöser Injektion in niedriger Dosierung gemessen werden, wirken Strophanthine hingegen stimulierend auf die Natrium-Kalium-Pumpe, was zur Senkung des zellulären Natrium- und Calciumgehalts führt.[13][14]
Im Tierversuch konnte gezeigt werden, dass g-Strophanthin aufgrund der gegensätzlichen zellulären Wirkung die Giftwirkung von Digitalis vermindert.[15]
Geschichte
In westlichen Teilen Afrikas wurde ein Extrakt aus dem Strophanthus-Samen traditionell als Pfeilgift unter anderem zur Elefantenjagd verwendet.[8][16]
Nachdem der Botaniker John Kirk während der Livingstone-Expedition 1859 die stark herzwirksame Wirkung von versehentlich eingenommenen pulverisierten Strophanthus kombé-Samen entdeckt und der schottische Pharmakologe und Arzt Thomas Richard Fraser den wirksamen Bestandteil 1862 als k-Strophanthin isoliert hatte, wurde das g-Strophanthin von Arnaud, einem französischen Chemiker, im Jahr 1888 aus Strophanthus gratus und dem Ouabaio-Baum isoliert.
Ab 1865 waren alkoholische Lösungen von Strophanthus kombé-Samen als Gesamtextrakt in Gebrauch, ab 1885 recht häufig in ganz Europa. Unsichere Konzentrationsverhältnisse und die abführend wirkenden Begleitstoffe machten die Therapie jedoch schwierig, auch wenn sie von vielen Klinikern angewendet wurde. Ab 1904 stand auch eine standardisierte g-Strophanthin-Lösung zur Verfügung.
Nach privaten Tierversuchen in Heidelberg um das Jahr 1900 erprobte der badische Arzt Albert Fraenkel im Jahre 1905 intravenöses k-Strophanthin bei Herzkranken in der Straßburger Universitätsklinik unter der Leitung von Ludolf von Krehl. Der Erfolg[17] erregte Aufsehen, und bereits ein Jahr später war die Therapie weit verbreitet. Das Präparat war als Kombetin von der Firma C. F. Boehringer & Soehne im Handel. 1910 schrieben Rudolf Gottlieb und der Pharmakologe Hans Horst Meyer in der ersten Auflage ihres Pharmakologie-Lehrbuchs, die intravenöse Einverleibung habe sich „seit der Empfehlung ... durch Fraenkel und Schwartz ... als ein wichtiger Fortschritt der Therapie erwiesen“.[18] Ähnliches berichtet die 9. Auflage 1936.[19]
Anwendungsgebiete waren alle Herzerkrankungen wie Herzinsuffizienz, Rhythmus-Anomalien, akute Myokardschäden durch z. B. Grippe und Diphtherie, Digitalis-Intoxikationen, Angina Pectoris, Herzinfarkt und Bluthochdruck.[20][21][22][23]
Während der nationalsozialistischen Diktatur wurde Strophanthin vereinzelt in Konzentrationslagern zur Ermordung von Häftlingen eingesetzt, so z. B. bei Paul Schneider.[24]
Nach dem Zweiten Weltkrieg standen auch orale Digitalis-Präparate zur Verfügung, sodass das für Arzt und Patient beschwerliche Spritzen von Strophanthin seltener angewendet wurde. Nach 1947 entwickelte Boehringer Mannheim in Kooperation mit dem Stuttgarter Internisten Berthold Kern ein orales Präparat, das zu 90 % aus g- und zu 10 % aus k-Strophanthin bestand, das Strophoral, in Tabletten- und Tropfenform. Im Laufe der Zeit entstanden eine Reihe weitere Präparate, z. B. Strophinos-Tropfen, Purostrophan-Tropfen, Strodival-Kapseln; letztere waren seit 1984 alleinig am Markt bis 2012.
Heutige Bedeutung
Intravenös zugeführtes Strophanthin wurde noch bis 1992 bei akuter Herzinsuffizienz vom Lehrbuch empfohlen,[25] da es das am schnellsten wirksame Herzglykosid ist.[26] Heute plädieren die internationalen Leitlinien auch hinsichtlich der Behandlung der chronischen Herzinsuffizienz generell erst an zweiter Stelle für Herzglykoside, dabei jedoch meist für die Anwendung von Digoxin.[27]
g-Strophanthin verbessert ähnlich wie Nitroglycerin[28] die Vorlast des Herzens und die Sauerstoffmangeltoleranz[29] bei Patienten mit Koronarinsuffizienz. Die Gabe von Strophantin hat dabei dennoch keine Bedeutung mehr, da die Pharmakokinetik sowohl bei oraler als auch bei intravenöser Anwendung als unvorhersehbar gilt.[30]
g-Strophanthin hat zwar eine mäßig positiv inotrope (kraftsteigernde) Wirkung, die zugeschriebenen positiven Effekte bei der Vorbeugung und Akutbehandlung der Angina pectoris und des Herzinfarktes wurden jedoch nur im Rahmen älterer Studien aus den 1950er bis 1980er Jahren belegt,[31] die mehrheitlich nicht den heutigen Qualitätsanforderungen an klinische Studien entsprachen.[32]
Weder in den Leitlinien zur Behandlung des akuten Koronarsyndroms[6] noch der chronischen koronaren Herzkrankheit[7] spielt g-Strophanthin daher heute eine Rolle.
Weblinks
- Y. Shah: Strophanthin - ein besonderes Herzglykosid. (PDF) In: Zeitschrift für Komplementärmedizin. 2, 2011, S. 48–51.
Literatur
- Hauke Fürstenwerth: Strophanthin – die wahre Geschichte, Books on Demand, 2016, ISBN 9783739213521
- Eberhard J. Wormer: Strophanthin. Comeback eines Herzmittels. Kopp, Rottenburg 2015, ISBN 9783864452291
Einzelnachweise
- Hermann Ammon (Hrsg.): Hunnius pharmazeutisches Wörterbuch. 8. Auflage, de Gruyter, Berlin 2004, ISBN 3-11-015792-6.
- Eintrag zu Ouabain in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Eintrag zu 3-(6-deoxy-α-L-mannopyranosyloxy)-1,5,11a,14,19-pentahydroxycard-20(22)-enolide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu CAS-Nr. 630-60-4 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Serva: Sicherheitsdatenblatt gemäß 1907/2006/EG, Artikel 31 vom 19. Dezember 2011. (PDF; 133 kB).
- Van de Werf F et al.: Management of acute myocardial infarction in patients presenting with persistent ST-segment elevation: the Task Force on the Management of ST-Segment Elevation Acute Myocardial Infarction of the European Society of Cardiology. Eur Heart J. 2008 Dec;29(23):2909-45. PMID 19004841.
- Nationale Versorgungsleitlinie der Bundesärztekammer, Chronische KHK, Version 1.8, April 2008. Online als PDF.
- Pfeilgift, in Deutsches Kolonial-Lexikon (1920), Band III, S. 49
- W. Schoner, G. Scheiner-Bobis: Endogenous and exogenous cardiac glycosides and their mechanisms of action. In: American Journal of Cardiovascular Drugs. Band 7, Nummer 3, 2007, S. 173–189, PMID 17610345. (Review).
- S. Baecher, M. Kroiss, M. Fassnacht, M. Vogeser: No endogenous ouabain is detectable in human plasma by ultra-sensitive UPLC-MS/MS. In: Clinica Chimica Acta. Band 431, April 2014, S. 87–92, doi:10.1016/j.cca.2014.01.038. PMID 24508998.
- L. K. Lewis, T. G. Yandle, P. J. Hilton, B. P. Jensen, E. J. Begg, M. G. Nicholls: Endogenous ouabain is not ouabain. In: Hypertension. Band 64, Nummer 4, Oktober 2014, S. 680–683, doi:10.1161/HYPERTENSIONAHA.114.03919. PMID 25001271.
- W. Schoner, G. Scheiner-Bobis: Role of endogenous cardiotonic steroids in sodium homeostasis. In: Nephrology Dialysis Transplantation. 2008, 23: S. 2723–2729.
- Gao J, Wymore RS, Wang Y, et al.: Isoform-specific stimulation of cardiac Na/K pumps by nanomolar concentrations of glycosides. In: J. Gen. Physiol.. 119, Nr. 4, April 2002, S. 297–312. PMID 11929882. PMC 2238186 (freier Volltext).
- Balzan S, D'Urso G, Nicolini G, Forini F, Pellegrino M, Montali U: Erythrocyte sodium pump stimulation by ouabain and an endogenous ouabain-like factor. In: Cell Biochem. Funct.. 25, Nr. 3, 2007, S. 297–303. doi:10.1002/cbf.1387. PMID 17191274.
- Nesher M, Shpolansky U, Viola N, et al.: Ouabain attenuates cardiotoxicity induced by other cardiac steroids. In: Br. J. Pharmacol.. 160, Nr. 2, Mai 2010, S. 346–54. doi:10.1111/j.1476-5381.2010.00701.x. PMID 20423344.
- Das giftige Geheimnis der Mähnenratte.
- Albert Fraenkel und G. Schwartz: Abhandlungen zur Digitalistherapie. I. Über intravenöse Strophanthininjektionen bei Herzkranken. In: Archiv für experimentelle Pathologie und Pharmakologie. 57, 1907, S. 79–122. doi:10.1007/BF01841302.
- Hans H. Meyer und R. Gottlieb: Die experimentelle Pharmakologie als Grundlage der Arzneibehandlung, S. 259–260. Urban & Schwarzenberg, Berlin und Wien 1910.
- Hans H. Meyer und Ernst P.Pick: Die experimentelle Pharmakologie als Grundlage der Arzneibehandlung. Neunte Auflage, S. 376. Urban & Schwarzenberg, Berlin und Wien 1936.
- Ernst Edens: Digitalisfibel für den Arzt, S. 21, Verlag Julius Springer, Berlin 1941.
- Ernst Edens: Münch Med Wschr 1934, Nr. 37, S. 1424–1427.
- Heinz Zimmermann: Die klinische Strophanthin-Lehre von Edens im Lichte neuer Forschungsergebnisse. Teil I: Medizinische Klinik 1951, 46: 1028-1031 – Teil II: Med Klin 1951, 46: 1049-1052.
- Fritz Meyer (Uni-Klinik Köln): Normale oder unterschwellige Strophanthindosierung. Klin Wschr 1936, 15: 1238-1241.
- Walter Poller: Arztschreiber in Buchenwald, Offenbach a. M.: Verlag Das Segel, 1960; (zitiert aus/nach: Prediger in der Hölle, Gedenkheft zur 25. Wiederkehr des Todestages von Paul Schneider, Verlag Kirche und Mann, Gütersloh).
- K. Luckhaupt-Koch: Besonderheiten der Intensivbehandlung, in W. Dick (Hrsgb.), unter Mitwirkung von H. P. Schuster: Notfall- und Intensivmedizin, De Gruyter Lehrbuch, Berlin – N.Y., 1992, S. 436–450, dort S. 437.
- Lüllmann H & van Zwieten PA: The kinetic behaviour of cardiac glycosides in vivo, measured by isotope techniques. In: Journal of Pharmacy and Pharmacology. 21: 1-8, 1969, S. 2.
- Leitlinien zur Therapie der chronischen Herzinsuffizienz der Deutschen Gesellschaft für Kardiologie (PDF, 391 kB).
- Belz GG, Matthews J, Sauer U, Stern H, Schneider B: Pharmacodynamic effects of ouabain following single sublingual and intravenous doses in normal subjects. In: Eur J Clin Pharmacol. 26, Nr. 3, 1984, S. 287–92. PMID 6428911.
- Sharma B, Majid PA, Meeran MK, Whitaker W, Taylor SH: Clinical, electrocardiographic, and haemodynamic effects of digitalis (ouabain) in angina pectoris. In: British Heart Journal. 34, Nr. 6, Juni 1972, S. 631–7. PMID 4402698. PMC 458511 (freier Volltext).
- U. C. Hoppe, E. Erdmann. Leitlinien zur Therapie der chronischen Herzinsuffizienz. Mitt Österr Ges Kardiol 1999; 2 (2): 9–16.
- Fürstenwerth H: Ouabain – the insulin of the heart. In: Int. J. Clin. Pract.. 64, Nr. 12, November 2010, S. 1591–4. doi:10.1111/j.1742-1241.2010.02395.x. PMID 20946265.
- J. Wipplinger: Strophanthin: Das verschwundene Herzmedikament, medizin-transparent.at, 6. Februar 2015.