Ethenon
Ethenon oder auch Keten (Betonung auf der zweiten Silbe: Keten) ist die einfachste chemische Verbindung aus der Gruppe der Ketene und kann als inneres Anhydrid der Essigsäure aufgefasst werden.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemeines | ||||||||||||||||
| Name | Ethenon | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C2H2O | |||||||||||||||
| Kurzbeschreibung |
hochentzündliches, farbloses Gas mit stechendem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 42,04 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte |
1,93 kg·m−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
−56 °C[1] | |||||||||||||||
| Löslichkeit |
hydrolysiert in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 0,5 ml·m−3 bzw. 0,9 mg·m−3[3] | |||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−47,5 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
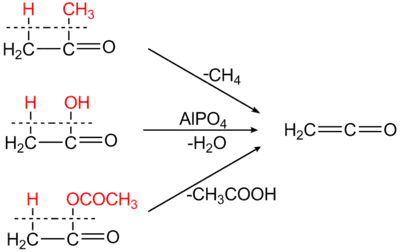
Keten entsteht durch Dehydratisierung von Essigsäure oder bei der Pyrolyse von Aceton. So wird beim Leiten von Acetondämpfen durch erhitzte Rohre oder elektrisch beheizte Metalldrähte bei 500–600 °C in Gegenwart von wenig Schwefelkohlenstoff Ethenon neben Methan in Ausbeuten bis 95 % d.Th. gebildet.[5][6] Die Ketonpyrolyse ist in der industriellen Chemie inzwischen von der Dehydratisierung von Essigsäure (Schmidlin-Bergman[7]-Wilsmore-Reaktion) weitgehend abgelöst worden.
 Herstellung von Keten
Herstellung von Keten
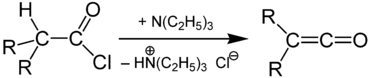
Im Labor kann Keten durch die Umsetzung von Acetylchlorid mit einem tertiären Amin dargestellt werden.
Ethenon wurde etwa gleichzeitig von Hermann Staudinger[8] – durch Reaktion von Bromacetylbromid mit metallischem Zink – und Norman Thomas Mortimer Wilsmore[9] – durch thermische Zersetzung von Essigsäureanhydrid – gefunden.
Eigenschaften
Ethenon ist chemisch instabil. Das Gas ist nur bei tiefen Temperaturen (−80 °C) einigermaßen beständig. Es muss daher für jede Verwendung stets neu hergestellt und gleich weiterverarbeitet werden, da sonst eine Dimerisierung zu Diketen erfolgt bzw. eine Reaktion zu schwer handhabbaren Polymeren. Der Polymeranteil bei der Herstellung von Diketen wird daher auch z. B. durch Zugabe von Schwefeldioxid zum Ketengas oder den Reaktionsmedium verringert.[10] Wegen seiner kumulierten Doppelbindungen ist Ethenon sehr reaktiv und addiert H-azide Verbindungen nucleophil zu den entsprechenden Essigsäurederivaten; so hydrolysiert es z. B. mit Wasser zu Essigsäure oder reagiert mit prim. oder sek. Aminen zu den entsprechenden Acetamiden.
Keten ist hochgiftig; die Toxizität beträgt etwa das Achtfache von Phosgen.[11]
Verwendung
Ethenon dient zur Herstellung von Essigsäureanhydrid aus Essigsäure. Allgemein es wird zur Acetylierung von chemischen Verbindungen verwendet.[11]
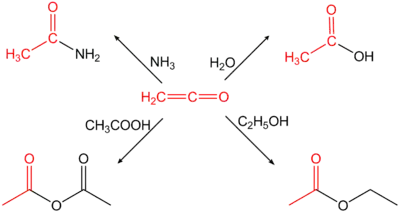 Darstellung von Acetamid, Ethylacetat, Essigsäure und Essigsäureanhydrid
Darstellung von Acetamid, Ethylacetat, Essigsäure und Essigsäureanhydrid
 Mechanismus der Umsetzung von Keten mit einem Protonendonator H–A
Mechanismus der Umsetzung von Keten mit einem Protonendonator H–A
Ethenon reagiert mit Formaldehyd in Gegenwart von Lewis-Säuren wie AlCl3, ZnCl2 oder BF3 als Katalysatoren zu β-Propiolacton.[12] Die technisch bedeutendste Verwendung von Ethenon ist die Synthese von Sorbinsäure durch Reaktion von Crotonaldehyd (2-Butenal) mit Keten in Toluol bei ca. 50 °C in Anwesenheit von Zinksalzen langkettiger Carbonsäuren. Dabei entsteht ein Polyester der 3-Hydroxy-4-hexensäure, der thermisch[13] oder hydrolytisch zu Sorbinsäure depolymerisiert wird.
Sicherheitshinweise
Ethenon neigt zur spontanen Polymerisation. Der Kontakt mit Wasserstoffperoxid führt zu explosivem Diacetylperoxid.[14] Die Dämpfe von Keten können mit Luft ein explosionsfähiges Gemisch bilden.
Einzelnachweise
- Eintrag zu Keten in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Februar 2017. (JavaScript erforderlich)
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von Ketene im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 27. Februar 2018.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 463-51-4 bzw. Ethenon), abgerufen am 2. November 2015.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-21.
- K.-H. Lautenschläger, W. Schröter, A. Wanninger, "Taschenbuch der Chemie", 20. Aufl. 2006, ISBN 978-3-8171-1761-1.
- C.D. Hurd: Ketene In: Organic Syntheses. 4, 1925, S. 39, doi:10.15227/orgsyn.004.0039; Coll. Vol. 1, 1941, S. 330 (PDF).
- J. Schmidlin, M. Bergman, Ber. dtsch. Chem. Ges., 43, 2821 (1910), DOI:10.1002/cber.19100430340.
- Tidwell, T. T. (2005), Ein Jahrhundert Ketene (1905–2005): die Entdeckung einer vielseitigen Klasse reaktiver Intermediate. Angewandte Chemie, 117: 5926–5933. doi:10.1002/ange.200500098 und H. Staudinger, H. W. Klever, Ber. dtsch. Chem. Ges., 41, 5943 (1908).
- N. T. M. Wilsmore, J. Chem. Soc., 91, 1938 (1907), DOI:10.1039/ct9079101938.
- Patent EP0377438: Veröffentlicht am 11. Juni 1990, Anmelder: Lonza AG, Erfinder: R. Bergamin et al..
- Eintrag zu Diketen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 16. Juni 2014.
- Hans-Jürgen Arpe, "Industrielle Organische Chemie", 6. Aufl., 2007, WILEY-VCH Verlag, Weinheim, ISBN 978-3-527-31540-6.
- Patent EP1295860: Veröffentlicht am 26. März, Anmelder: Nutrinova GmbH, Erfinder: D. Decker et al..
- L. Roth, U. Weller-Schäferbarthold: Gefährliche Chemische Reaktionen - Potentiell gefährliche chemische Reaktionen zu über 1750 Stoffen, Eintrag für Keten, CD-ROM Ausgabe 8/2021, ecomed Sicherheit Landsberg/Lech, ISBN 978-3-609-48040-4 .