Enamine
Enamine sind ungesättigte chemische Verbindungen, die durch Reaktion von Aldehyden oder Ketonen mit sekundären Aminen unter Abspaltung von Wasser (H2O) entstehen.[1] Bei primären Aminen oder Ammoniak als Edukten liegt das Tautomerengleichgewicht nicht auf der Seite des Enamines, sondern auf der Seite des Imines (Imin-Enamin-Tautomerie).
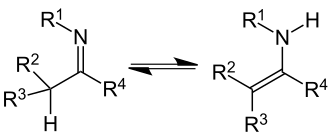
| Enamine |
|---|
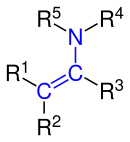 |
| Allgemeine Struktur der Enamine mit der blau markierten Enamin-Funktion. Die Reste R1, R2, R3 und R4 stellen dabei unabhängig voneinander einen aliphatischen, cyclischen oder aromatischen Rest oder auch ein Wasserstoff-Atom dar. Das einfachste Enamin ist Vinylamin (R1 bis R5 = Wasserstoff). |
Der Begriff „Enamin“ entsteht aus der Vorsilbe „en“ (als Kennzeichnung für das enthaltene Alken, ähnlich wie bei „enol“) und „amin“, welches dem Alken als funktionelle Gruppe angelagert ist.
Herstellung
Übersichtsreaktion
Die bequemste und am häufigsten genutzte Methode zur Herstellung von Enaminen ist die säurekatalysierte Kondensationsreaktion einer Carbonylverbindung mit einem sekundären Amin (z. B. Pyrrolidin, Piperidin oder Morpholin):
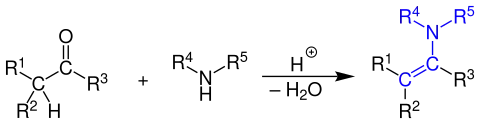
Damit die Reaktion gelingt, muss die verwendete Carbonylverbindung mindestens ein Wasserstoff-Atom an einem der α-Kohlenstoff-Atome besitzen.
Reaktionsmechanismus
Im ersten Schritt zur Bildung eines Enamins findet ein nukleophiler Angriff des sekundären Amins (2) auf den positiv polarisierten Kohlenstoff der Carbonylverbindung (1) statt, wodurch ein tetraedrisches, zwitterionisches Additionsprodukt (3) gebildet wird. Es erfolgt rasch eine Umprotonierung, wodurch ein Halbaminal (4) entsteht. Durch die zugegebene Säure findet im Gleichgewicht eine Protonierung der Hydroxygruppe statt, wodurch Wasser als gute Abgangsgruppe (5) entsteht. Nach Abspaltung eines Wasser-Moleküls wird intermediär ein resonanzstabilisiertes Iminium-Ion (6) gebildet. Eine abschließende Deprotonierung am (früheren) α-Kohlenstoff-Atom liefert schließlich das Enamin (7).
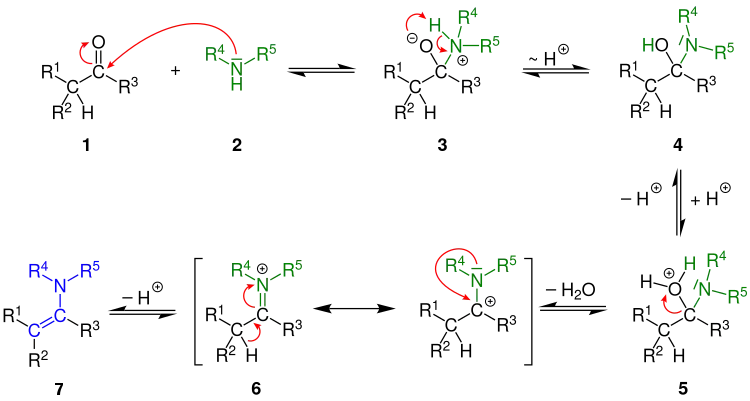
Bei all diesen Schritten handelt es sich um Gleichgewichtsreaktionen, da die Enamin-Bildung reversibel ist.
Verwendung
Enamine sind bei der Synthese von chemischen Verbindungen von Bedeutung, da die Ladungsaufspreizung in dem mesomeren System eine leichte Reaktion von Elektrophilen (z. B. von Säurechloriden und aktivierte Alkylierungsmitteln wie Allylhalogeniden und α-Halogencarbonsäureestern sowie elektronenarmen Alkenen) am zweiten Kohlenstoffatom ermöglicht.[2]
Beachte auch
- Enamin-Alkylierung und -Acylierung[3]
- Thorpe-Ziegler-Reaktion
- Stork-Enamin-Reaktion
- Enamin-Lacton-Umlagerung
- Michael-Addition (kann mit Enaminen ausgeführt werden)
- Nukleophile Addition
Einzelnachweise
- Eberhard Breitmaier, Günther Jung: Organische Chemie, 7. Auflage, Thieme Verlag, 2012, S. 325, ISBN 978-3-13-541507-9.
- Ludwig Gattermann und Heinrich Wieland: Die Praxis des organischen Chemikers, ISBN 3-11-006654-8.
- namensreaktionen.de: Enamin-Alkylierung und -Acylierung