Dichloressigsäure
Dichloressigsäure (kurz DCA, von englisch Dichloroacetic Acid) ist eine chlorierte Essigsäure, bei der zwei Wasserstoffatome der Methylgruppe durch zwei Chloratome substituiert sind. Die Salze werden als Dichloracetate bezeichnet.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
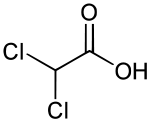 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Dichloressigsäure | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C2H2Cl2O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit stechendem Geruch[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 128,94 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||||||||
| Dichte |
1,57 g·cm−3 (20 °C)[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
194 °C[2] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| pKS-Wert |
1,29[3] | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Brechungsindex |
1,466[4] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||||||||
| ΔHf0 |
−496,3 kJ/mol[7] | |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Vorkommen
Dichloressigsäure kann in gechlortem Trinkwasser bei Kontakt mit organischer Materie entstehen.[8][9]
Gewinnung und Darstellung
Dichloressigsäure kann aus Trichloressigsäure oder bei der Reaktion von Essigsäure mit Chlor gewonnen werden, wobei allerdings ein Gemisch von Mono-, Di- und Trichloressigsäure entsteht, das nur schwer aufzutrennen ist. Ein direkter Zugang ergibt sich über die Umsetzung von Chloralhydrat und Kaliumcyanid oder Kaliumhexacyanidoferrat(II) in wässriger Lösung durch Kochen unter Rückfluss.[10]
Verwendung
Dichloressigsäure wird als Lösungsmittel sowie als Ausgangsstoff zur Synthese anderer Chemikalien (etwa Sulfonamide[11]) benutzt.
Arzneistoff
In klinischen Studien wird die Anwendung von Dichloracetat als Arzneistoff bei mehreren Erkrankungen geprüft. Bei der Laktatazidose hemmt es die Enzym-eigene Kinase des Enzymkomplexes Pyruvat-Dehydrogenase. Bei Morbus Crohn erwies es sich an Mäusen als heilsam durch Anregung der Darmregeneration und Steigerung der Mitochondrien-Funktion.[12]
Seit einer wissenschaftlichen Veröffentlichung im Januar 2007[13] ist ein Einsatz als Arzneistoff auch gegen spezielle Krebsformen Gegenstand von Untersuchungen.[14][15][16] Für eine kommerzielle Vermarktung liegen bisher keine ausreichenden Belege der klinischen Wirksamkeit und Sicherheit vor. Eine Studie musste 2006 wegen Nervenschädigungen abgebrochen werden.[17] Aufgrund fehlender Patentierbarkeit ist die Finanzierung klinischer Studien sehr schwierig,[18] da insofern kein finanzieller Anreiz für Pharmakonzerne besteht.
Sicherheitshinweise
Die IARC stufte Dichloressigsäure im Jahr 2014 als möglicherweise krebserzeugend ein.[19]
Siehe auch
Einzelnachweise
- Eintrag zu Dichloressigsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. Oktober 2014.
- Eintrag zu Dichloressigsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Lawrence H. Keith,Douglas B. Walters; The National Toxicology Program's Chemical Data Compendium; ISBN 978-0-87371-716-8
- Datenblatt Dichloroacetic acid bei Sigma-Aldrich, abgerufen am 21. Februar 2013 (PDF).
- Eintrag zu Dichloroacetic acid im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- AMA Archives of Industrial Hygiene and Occupational Medicine. Vol. 4, 1951. S. 119.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-21.
- Greenfacts: Dichloroacetic acid.
- WHO: Dichloroacetic Acid in Drinking-water (PDF-Datei; 183 kB).
- Ernst Albert Schmidt: Ausführliches Lehrbuch der pharmaceutischen Chemie. F. Vieweg und Sohn, 1901, S. 408 (eingeschränkte Vorschau in der Google-Buchsuche).
- International Agency for Research on Cancer: Dichloroacetic acid.
- Sevana Khaloian, Eva Rath, Dirk Haller et al: Mitochondrial impairment drives intestinal stem cell transition into dysfunctional Paneth cells predicting Crohn’s disease recurrence. Gut 2020;0:1–13, 28. Februar 2020, abgerufen am 15. April 2020 (englisch).
- Small molecule offers big hope against cancer (Memento vom 27. Februar 2007 im Internet Archive), University of Alberta Express News, 16. Januar 2007
- NZZ online: Krebszellen unter Zwangsbeatmung. 4. April 2007.
- Rosemary Cashman: Dichloroacetic Acid (DCA) for brain tumours. (PDF; 1,6 MB) BC Cancer Agency, abgerufen am 1. Februar 2012 (englisch).
- N. Zhang, A. F. Palmer: Development of a dichloroacetic acid-hemoglobin conjugate as a potential targeted anti-cancer therapeutic. In: Biotechnology and bioengineering. Band 108, Nummer 6, Juni 2011, S. 1413–1420, doi:10.1002/bit.23071. PMID 21328317.
- Franziska Badenschier: Experten warnen vor vermeintlichem Wundermittel. spiegel.de, 30. März 2007, abgerufen am 1. Februar 2012.
- FAZ Community Blogs: Altes Molekül als Krebsmedikament?
- IARC Monograph 106 - Dichloressigsäure, 2014.



