Burkitt-Lymphom
Das Burkitt-Lymphom (BL, englisch Burkitt’s lymphoma) ist ein malignes Lymphom und wird zu den B-Zell-Non-Hodgkin-Lymphomen gezählt. Es ist nach seinem Erstbeschreiber, dem britischen Chirurgen Denis Parsons Burkitt benannt.[1]
| Klassifikation nach ICD-10 | |
|---|---|
| C83.7 | Burkitt-Tumor ICD-O 9687/3 (Lymphom) ICD-O 9826/3 (Leukämie) |
| ICD-10 online (WHO-Version 2019) | |
Die Weltgesundheitsorganisation (WHO) unterscheidet drei verschiedene Typen:
- das endemische Burkitt-Lymphom, das sich vor allem im tropischen Afrika findet, wo es zu den häufigsten Tumorerkrankungen bei Kindern zählt,
- das sporadische Burkitt-Lymphom, das in gemäßigten Klimazonen auftritt, und
- das HIV-assoziierte Burkitt-Lymphom, das bei HIV-Infektion auftreten kann.
Das BL ist einer der am schnellsten wachsenden humanen Tumoren und hat entsprechend eine außerordentlich hohe Zellteilungsrate (der sogenannte Ki-67-Index ist größer 95 %, d. h. mehr als 95 % der Zellen befinden sich in Teilung). Gerade wegen des rasanten Wachstums ist der Tumor jedoch in der Regel sehr empfindlich gegenüber Chemotherapie und Strahlentherapie. Bei ausgeprägtem Knochenmarkbefall durch das BL (>20 % Zellanteil) spricht man auch von Burkitt-Leukämie oder „reifzelliger B-ALL“/„L3-ALL“. Dies ist ein seltenes Krankheitsbild (nur ca. 3–5 % aller akuten lymphatischen Leukämien, d. h. in ganz Deutschland weniger als 100 Fälle pro Jahr).
Klinisch kann das BL überall dort auftreten, wo sich Lymphozyten befinden. Bevorzugt tritt es in den Lymphknoten auf. Für das endemische BL sind eine Invasion der Mandibula oder Maxilla (Ober- und Unterkieferknochen) typisch. Beim sporadischen BL (in Europa und Nordamerika) findet man diese Manifestation eher selten. Stattdessen sind häufig die Lymphknoten im Bauchraum betroffen.
Stadieneinteilung
Die Stadieneinteilung in die Stadien I bis IV erfolgt nach dem System von Ann-Arbor. Für Kinder und Jugendliche erfolgt die Stadieneinteilung nach der St.-Jude’s-Modifikation der Ann-Arbor-Klassifikation.
| St. Jude’s Modifikation der Ann Arbor Klassifikation für Non-Hodgkin-Lymphome im Kindes- und Jugendalter | |
|---|---|
| Stadium | Definition |
| Stadium I | eine einzelne nodale oder extranodale Tumormanifestation ohne lokale
Ausbreitung
|
| Stadium II | mehrere nodale und/oder extranodale Manifestationen auf derselben Seite
des Zwerchfells mit oder ohne lokale Ausbreitung
|
| Stadium III | Lokalisationen auf beiden Seiten des Zwerchfells
|
| Stadium IV | Befall des Knochenmarks und/oder des Zentralnervensystems (Gehirn und Rückenmark) |
Als Befall des Knochenmarks wird ein Blastenanteil von mehr als 5 % und weniger als 25 % in der zytologischen Untersuchung des Knochenmarks (Knochenmarkausstrich) definiert. Wenn 25 % oder mehr Blasten im Knochenmark vorhanden sind, handelt es sich um eine Burkitt-Leukämie (L3-ALL). Als Befall des Zentralnervensystems wird jeder Nachweis von Blasten im Nervenwasser (Liquor) gewertet. Ein Befall des Zentralnervensystems ist auch dann gegeben, wenn jede Raumforderung im Zentralnervensystem bei gesichertem Burkitt-Lymphom an einer anderen Lokalisation wie Brustkorb, Unterkiefer und Abdomen nicht gesichert auf eine andere Ursache zurückgeführt werden kann.
Diagnostik
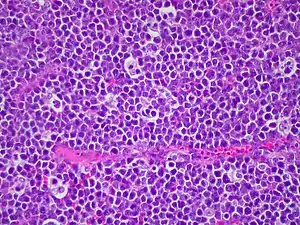
Bei Diagnosestellung eines BL muss zunächst ein komplettes Staging, d. h. eine Ausbreitungsdiagnostik erfolgen. d. h. es muss festgestellt werden, welches Stadium vorliegt, da die Therapie sich daran orientiert (je ausgebreiteter das Lymphom, desto intensiver und länger die Therapie). Die folgenden Untersuchungen sind notwendig:
- Knochenmarkuntersuchung
- Computertomographie (CT) oder Magnetresonanztomographie (MRT) von Hals, Thorax und Abdomen
- Blutuntersuchungen (Blutbild, LDH, Harnsäure, Kreatinin, …)
Der Lactatdehydrogenase (LDH) im Serum oder Plasma kommt bei den Burkitt-Lymphomen im Kindes- und Jugendalter besondere Bedeutung zu, da der LDH-Wert bei Diagnosestellung die Risikogruppe mitbestimmt (mehr als 500 U/L LDH im Serum oder Plasma entsprechen dabei einer höheren Risikogruppe). Die Mitbestimmung der LDH in der Risikogruppen-Zuteilung wird vor allem bei den Therapieoptimierungsstudien im deutschen Sprachraum und mittlerweile auch in Europa angewendet.
Therapie
Die Mortalität betroffener Patienten hat sich seit Einführung der Chemotherapie (Joseph H. Burchenal und andere in den 1960er Jahren) sehr deutlich verbessert, davor starben die Betroffenen rasch. Der Tumor ist außerordentlich chemo- und strahlensensibel. Die Aussichten auf komplette Heilung sind desto besser, je lokalisierter der Tumor ist.
Ist die Krankheit ausgedehnter oder betrifft das Knochenmark oder zentrale Nervensystem (ZNS), verschlechtert sie sich. Trotzdem sind die kurativen Aussichten heutzutage häufig über 50 %. Betroffene Erwachsene haben eine schlechtere Prognose als Kinder. Bewährt haben sich chemotherapeutisch das CHOP-Schema (wenn möglich im 14-tägigen Abstand) und insbesondere auch Therapieschemata mit hochdosiertem Methotrexat (MTX), wie sie z. B. im Rahmen der Deutschen Multizentrischen Therapiestudie der akuten lymphatischen Leukämie des Erwachsenen (GMALL) gängig sind. Außerdem enthalten alle neueren Schemata den rekombinanten monoklonalen Antikörper Rituximab. Eine ZNS-Prophylaxe/Therapie ist in den meisten Fällen indiziert, in diesem Fall verabreicht man Methotrexat intrathekal. Ein chirurgisches oder alleiniges strahlentherapeutisches Vorgehen ist generell nicht sinnvoll und ein Kunstfehler (davon ausgenommen sind natürlich diagnostische Eingriffe um Tumorgewebe zu gewinnen, z. B. Lymphknotenentnahme). Wegen des sehr schnell wachsenden Tumors besteht bei allen Patienten die Gefahr eines Tumorlyse-Syndroms, dem es vorzubeugen gilt.
Bei Kindern und Jugendlichen erfolgt die Therapie des Burkitt-Lymphoms nach Therapieoptimierungsstudien für hochmaligne (lymphoblastische) B-Zell-Non-Hodgkin-Lymphome. Diese umfassen eine stratifizierte (Stadien- und Risikofaktor-gesteuerte) Therapie. Diese besteht zumeist aus einer Kombinationschemotherapie. Wichtige Zytostatika sind hierbei Methotrexat (in hoher Dosis: mehr als 1000 mg/m² KOF pro Einzeldosis), Adriamycin (Doxorubicin), Cyclophosphamid oder Ifosfamid, Cytarabin, Dexamethason, Etoposid und Vincristin. Neben der systemischen Zytostatika-Gabe ist auch eine intrathekale Therapie (bei Befall) oder Prophylaxe durchzuführen: diese erfolgt zumeist als regelmäßige intrathekale Injektion einer Kombination der drei Zytostatika Methotrexat, Cytarabin und Prednison (sogenannte Triple-LP). Für therapierefraktäre Burkitt-Lymphome wird nach der vorbeschriebenen Standardchemotherapie zumeist eine myeloablative (knochenmarkeliminierende) Hochdosis-Chemotherapie mit nachfolgender autologer Stammzelltransplantation durchgeführt. Die Behandlung von Burkitt-Lymphomen mit Rituximab ist im Kindes- und Jugendalter gegenwärtig kein Standard. Die Strahlentherapie spielt infolge der guten bis sehr guten Behandelbarkeit der Burkitt-Lymphome mittels Kombinationschemotherapie im Kindes- und Jugendalter eine deutlich untergeordnete Rolle: In den Therapieoptimierungsstudien (Standard) im deutschsprachigen Raum wird die Strahlentherapie nur im Ausnahmefall eingesetzt.
Pathophysiologie, genetische Eigenschaften
Typisch für das Burkitt-Lymphom sind genetische Veränderungen, die das Myc-Gen auf Chromosom 8 betreffen. Allerdings finden sich diese selten auch bei anderen malignen Lymphomen, insbesondere beim diffus-großzelligen B-NHL, so dass sie nicht 100 % spezifisch für das BL sind. Zytogenetisch findet man in der größten Mehrheit der Fälle eine der folgenden Chromosomentranslokationen:
- t(8;14)(q24;q32) – in ca. 85 % der Fälle
- t(8,22)(q24;q11) – in ca. 10 % der Fälle.
- t(2;8)(p11;q24) – in ca. 5 % der Fälle
Allen 3 Translokationen ist gemeinsam, dass dabei das MYC-Gen in die Nähe von Immunglobulin (IG)-Genen gelangt, und zwar in den Bereich der Immunglobulin-Schwerkette auf Chromosom 14 oder der Leichtketten kappa auf Chromosom 2 oder lambda auf Chromosom 22. Die beiden letztgenannten Translokationen werden auch als variante Translokationen bezeichnet. Selten werden auch Chromosomentranslokationen von MYC in Nicht-IG-Genbereiche gefunden.[2]
Durch die Translokation kommt es zu einer Dysregulation des MYC-Gens, welches eine Steuerungsfunktion bei der Zellteilung wahrnimmt und eine Vielzahl anderer Gene beeinflusst. Die Expression des MYC-Gens wird im Falle einer Translokation nicht mehr von dessen normalen DNA-Kontrollsequenzen (Promotor, Inhibitoren) auf Chromosom 8, sondern von den DNA-Kontrollsequenzen der Immunglobulin-Leicht- bzw. Schwerketten gesteuert. Zusätzlich kann auch das MYC-Gen selbst geschädigt werden. Da die Leicht- und Schwerketten von Immunglobulinen in B-Zellen im Rahmen der Antikörperproduktion quasi ständig abgelesen und exprimiert werden, geschieht dies für das MYC-Gen und MYC-Protein ebenfalls. Damit wird die Steuerung der Zellteilung empfindlich gestört; es kommt durch die Überexpression von MYC-Protein zu einer deutlich gesteigerten bis (im Falle eines Burkitt-Lymphoms) ungehemmten Zellteilung aus einer einzelnen genetisch veränderten Zelle (maligne Transformation mit monoklonaler Proliferation), wobei die Dysregulation des MYC-Gens allein nicht ausreichend ist. Eine alleinige Überexpression von MYC würde neben der Zunahme der Proliferationsrate auch zu einer Zunahme von MYC-abhängigen Apoptose-Mechanismen führen (beispielsweise über das CD95 Antigen). Somit sind neben einer Dysregulation des MYC-Gens auch weitere genetische Veränderungen notwendig, um eine maligne Transformation zu einem Burkitt-Lymphom zu vollenden. Eine mögliche Ursache könnte das Auftreten einer Translokation von MYC zeitgleich mit dem sogenannten Immunglobulin-Gen Rearrangement in B-Zellen sein, wodurch die Apoptose-Induktion einer MYC- Überexpression umgangen wird.
Die geographisch unterschiedlichen Formen (endemisch vs. sporadisch) spiegeln sich auch in der Genetik wider: Die Bruchpunktlokalisation des c-myc Gens auf Chromosom 8 variiert nach der Lokalisation, sind aber nur mit Einschränkungen spezifisch für den Erkrankungstyp (endemisch vs. sporadisch).
Neben den genetischen Veränderungen am MYC-Gen sind in ca. 40 % der Burkitt-Lymphome auch Mutationen des Protein 53 (p53)-Gens beschrieben. Auch sind Mutationen des Retinoblastom (Rb)-Gens und dessen Produkten Protein 107 (p107) und Protein 130 (p130) identifiziert worden.
Ursächlich für die Entstehung der endemischen Form in Afrika sieht man eine stufenweise Karzinogenese (Krebsentwicklung), bei der verschiedene Faktoren für die einzelnen Schritte verantwortlich sind. Der erste Schritt besteht in der Infektion von B-Zellen durch EBV (Epstein-Barr-Virus), wodurch es zum polyklonalen Wachstum der B-Lymphozyten kommt. In vitro können normale B-Zellen durch Infektion mit EBV immortalisiert (unsterblich gemacht) werden. In den Gegenden in Äquatorial-Afrika, wo das Burkitt-Lymphom endemisch ist, sind etwa 80 % der Kinder mit EBV infiziert. Im zweiten Schritt kommt die Infektion mit Malaria hinzu. Diese herrscht dort auch endemisch und verursacht eine zusätzliche Immunsuppression. Dadurch wird die T-Zell-Population so gestört, dass sie die Proliferation von B-Zell-Klonen nicht mehr kontrollieren kann und sich damit der Anteil von B-Zellen erhöht, der für Translokationen anfällig ist. Der dritte Schritt besteht in einer Dysregulation des MYC-Onkogens durch die oben genannten Chromosomentranslokationen. Dieser Vorgang gleicht einem Dammbruch. Die Zellen wachsen nun unbegrenzt und sehr schnell, das BL entwickelt sich unaufhaltsam.
In Europa und Nordamerika sind EBV-Infektionen und Malaria im Kindesalter viel seltener. Die sporadischen BL zeigen in weniger als 20 % Assoziation mit EBV. Was allen BL gemeinsam ist, ist die Translokation von IG- und MYC-Genen.
Literatur
- P.A. Pizzo, D.G. Poplack: Principles and Practice of Pediatric Oncology. 4th Edition. Lippincott Williams & Wilkins Publishers, Philadelphia / Baltimore / New York, 2001, ISBN 0-7817-2658-1
Weblinks
- S1-Leitlinie Non-Hodgkin-Lymphome der Deutsche Krebsgesellschaft und Gesellschaft für Pädiatrische Onkologie und Hämatologie. In: AWMF online (Stand Januar 2009)
- Leitlinie Maligne Lymphome. (PDF) Deutsche Gesellschaft für Hämatologie und Onkologie (Stand Februar 2007)
Einzelnachweise
- D Burkitt: A sarcoma involving the jaws in African children. In: British Journal of Surgery. 46, Nr. 197, 1958, S. 218–23. doi:10.1002/bjs.18004619704. PMID 13628987.
- P Bertrand, C Bastard, C Maingonnat, F Jardin, C Maisonneuve, MN Courel, P Ruminy, JM Picquenot, H Tilly: Mapping of MYC breakpoints in 8q24 rearrangements involving non-immunoglobulin partners in B-cell lymphomas. In: Leukemia, 2007, 21(3), S. 515–523, PMID 17230227