Rituximab
Rituximab ist ein biotechnologisch hergestellter Antikörper, der als Arzneistoff in der Krebsimmuntherapie vorwiegend bei der Behandlung von malignen Lymphomen (Lymphdrüsenkrebs) sowie zur Behandlung verschiedener Autoimmunerkrankungen eingesetzt wird.
| Rituximab | ||
|---|---|---|
| ||
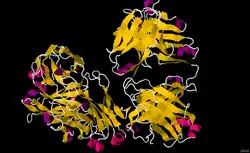
| Fab-Fragment von Rituximab mit einem Peptid-Epitop | ||
|
Vorhandene Strukturdaten: 2OSL | ||
| Masse/Länge Primärstruktur | 143,9 kDa | |
| Bezeichner | ||
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | L01XC02 | |
| DrugBank | DB00073 | |
| Wirkstoffklasse | Zytostatikum, monoklonaler Antikörper | |
Rituximab war einer der ersten Wirkstoffe einer neuen Generation von Medikamenten in der Krebsimmuntherapie und gilt daher als Vorreiter der gezielten Krebstherapie. Der variable Teil des Antikörpers richtet sich gegen das Zelloberflächenmolekül CD20, welches sich zum Beispiel bei einem Teil der Non-Hodgkin-Lymphome nachweisen lässt.
Entwicklung und Vermarktung
Ursprünglich wurde Rituximab von Lee Nadler, der auch das Antigen CD20 erstmals beschrieb, am Dana-Farber Cancer Institute entwickelt. Rituximab war der erste Antikörper, der zur Behandlung von Krebs zugelassen wurde (FDA 1997, EC 1998).
Seit Juli 2006 ist der monoklonale Antikörper in Europa in Kombination mit Methotrexat (MTX) zusätzlich für die Behandlung der rheumatoiden Arthritis zugelassen. Rituximab ist die erste Biomarker-basierte Therapie in der rheumatoiden Arthritis. Als praxisrelevante Biomarker gelten bisher vor allem Rheumafaktor und Antikörper gegen citrullinierte Proteine (ACPA). Im April 2011 hat die amerikanische Arzneimittelbehörde FDA Rituximab in Kombination mit Glucocorticoiden zur Behandlung der Granulomatose mit Polyangiitis (GPA) und Mikroskopischen Polyangiitis (MPA) zugelassen. Die erweiterte Zulassung für die EU wurde im April 2012 bei der europäischen Arzneimittelagentur EMA beantragt. Im Februar 2017 erteilte die Europäische Kommission die Zulassung für das Rituximab-Biosimilar Truxima.[1]
Anwendungsgebiete
Rituximab ist ein chimärer monoklonaler anti-CD20-Antikörper. Neben der Behandlung von Krebserkrankungen ist Rituximab ferner bei Autoimmunerkrankungen (rheumatoide Arthritis, Pemphigus vulgaris (Blasensucht), Granulomatose mit Polyangiitis und mikroskopische Polyangiitis) angezeigt. Die Wirksamkeit bei idiopathischer thrombozytopenischer Purpura (ITP)[2] oder Lupusnephritis[3] wird untersucht. Im off-label-use wird das Medikament zur Behandlung der Multiplen Sklerose,[4][5] und der Membranöse Glomerulonephritis verschrieben.[6]
Onkologie
Rituximab gehört heutzutage zur Standardtherapie in der Behandlung von sowohl hoch- als auch niedrigmalignen Non-Hodgkin-Lymphomen, meist in Kombination mit einer konventionellen Chemotherapie (beispielsweise CHOP bzw. R-CHOP oder in Kombination mit Bendamustin). Der Einsatz von Rituximab ist jedoch nur sinnvoll, wenn sich die Krebszellen durch das Oberflächenmolekül CD20 auszeichnen; daher muss vor der Behandlung mit Rituximab das Tumorgewebe entsprechend getestet werden.
Rituximab ist das wichtigste Medikament bei der Behandlung von transplantationsassoziierten Lymphomen (PTLD), die häufig CD20-positiv sind.
Rheumatoide Arthritis
Bei der rheumatoiden Arthritis wird Rituximab derzeit nach Versagen von Basismedikamenten und dem initialen TNF-α-Hemmer eingesetzt. Etwa 30 % der Patienten mit rheumatoider Arthritis sprechen nicht auf einen TNF-α-Hemmer an.[7] Bei unzureichendem Ansprechen und/oder Unverträglichkeit eines TNF-α-Hemmers wird eine Umstellung auf einen weiteren TNF-α-Hemmer oder auf Biologika mit anderem Wirkmechanismus wie z. B. Rituximab empfohlen.[8]
Mit zwei Infusionen innerhalb von 14 Tagen kann mit Rituximab eine signifikante Verbesserung der Symptome über einen Zeitraum von bis zu über einem Jahr erreicht werden. Weitere Behandlungen können den Therapieerfolg erhalten oder steigern. Empfohlen wird ein Therapieintervall von sechs Monaten. Dabei wird ein Wiederaufflammen der Krankheitsaktivität reduziert und das Ansprechen auf die Behandlung verbessert.[9]
Wirkungsmechanismus
Rituximab induziert eine selektive Zelldepletion (Entfernung körpereigener Substanzen) CD20-positiver B-Zell-Subpopulationen. Aus diesem Grund spricht man auch von der B-Zell-Therapie mit Rituximab. Über die folgenden drei Mechanismen wird eine B-Zell-Depletion bewirkt:[10]
- Apoptose
- komplementabhängige B-Zell-Lyse (CDC = complement-dependent cytotoxicity)
- Antikörper-abhängige zelluläre Zytotoxizität über Makrophagen, Granulozyten und natürliche Killerzellen (ADCC = antibody-dependent cell-mediated cytotoxicity)
Unerwünschte Wirkungen
Onkologie
Während der Behandlung mit Rituximab kommt es bei bis zu 50 % der Patienten zu teils starken Nebenwirkungen mit Fieber, Schüttelfrost, Atembeschwerden und Hautausschlägen. Die Beschwerden werden vermutlich durch den massiven Zerfall der Krebszellen verursacht, wodurch eine Vielzahl von Zytokinen freigesetzt wird. Man bezeichnet dieses Syndrom daher auch als „Cytokine release-Syndrome“. Diese Probleme treten vor allem bei Patienten mit hoher Tumorlast (viel Tumormasse) bei der ersten Behandlung auf, im weiteren Verlauf der Behandlung bessern sich die Nebenwirkungen meist.
Unter Behandlung mit Rituximab kam es zum Auftreten einer progressiven multifokalen Leukenzephalopathie (PML) bei einzelnen Patienten. Die PML ist eine schwerwiegende opportunistische Virusinfektion des Gehirns, die bei Patienten mit Immunschwäche durch das JC-Virus ausgelöst wird und oft tödlich verläuft. Die Mehrzahl der bekannten PML-Fälle nach Behandlung mit Rituximab traten bei Patienten mit Lymphknotenkrebs auf. Die Patienten, die nach Therapie mit Rituximab eine PML entwickelten, wurden in der Regel auch mit anderen immunsuppressiven Zytostatika behandelt. Daher kann der Kausalzusammenhang mit Rituximab im Einzelfall nicht als gesichert eingestuft werden. Viele dieser Patienten hatten auch weitere Risikofaktoren. Weitere PML-Fälle wurden bei Patienten mit Autoimmunerkrankungen bekannt.[11][12]
Rheumatoide Arthritis
Daten zur Langzeitsicherheit zeigen, dass Rituximab über einen Zeitraum von 10 Jahren gut vertragen wird. Patienten unter Rituximab haben kein erhöhtes Infektionsrisiko. Die häufigsten Nebenwirkungen treten überwiegend bei der ersten Verabreichung in Form von leichten bis moderaten Infusionsreaktionen innerhalb der ersten 24 Stunden nach Beginn der Infusion auf.[13]
Das „Cytokine release-Syndrome“ soll auch für das Auftreten von Todesfällen verantwortlich sein, die in seltenen Fällen unter der Behandlung der rheumatoiden Arthritis auftraten.[14] Patienten erhalten zur Vorbeugung eine Kombination von schützenden Medikamenten (Antihistaminika, Kortison, NSAR), so dass die Therapie insgesamt meist gut vertragen wird.
Allgemein
Als schwere Nebenwirkungen werden sehr selten (bei unter 0,01 % der Behandelten) Hautreaktionen wie eine toxische epidermale Nekrolyse und das Stevens-Johnson-Syndrom berichtet.[15] Da Fälle einer Hepatitis-B-Reaktivierung, einschließlich schwerer Verläufe mit tödlichem Ausgang berichtet wurden, empfiehlt sich ein Hepatitis-B-Virus-Screening vor Behandlungsbeginn.[10]
Kontraindikationen
Wie alle anderen Medikamente, darf auch Rituximab bei Überempfindlichkeit gegen den Wirkstoff nicht verwendet werden. Dabei müssen vor allem auch bekannte Überempfindlichkeiten gegen Maus-Proteine berücksichtigt werden.
Akute und schwere Infektionen müssen ausheilen oder zumindest unter Kontrolle sein, bevor Rituximab angewendet wird. Bei chronischen Infektionen und stark eingeschränkter Immunabwehr muss eine genaue Evaluierung von Nutzen und Risiko erfolgen. Dies gilt insbesondere auch für die Hepatitis-B-Patienten mit aktiver Hepatitis-B-Erkrankung, sie dürfen nicht mit Rituximab behandelt werden[16]
Bei schweren, nicht medikamentös kontrollierbarer Herzinsuffizienz oder anderer nicht zu kontrollierenden schweren Herzerkrankungen darf Rituximab nicht angewendet werden.
Aufgrund einer unzureichenden Datenlage wird empfohlen, während Schwangerschaft und Stillzeit auf Rituximab zu verzichten.[16] Studien zeigen jedoch, dass es wahrscheinlich doch zu keinen Schädigungen des Fetus kommt.[17]
Studien
Studiendaten aus der Onkologie
Die bislang größte Studie für Patienten mit aggressivem Non-Hodgkin-Lymphom (RICOVER-60) erzielte im Vergleich zu anderen Kombinationsbehandlungen die besten Ergebnisse. Der Studie nach sind nach 3 Jahren 78 % der Patienten mit aggressivem NHL nach der Kombinationstherapie CHOP-14 (6×) plus Rituximab (8×) am Leben. Aufgrund dieser Überlegenheit wurde die Studie frühzeitig beendet.[18]
Studiendaten zur rheumatoiden Arthritis
Die Zulassung für Rituximab beruht auf den Ergebnissen der REFLEX-Studie. In der Studie konnte die körperliche Funktionsfähigkeit der Patienten unter Rituximab verbessert werden.[19] Ebenfalls wurde das Fortschreiten der Gelenkzerstörung gehemmt.[20]
Bestimmte Biomarker im Blut wie Rheumafaktor oder ACPAs können auf die Erkrankung und die Schwere des Verlaufs hindeuten. In verschiedenen Studien wurde festgestellt, dass Rheumafaktor- oder ACPA-seropositive Patienten meist besonders gut auf Rituximab ansprechen.[21]
Seropositive Patienten, bei denen sich die Vortherapie mit einem TNF-α-Hemmer als unzureichend erweist und/oder sich eine Unverträglichkeit zeigt, sprechen meist besser auf eine Behandlung mit Rituximab an als auf eine Therapie mit einem weiteren TNF-α-Hemmer.[22]
Studiendaten zum chronischen Erschöpfungssyndrom
Eine Studie mit 30 Teilnehmern zeigte gute Erfolge bei der Behandlung des Chronischen Erschöpfungssyndroms bei 67 % der Erkrankten, aber bei Einzelnen traten unerwartet schwere Nebenwirkungen auf, die deren Zustand erheblich verschlechterten.[23] Eine nachfolgende detailliertere Studie konnte keinen Effekt von Rituximab auf das chronische Erschöpfungssyndrom feststellen.[24]
Weitere Studien zu Rituximab
Die Zulassung für die Granulomatose mit Polyangiitis und die Mikroskopische Polyangiitis stützt sich auf die positiven Ergebnisse der US-amerikanischen Studie RAVE.[25]
Handelsnamen
Roche/Genentech: MabThera (EU), Rituxan (USA)
Biosimilars
Rixathon (EU), Truxima (EU, USA)
Siehe auch
- Ibritumomab-Tiuxetan
- Nomenklatur der monoklonalen Antikörper: Konvention zur Benennung von monoklonalen Antikörpern
Literatur
- P. McLaughlin et al.: Rituximab chimeric anti-CD20 monoclonal antibody therapy for relapsed indolent lymphoma: half of patients respond to a four-dose treatment program. In: J. Clin. Oncol., 1998, Band 16, S. 2825–2833. PMID 9704735
- JA Singh, R Christensen, GA Wells et al.: Biologics for rheumatoid arthritis: an overview of Cochrane reviews. In: Cochrane Database Syst Rev. Nr. 4, 2009, S. CD007848. doi:10.1002/14651858.CD007848.pub2. PMID 19821440.
Weblinks
- Video zu Rituximab bei Membranöse Glomerulonephritis
- Artikel über Rituximab bei rheumatoider Arthritis
- Deutsche Gesellschaft für Rheumatologie e. V. – Leitlinien in der Rheumatologie
- Produktinformation zu MabThera auf der Website der Europäischen Arzneimittelagentur
- EMA Produktinformation: MabThera (PDF; 1,4 MB)
Einzelnachweise
- gelbe-liste.de
- P. Braendstrup et al.: Rituximab chimeric anti-CD20 monoclonal antibody treatment for adult refractory idiopathic thrombocytopenic purpura. In: Am. J. Hematol., 2005, Band 78, S. 275–280. PMID 15795920
- Camous L. et al.: Complete remission of lupus nephritis with rituximab and steroids for induction and rituximab alone for maintenance therapy. In: Am J Kidney Dis., 2008;52, S. 346–352 PMID 18572292
- arznei-news.de
- KKNMS Qualitätshandbuch-MS-NMOSD 2018 webfrei.pdf. (PDF) Abgerufen am 20. September 2020.
- H. Pavenstädt Die membranöse Glomerulonephritis abgerufen am 16. Februar 2021
- A. Georgi et al.: Therapiemöglichkeiten nach Nichtansprechen von TNF-Blockern bei rheumatoider Arthritis. In: J Miner Stoffwechs, 2010; 17, S. 15–20.
- JS Smolen et al.: EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs. In: Ann Rheum Dis, 2010, 69, S. 964–975.
- P Emery et al.: Retreatment with rituximab based on a treatment-to-target approach provides better disease control than treatment as needed in patients with rheumatoid arthritis: a retrospective pooled analysis. In: Rheumatology, 2011, doi:10.1093/rheumatology/ker253.
- Fachinformation MabThera® 100 mg / 500 mg, Stand: Juni 2013
- Information for Healthcare Professionals. Rituximab (marketed as Rituxan) Information. US Food and Drug Administration; abgerufen am 17. September 2008.
- Progressive multifokale Leukenzephalopathie nach Rituximab (Aus der UAW-Datenbank). Arzneimittelkommission der deutschen Ärzteschaft. Abgerufen am 7. November 2008.
- RF van Vollenhoven et al.: Long-term safety of Rituximab: 10-year follow-up in the rheumatoid arthritis global clinical trial programme. In: Ann Rheum Dis, 2012, 71 (Suppl 3), S. 195
- Rote-Hand-Brief von Roche am 5. August 2011. (PDF; 2,1 MB) Abgerufen am 8. August 2011.
- Rote Hand Brief von Roche im April 2013. (PDF; 2,1 MB) Abgerufen am 17. April 2013.
- Roche: Fachinformation MabThera i.v., Stand: März 2019.
- R.E. Fischer-Betz, M. Schneider: Biologika in Schwangerschaft und Stillzeit. In: Zeitschrift für Rheumatologie, 69, 2010, S. 780–787, doi:10.1007/s00393-010-0640-2.
- Kongressbericht, 2 European Congress on Hematologic Malignancies, 25. Februar 2006, Barcelona: Indolente und aggressive Lymphome. In: Onkologie, 2/2006, Haug-Verlag, S. 28–30, tellmed.ch; abgerufen am 15. Mai 2014
- SB Cohen et al.: Rituximab for rheumatoid arthritis refractory to anti-tumor necrosis factor therapy: Results of a multicenter, randomized, double-blind, placebo-controlled, phase III trial evaluating primary efficacy and safety at twenty-four weeks. In: Arth Rheum, 2006, 54, S. 2793–2806
- E Keystone et al.: Sustained inhibition of structural damage in patients with rheumatoid arthritis and an inadequate response to tumor necrosis factor inhibitors prior to rituximab treatment: 5-year data from the REFLEX study. In: Ann Rheum Dis, 2012, 71 (Suppl 3), S. 374
- H Tony et al.: Impact of rheumatoid factor and anti-CCP antibodies on EULAR response to long-term treatment with Rituximab in patients with rheumatoid arthritis after failing one TNFI (FIRST and ReFIRST). In: Ann Rheum Dis, 2012; 71 (Suppl 3), S. 500
- P Emery et al.: Relative effectiveness of Rituximab versus an alternative TNF inhibitor in patients with rheumatoid arthritis and an inadequate response to a single previous TNF inhibitor: results from SWITCH-RA, a global, comparative-effectiveness, observational study. EULAR 2012, Abstract 2203
- Øystein Fluge, Ove Bruland u. a.: Benefit from B-Lymphocyte Depletion Using the Anti-CD20 Antibody Rituximab in Chronic Fatigue Syndrome. A Double-Blind and Placebo-Controlled Study. In: PLoS ONE. 6, 2011, S. e26358, doi:10.1371/journal.pone.0026358.
- Øystein Fluge, Ingrid G. Rekeland, Katarina Lien, Hanne Thürmer, Petter C. Borchgrevink: B-Lymphocyte Depletion in Patients With Myalgic Encephalomyelitis/Chronic Fatigue Syndrome. In: Annals of Internal Medicine. 2. April 2019, doi:10.7326/M18-1451 (annals.org [abgerufen am 16. April 2019]).
- Stone et al.: Rituximab versus Cyclophosphamide for ANCA-associated vasculitis. In: N Engl J Med 2010; 363: 221–232