Burkholderia mallei
Burkholderia mallei ist ein gramnegatives, stäbchenförmiges, aerobes Bakterium. Es ist eine pathogene Burkholderia-Art, die bei Mensch und Tier die Erkrankung Rotz auslösen kann, die beim Menschen zu Lungenentzündung, Sepsis sowie Haut- und Schleimhautinfektionen führt.[1] Der lateinische Name dieser meldepflichtigen Krankheit, malleus, gab dem früher Malleomyces mallei genannten Erreger den Namen. Burkholderia mallei unterscheidet sich von allen anderen Vertretern der Gattung Burkholderia durch seinen echten Parasitismus, seine Unbeweglichkeit und sein langsames Wachstum in Kultur. B. mallei steht ebenso wie B. pseudomallei auf der Liste für potenzielle Biowaffen-Agentien.
| Burkholderia mallei | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
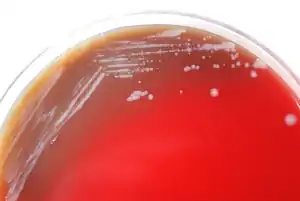
Kolonien von Burkholderia mallei auf Blutagar | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Burkholderia mallei | ||||||||||||
| (Zopf 1885) Yabuuchi et al. 1993 |
Taxonomie
Seit seiner Entdeckung wurde der Erreger in zahlreiche systematische Gruppen eingeordnet: Bacillus, Corynebacterium, Mycobacterium, Peifferella, Loefflerella, Malleomyces, Actinobacillus, Pseudomonas. Der Gattung Burkholderia wird das Bakterium erst seit Anfang der 1990er Jahre zugeordnet.
Morphologie
Aufgrund fehlender Begeißelung ist B. mallei als einziger Vertreter seiner Gattung nicht beweglich. Seine variable Form (Pleomorphismus) ist eine Mischung zwischen Stäbchen und Kugel. Das Bakterium misst 1,5–3 μm in der Länge und 0,5–1 μm in der Breite, die Enden sind stumpf oder abgerundet. Die Stäbchenform ist gerade oder leicht gekrümmt. In Probenmaterial und jungen Bakterienkulturen kommt der Erreger überwiegend in Stäbchenform vor, in älteren Kulturen dominiert ein pleomorphes Bild. B. mallei bildet keine Endosporen. Das Bakterium besitzt eine kapselähnliche Struktur (Exopolysaccharid-Kapsel), die nur im elektronenmikroskopischen Bild sichtbar wird.
Färbeverhalten und mikroskopischer Nachweis
Färbungen nach Gram sind möglich. Das Bakterium färbt sich oft nur schwach an oder zeigt gramlabiles Verhalten (gleichzeitiges Auftreten von grampositiven und -negativen Keimen im gleichen Präparat). Gespeichertes Poly-β-Hydroxybutyrat im Cytoplasma lässt das Bakterium granuliert und bipolar (Färbeunterschied zwischen Mitte und Enden des Bakteriums) erscheinen. Alternative Färbemethoden sind die Färbungen nach Wright, Giemsa oder mit Methylenblau. Die Kapsel ist lichtmikroskopisch nicht darstellbar.
Aus Gewebeschnitten ist der mikroskopische Nachweis von B. mallei schwierig, da der Erreger in kugeliger Form vorliegen kann. In Probenmaterial aus sekundär infizierten oder kontaminierten Bereichen kann der Rotzerreger mikroskopisch nicht von anderen Bakterien unterschieden werden.
Vorkommen im Organismus
Als obligat parasitär lebender Organismus kann sich der Erreger nur in infizierten Wirten vermehren. In klinischem Probenmaterial findet sich der Erreger oft außerhalb der Körperzellen (extrazellulär). Er kann gut aus frischen Hautläsionen isoliert werden, während er in älteren Läsionen (vor allem beim chronischen Rotz) nur spärlich vorkommt. Sputum, Speichel, Tränenflüssigkeit, Urin, Kot, Milch und Sperma können ebenfalls erregerhaltig sein. Aus Blut kann er nur während der Phase der disseminierten Infektion (Bakteriämie) nachgewiesen werden.
Wachstumsansprüche
Ein optimales Wachstum findet im neutralen pH-Bereich, bei mesophilen Temperaturen (37 °C) und unter Anwesenheit von Sauerstoff (Aerobier) statt. Bei gleichzeitiger Anwesenheit von Nitrat kann auch ein Wachstum unter anaeroben Verhältnissen erfolgen (fakultativer Anerobier). Bei Temperaturen unter 5 °C und über 42 °C erfolgt keine Vermehrung des Erregers mehr.
Kulturelle Anzucht
Der Erreger kann auf üblichen, bluthaltigen Nährböden angezüchtet werden. Das Wachstum erfolgt nur langsam (48–72 h Inkubation) und es besteht die Gefahr der Überwucherung durch schneller wachsende Begleitkeime. Die Zugabe von Glycerin beschleunigt das Wachstum, sodass eine Voranreicherung mit Glycerin sinnvoll sein kann. Auf Glycerin-haltigen Nährböden wächst der Keim als weicher, feuchter, zartcremefarbener Schleier, bei dem die größenvariablen Einzelkolonien zum Zerfließen neigen. Mit zunehmendem Alter der Kultur wird die Bakterienschicht dicker, bernsteinfarben und bekommt eine zähe, klebrige Konsistenz. Zur Anzucht eignen sich auch Glycerin-Kartoffel-Medium oder Glycerin-Bouillon. Auf einfachem Nähragar oder in Gelatinekulturen erfolgt nur spärliches Wachstum. Traditionell wurde B. mallei auf Kartoffelscheiben angezüchtet. Charakteristisch für die Bakterienkulturen ist ein aromatischer Geruch. Zur Unterdrückung unerwünschter Begleitflora werden klinische Proben mit Penicillin vorbehandelt oder es erfolgt ein Zusatz bakterienhemmender Stoffe (Proflavin, Kristallviolett) zu den Nährmedien. Für die Anzucht des Erregers wurde ein selektives Medium auf der Basis von Glycerin, Serum (Pferd oder Esel) und Tryptose entwickelt, dem Polymyxin E, Bacitracin und Actidion zugesetzt werden.
Biochemische Eigenschaften
B. mallei ist chemo-organotroph. Auf bluthaltigen Nährmedien wird keine Hämolyse beobachtet. Der Erreger besitzt die Enzyme Oxidase und Katalase. Indol-Test und Voges-Proskauer-Reaktion fallen negativ aus. Der Erreger kann Nitrat reduzieren. Photosynthetische Farbpigmente werden während des Wachstums nicht gebildet. Der Glukose-Abbau erfolgt überwiegend oxidativ. Obwohl die Gattung Burkholderia den Non-Fermentern (kein Abbau von Substrat durch Gärung) zugeordnet wird, gibt es Hinweise auf vereinzelte Fermentation von Glukose, Mannose, Arabinose und Fruktose. Die präzise Bestimmung der Spezies Burkholderia mallei auf biochemischer Basis ist bei der Verwendung handelsüblicher Testsysteme (Bunte Reihe) nicht möglich.
Widerstandsfähigkeit in der Umwelt
In der freien Umwelt ist B. mallei weder lebens- noch vermehrungsfähig, die Widerstandsfähigkeit (Tenazität) gegen äußere Einflüsse ist gering. Er ist empfindlich gegen Austrocknung, Hitze und Sonnenlicht. Direkte Sonneneinstrahlung tötet den Erreger innerhalb von 24 h.[2] In eingetrockneten Sekreten verliert er schon nach wenigen Tagen seine Infektiosität. An feuchten, dunklen Orten kann er jedoch bis zu 3 Monaten überleben, in Tränkewasser bleibt er 1 Monat lang kontagiös.
In Urin wird der Erreger innerhalb von 40 min, durch Magensaft innerhalb einer halben Stunde inaktiviert.[3] Fäulnis zerstört ihn erst nach 2–4 Wochen.[4]
Das Bakterium ist gegenüber zahlreichen Desinfektionsmitteln empfindlich, darunter Formaldehyd (2 %), Glutaraldehyd (2 %), Benzalkoniumchlorid, Iod, Bleichlorid, Kaliumpermanganat, Natriumhypochlorit (1 %) und Ethanol (70 %). Phenolhaltige Mittel zeigen dagegen wenig Wirksamkeit. Historisch bedeutsame Desinfektionsmittel waren Chlorkalk und Phenol.
Die Mikroorganismen werden durch Hitze inaktiviert. Ausreichend sind einmaliges Aufkochen, Temperaturen von 80 °C für 5 min oder 55 °C für 10 min.[4] UV-Bestrahlung tötet das Bakterium ebenfalls ab. Durch Kälte wird der Erreger nicht eliminiert.[2]
Die natürliche Wachstumsgrenze des Erregers liegt zwischen 20 °C und 45 °C.[5]
Antibiotikaresistenz
Antibiotika wie Ceftazidim, Imipenem, Aminoglykoside wie Streptomycin,[6] Amikacin, Tetracyclin, Doxycyclin und Sulfathiazol waren zumindest in vitro effektiv. Eine (achtwöchige) antibiotische Therapie des Rotz beim Menschen kann mit Imipenem und Doxycyclin erfolgen.
Weblinks
Bioinformatics Ressource Center: Pathema-Burkholderia
Quellen/Literatur
- Wolfgang Bisping & Gunter Amtsberg: Farbatlas zur Diagnose bakterieller Infektionserreger der Tiere., zweisprachig (dt./engl.), Paul Parey Scientific Publishers, Berlin und Hamburg (1988), ISBN 3-489-50716-9
- Martina B. Oberdorfer: Phänotypische Charakterisierung der Spezies des Genus Burkholderia mittels biochemischer Feintypisierung und in vitro-Resistenztestung. Diss.(med.vet.), Universität Gießen (2007)
- E. Lührs: ‚Rotz‘ in: Tierheilkunde und Tierzucht. Eine Enzyklopädie der praktischen Nutztierkunde. hrsg. Valentin Strang & David Wirth. Urban und Schwarzenberg Berlin, Wien (1930). Band 8, S. 641–662.
- Franz Friedberger & Eugen Fröhner: ‚Der Rotz.‘ in: Lehrbuch der speciellen Pathologie und Therapie der Haustiere. Ferdinand Enke, Stuttgart (1904), Band 2, S. 437–469.
- World Organisation for Animal Health: Glanders (Memento vom 7. April 2009 im Internet Archive) (PDF-Datei; 80 kB; engl., Archivversion)
- Center for Food Security & Public Health: Glanders (Memento vom 3. August 2015 im Internet Archive) (PDF-Datei; 118 kB; engl., Archivversion)
- Bridget Carr Gregory & David M. Waag: Glanders (Memento vom 12. Juni 2009 im Internet Archive) in: Medical aspects of biological warfare. Borden Institute (2007)
Einzelnachweise
- Marianne Abele-Horn: Antimikrobielle Therapie. Entscheidungshilfen zur Behandlung und Prophylaxe von Infektionskrankheiten. Unter Mitarbeit von Werner Heinz, Hartwig Klinker, Johann Schurz und August Stich, 2., überarbeitete und erweiterte Auflage. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4, S. 218 f.
- Vgl. Lührs, S. 644
- Vgl. Oberdorfer, S. 7 .
- Vgl. Friedberger & Fröhner, S. 440 .
- Vgl. Friedberger & Fröhner, S. 439.
- Marianne Abele-Horn (2009), S. 219.