2-Methoxynaphthalin
2-Methoxynaphthalin (auch 2-Naphthylmethylether oder Yara-Yara genannt) ist eine organische chemische Verbindung, die das Gerüst des Naphthalins hat und die sich vom 2-Naphthol (auch β-Naphthol genannt) ableitet. Es ist ein farbloser Feststoff, der seit über einem Jahrhundert als Duftmittel eingesetzt wird, beispielsweise in billigen Seifen[7][8] oder in Räucherstäbchen.[6] Der Geruch erinnert an Orangenblüten und damit an das Orangenblütenöl Neroli. Deshalb wurde 2-Methoxynaphthalin – wie das ähnlich durftende homologe 2-Ethoxynaphthalin – auch als Nerolin vermarktet. Zur Unterscheidung wurde 2-Methoxynaphthalin Nerolin I oder Nerolin alt genannt, 2-Ethoxynaphthalin Nerolin II oder Nerolin neu. Der Duft des Methylethers wird auch als Akaziennote beschrieben.[9] Diese Stoffe sind Ersatzstoffe, die nicht in den duftenden Blüten der Natur vorkommen.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
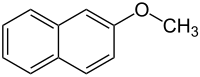 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2-Methoxynaphthalin | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C11H10O | ||||||||||||||||||
| Kurzbeschreibung |
farb- kristallines Pulver[3] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 158,20 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,064 g·cm−3[4] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
274 °C[3] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in kaltem Wasser[6] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Geschichte
Über eine erste Darstellung und Charakterisierung von 2-Methoxynaphthalin wurde 1879 berichtet, wobei der Geruch damals als „nach Ananas“ beschrieben wurde.[10]
Darstellung
Die Darstellung erfolgt aus 2-Naphthol und einem Methylierungsreagenz wie Methanol, Dimethylsulfat oder Diazomethan, wobei insbesondere die Methylierung mittels Dimethylsulfat genannt wurde.[9] Als Katalysator für die Reaktion zwischen 2-Naphthol und Methanol wird zumeist Schwefelsäure verwendet,[7] aber es können auch Molekularsiebe genutzt werden.[11] Auch eine Synthese vom Typ der Williamson-Ethersynthese ist möglich, sie geht z. B. vom Natriumsalz des 2-Naphthols aus, das mittels Halogenmethan methyliert wird.[7]
Eigenschaften
Physikalische Eigenschaften
2-Methoxynaphthalin ist in kaltem Wasser fast unlöslich (nur 75,9 mg/Liter[12]), in heißem kaum löslich. Nur wenig löst sich in Methanol oder Ethanol. Es ist in Ether, Benzol, Chloroform und Schwefelkohlenstoff leicht löslich.[1] 2-Methoxynaphthalin kann mit Wasserdampf destilliert werden.[1] Seine Bildungsenthalpie beträgt −98 kJ·mol−1, die Verbrennungsenthalpie −5660 kJ·mol−1.[13]
Chemische Eigenschaften
Bei der Nitrierung mit Salpetersäure entsteht 1-Nitro-2-methoxynaphthalin.[1]
Verwendung
2-Methoxynaphthalin wurde wegen seines anhaftenden Geruchs vor dem 1. Weltkrieg zur Vergällung von für Industriezwecke genutzten fetten Ölen verwendet.[14] In den 1960er Jahren wurde es in den USA in einer Konzentration von maximal 11 ppm als Aromastoff in Kaugummis verwendet.[15] Außerdem diente es als Ausgangsstoff für die Synthese des fiebersenkenden Arzneistoffes Naproxen, von dem im Jahr 1970 500 kg aus 2-Methoxynaphthalin hergestellt wurden.[16] Die wichtigste Verwendung ist die als Duftstoff in billigen Seifen.[6][7][8][9]
Sicherheitshinweise
Wie die meisten organischen Substanzen ist auch dieser Ether brennbar.[3] Er ist schädlich für Wasserorganismen. Beim Umgang damit Handschuhe und Schutzbrille tragen.
Einzelnachweise
- Deutsche Chemische Gesellschaft (Hrsg.): Beilsteins Handbuch der Organischen Chemie. Die Literatur bis 1. Januar 1910 umfassend. vierte Auflage. 6 Isocyclische Oxo-Verbindungen. Julius Springer, Berlin 1923, System-Nr. 538, Funktionelle Derivate des β-Naphthols, S. 640–641 (Internet Archive).
- Eintrag zu METHYL BETA-NAPHTHYL ETHER in der CosIng-Datenbank der EU-Kommission, abgerufen am 24. Oktober 2021.
- Eintrag zu 2-Methoxynaphthalin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 24. Februar 2021. (JavaScript erforderlich)
- Datenblatt 2-Methoxynaphthalene bei Sigma-Aldrich, abgerufen am 4. April 2020 (PDF).
- Yara Yara Safety Data Sheet. Vigon, 2018, abgerufen am 4. April 2020.
- Yara Yara - Yara Yara (2-Methoxynaphthalene) Manufacturer from Vadodara. Abgerufen am 4. April 2020 (englisch).
- Eduard Gildemeister, Friedrich Hoffmann: Die ätherischen Öle. Dritte Auflage. Erster Band. Verlag der Schimmel & Co. Aktiengesellschaft, L. Staackmann, Leipzig 1928, III, Hauptbestandteile der ätherischen Öle, natürliche und künstliche Riechstoffe; Phenole und Phenoläther, β-Naphtoläther, S. 624 (Internet Archive [abgerufen am 4. April 2020] englische Version „The Volatile Oils“ von 1913 (Longmans, Green and Co, London) Seite 495–496): „zum Parfümieren billiger Haus- und Toilettenseifen viel gebrauchte Produkte“
- Walther Schrauth, C . Deite: Handbuch der Seifenfabrikation. Nach dem Handbuch von Dr. C. Deite. fünfte Auflage. Julius Springer, Berlin 1921, E. Die Feinseifen, I Die Rohstoffe für die Feinseifenfabrikation, 3. Die Riechstoffe für die Parfümierung der Feinseifen, S. 479–480 (Internet Archive): „zum Parfümieren billiger Haus- und Toilettenseifen“
- 2-Methoxynaphthalin. In: Lexikon der Chemie. Spektrum Akademischer Verlag, Heidelberg, 1998, abgerufen am 4. April 2020.
- C. Marchetti: Sopra alcuni derivati dei Naftoli. In: Gazzetta chimica Italiana. Band 9. Michele Amenta, Palermo 1879, S. 544–545 (Internet Archive, Zusammenfassung aus dem Jahresbericht über die Fortschritte der Chemie in der Hathi Trust Digital Library).
- T.Yu. Stoylkova, C.D. Chanev, H.T. Lechert, C.P. Bezouhanova: Methylation of 2-naphthol over molecular sieves. In: Catalysis Letters. Band 69, Nr. 1/2, 2000, S. 109–112, doi:10.1023/A:1019061604671.
- beta-naphthyl methyl ether, 93-04-9. In: thegoodscentscompany.com. Abgerufen am 4. April 2020 (englisch).
- M. Colomina, M.V. Roux, C. Turrion: Thermochemical properties of naphthalene compounds IV. Enthalpies of combustion and formation of 2-methoxynaphthalene, 2-ethoxynaphthalene, and 2,3- and 2,7-dihydroxynaphthalenes. In: The Journal of Chemical Thermodynamics. Band 8, Nr. 9, September 1976, S. 869–872, doi:10.1016/0021-9614(76)90164-6.
- Vergällung fetter Öle. Amtliche Verordnungen und Erlasse. In: Zeitschrift für Analytische Chemie. Band 52, Nr. 12, Dezember 1913, S. 4–6, doi:10.1007/BF01554318.
- Food Protection Committee, Food and Nutrition Board: Chemicals Used in Food Processing. Hrsg.: National Academy of Sciences, National Research Council. Publication 1274. Washington D. C. 1965, LCCN 65-060045, S. 165 (eingeschränkte Vorschau in der Google-Buchsuche).
- Peter J. Harrington, Eric Lodewijk: Twenty Years of Naproxen Technology. In: Organic Process Research & Development. Band 1, Nr. 1, Januar 1997, S. 72–76, doi:10.1021/op960009e.

