2-Iodoxybenzoesäure
2-Iodoxybenzoesäure ist eine chemische Verbindung aus der Gruppe der hypervalenten Iodverbindungen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
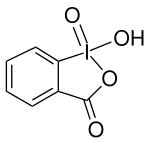 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2-Iodoxybenzoesäure | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C7H5IO4 | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 280,02 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
nahezu unlöslich in den meisten organischen Lösungsmitteln[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
2-Iodoxybenzoesäure kann durch den Dess-Martin-Prozess durch Reaktion von 2-Iodbenzoesäure mit Schwefelsäure und Kaliumbromat bei 55 °C gewonnen werden.[3] Die Verbindung wurde erstmals 1893 durch Christoph Hartmann und Victor Meyer durch Reaktion von Oxidation von 2-Iodbenzoesäure mit Kaliumpermanganat synthetisiert. Die chemische Struktur wurde 1936 von F. R. Greenbaum aufgeklärt.[1]
Eigenschaften
2-Iodoxybenzoesäure ist ein weißer kristalliner Feststoff mit intensiv saurem Geschmack, der unlöslich in den meisten organischen Lösungsmitteln ist. Er zersetzt sich bei 233 °C explosiv.[1] Das technische Produkt kommt mit Benzoesäure stabilisiert in den Handel.[2]
Trockenes, nicht stabilisiertes IBX zersetzt sich unter Licht- und Lufteinfluss, was sich in einer Verfärbung von farblos-grau nach hell rosa-orange zeigt.
Die Verbindung ist nach dem SprengG als explosionsgefährlich eingestuft und wurde der Stoffgruppe C zugeordnet.[4]
Verwendung
2-Iodoxybenzoesäure wird als Oxidationsmittel von primären und sekundären Alkoholen zu Aldehyden und Ketonen sowie von Aminen zu Iminen verwendet.[5]
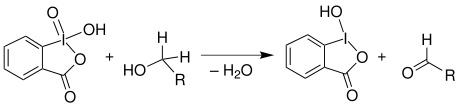
Es wird auch für andere chemische Reaktionen, so zur Beseitigung von VX-Kampfstoffen und für Dehydrierungen zu Enonen, für Oxygenierungen und für weitere oxidative Prozesse eingesetzt.[1][6]
Siehe auch
Einzelnachweise
- uni-heidelberg.de: Neue Anwendungen von IBX, abgerufen am 12. September 2015.
- Datenblatt 2-Iodoxybenzoic acid, contains stabilizer, 45 wt. % (IBX) bei Sigma-Aldrich, abgerufen am 12. September 2015 (PDF).
- W. L. F. Armarego, Christina Li Lin Chai: Purification of Laboratory Chemicals. Butterworth-Heinemann, 2013, ISBN 0-12-382161-4, S. 998 (eingeschränkte Vorschau in der Google-Buchsuche).
- Bekanntmachung der gemäß § 2 SprengG von der BAM seit 1987 neu getroffenen Feststellungen - Feststellungsbescheid Nr. 470 vom 25. November 2009 pdf-Link.
- K. C. Nicolaou, C. J. N. Mathison, T. Montagnon: New Reactions of IBX: Oxidation of Nitrogen‐ and Sulfur‐Containing Substrates to Afford Useful Synthetic Intermediates In: Angew. Chem. 115, 2003, S. 4211–4216, doi:10.1002/ange.200352076.
- Alexander Duschek, Stefan F. Kirsch: 2-Iodoxybenzoesäure - ein einfaches Oxidationsmittel mit einer Vielfalt an Anwendungsmöglichkeiten. In: Angewandte Chemie. 123, 2011, S. 1562, doi:10.1002/ange.201000873.

