1,4-Diazabicyclo(2.2.2)octan
1,4-Diazabicyclo[2.2.2]octan, auch Triethylendiamin (TEDA) genannt, ist ein bicyclisches, tertiäres Amin. Die in der Technik häufig verwendete Abkürzung „DABCO“ leitet sich direkt vom offiziellen IUPAC-Namen ab und ist ein eingetragener Markenname.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
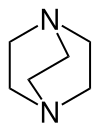 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1,4-Diazabicyclo[2.2.2]octan (IUPAC) | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H12N2 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff mit ammoniakartigem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 112,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,14 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
174–176 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Eigenschaften
TEDA ist ein bei Raumtemperatur farbloser Feststoff, der bei 159,8 °C schmilzt.[1] Es ist leicht löslich in Wasser. Durch den räumlichen Bau des Moleküls liegen die freien Elektronenpaare des Stickstoffs sterisch ungehindert vor, was sich in einer ausgeprägten Nucleophilie zeigt.
In der Umwelt ist TEDA persistent und mobil.[4]
Herstellung
TEDA wird industriell durch Umsetzung von Ethylendiamin an ZSM 5-Zeolithkatalysatoren hergestellt:[5]
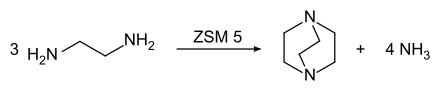
Die Verbindung kann auch durch das Erhitzen von N-Hydroxyethylpiperazin erhalten werden.[3]
Verwendung
TEDA wird als Katalysator zur Herstellung von Polyurethan-Kunststoffen[3] und als labiler Ligand oder als Base zum Beispiel bei der Baylis-Hillman-Reaktion verwendet. In der organischen Synthese dient es als Reagenz für die Spaltung von Estern, die Decarboxylierung von geminalen Diestern, zur Herstellung von Azirinen aus Vinylaziden und zahlreichen weiteren Reaktionen.[3] 1,4-Diazabicyclo[2.2.2]octan wird außerdem als Linker für die Synthese von Metall-organischen Gerüstverbindungen eingesetzt.[6]
Markenname
Die in der Technik häufig verwendete Abkürzung „DABCO“ leitet sich direkt vom offiziellen IUPAC-Namen 1,4-Diazabicyclo[2.2.2]octan ab und ist ein eingetragener Markenname des Unternehmens Evonik Industries AG für aminbasierte Katalysatoren.[7]
Einzelnachweise
- Eintrag zu 1,4-Diazabicyclo(2.2.2)octan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Februar 2017. (JavaScript erforderlich)
- Datenblatt 1,4-Diazabicyclo(2.2.2)octan (PDF) bei Merck, abgerufen am 15. Juni 2017.
- Eintrag zu 1,4-Diazabicyclo[2.2.2]octan. In: Römpp Online. Georg Thieme Verlag, abgerufen am 7. Dezember 2017.
- Isabelle Neuwald, Matthias Muschket, Daniel Zahn, Urs Berger, Bettina Seiwert: Filling the knowledge gap: A suspect screening study for 1310 potentially persistent and mobile chemicals with SFC- and HILIC-HRMS in two German river systems. In: Water Research. Band 204, 1. Oktober 2021, ISSN 0043-1354, S. 117645, doi:10.1016/j.watres.2021.117645 (sciencedirect.com [abgerufen am 4. Dezember 2021]).
- Patent EP0423526: Verfahren zur Herstellung von Triethylendiamin und Piperazin. Angemeldet am 29. September 1990, veröffentlicht am 18. November 1993, Anmelder: Bayer AG, Erfinder: Jens Weitkamp, Stefan Ernst, Dieter Lindner, Hans-Josef Buysch, Artur Botta, Lothar Puppe.
- Farnoosh ZareKarizi, Monika Joharian, Ali Morsali: Pillar-layered MOFs: functionality, interpenetration, flexibility and applications. In: Journal of Materials Chemistry A. Band 6, Nr. 40, 2018, ISSN 2050-7488, S. 19288–19329, doi:10.1039/C8TA03306D (englisch).
- Innovative polyurethane foam additives. Abgerufen am 11. Januar 2018.


