Thermitreaktion
Die Thermitreaktion ist eine Redoxreaktion, bei der Aluminium als Reduktionsmittel benutzt wird, um Eisen(III)-oxid zu Eisen zu reduzieren. Das verwendete Gemisch aus Aluminiumgrieß und Eisenoxidpulver hat den Markennamen Thermit. Die Reaktion läuft sehr stark exotherm ab, also unter starker Wärmeentwicklung. Die Reaktionsprodukte sind Aluminiumoxid und elementares Eisen in glühend-flüssigem Zustand, wobei das Aluminiumoxid auf dem Eisen schwimmt. Die Reaktion erfolgt beispielsweise in einem Tontiegel, als Zündmittel wird Bariumperoxid mit Magnesium an einem Thermitanzünder ähnlich einer Wunderkerze benutzt.



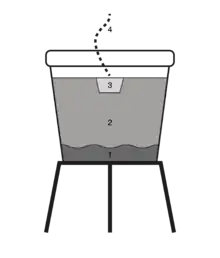



Reaktionsablauf
Die exothermische chemische Reaktion zwischen Eisenoxid und Aluminium, die umgangssprachlich Umsetzung genannt wird, liefert bei einer Temperatur von ca. 2400 °C flüssiges, kohlenstoffarmes Eisen und flüssige Aluminium-Schlacke (Aluminiumoxid, Korund):[1][2]
Bei der Bildung von Al2O3 aus den Elementen werden 1675,7 kJ/mol frei, und bei der Bildung von Fe2O3 aus den Elementen werden 824,2 kJ/mol frei:[3]
Für die Bildung des Al2O3 aus dem Fe2O3 muss dieses erst zerlegt werden, und dazu sind 824,2 kJ/mol aufzuwenden. Bei der Bildung des Al2O3 werden daher in diesem Fall insgesamt nur 1675,7 – 824,2 = 851,5 kJ/mol freigesetzt.[3]
Eine der Herausforderungen beim Thermit-Schweißen ist die Heftigkeit der Reaktion. Um zu vermeiden, dass sie so lebhaft ist, dass der Inhalt des Tiegels überkocht und Metall und Schlacke gleichermaßen verloren gehen, wird oft nicht-magnetisches Hämatit durch magnetisches Magnetit ersetzt, das aus dem Zunder von Walzwerken gewonnen werden kann:[4][5]
Nach dem gleichen Verfahren (Aluminothermie) können außer Eisen und Stahl auch andere Metalle wie Kupfer, Nickel, Titan, Chrom und Mangan erzeugt oder beigemengt werden, z. B.:
Geschichte
Das Thermitverfahren wurde 1894 von dem deutschen Chemiker Hans Goldschmidt entwickelt und wird bis heute zum aluminothermischen Verschweißen von Schienenstößen verwendet. Hans Goldschmidt betrieb als Gutsbesitzer in Paulinenaue von 1918 bis zu seinem Tod eine Forschungswerkstatt mit Schweißerei und Tischlerei.[6][7][8]
Sicherheit
Aluminothermische Schweißgemische sind keine Explosivstoffe und lassen sich nur durch eine sehr große Wärmezufuhr (Aktivierungsenergie) zur Umsetzung (Entzündung) bringen. Die Entzündungstemperatur des für Schweißzwecke verwendeten Zusatzwerkstoffes liegt bei über 1500 °C; diese wird mit einem pyrotechnischen Anzünder erreicht, aber auch ein einfacher Magnesiumstab kann die benötigte Energie und Temperatur liefern. Auch ein Gasbrenner mit Propan und Sauerstoff eignet sich als Anzünder. Als Sicherheitsmaßnahme werden Thermitschweißmassen und -anzünder getrennt gelagert, damit bei einem Brand eventuell brennende Anzünder nicht in die Schweißmasse fallen.
Die volumen- oder gewichtsmäßig bezogene Energiedichte (spezifische Enthalpie) von aluminothermischen Schweißmassen ist wesentlich geringer als diejenige von Stoffen, die mit Luftsauerstoff verbrennen (Leichtmetalle, Phosphor, Benzine, Benzol, Napalm II). Vergleich: Aluminothermische Schweißportionen besitzen ca. ein Viertel der spezifischen Enthalpie von Holz. Dies liegt daran, dass das in diesen Portionen enthaltene Eisenoxid überhaupt keine Energie liefert, sondern erst in metallisches Eisen und Sauerstoffionen zerlegt werden muss, was einen beträchtlichen Energieaufwand erfordert.
Da reagierende aluminothermische Schweißportionen keinen externen Sauerstoff benötigen, kann die Reaktion nicht erstickt werden und in jeder Umgebung – auch unter Sand oder Wasser – gezündet werden und weiterbrennen.
Löschversuche mit Wasser sowie Feuchtigkeit führen zu einer weiteren Redoxreaktion, in der das Wasser von den unedleren Metallen reduziert wird und so Metalloxid und Wasserstoff entstehen:
Der dabei entstehende Wasserstoff reagiert bei diesen Temperaturen wieder mit Luftsauerstoff zu Wasser, das wiederum mit Aluminium und Eisen reagiert. Die Anwesenheit von Wasser stellt daher eine große Gefahr bei der aluminothermischen Reaktion dar und führt zum explosionsartigen Ausschleudern glutflüssiger Stoffe sowie zu explosionsfähigen Wasserstoff-Sauerstoff-Mischungen (Knallgas). Aluminothermische Gemische müssen daher trocken gelagert werden. Schweißstellen im Gleisbau werden in der Regel zuvor mit einem Gasbrenner auf über 100 °C erhitzt, um sie zu trocknen.
Anwendungen
Die Anwendungen von aluminothermischen Reaktionen sind vielfältig. Die häufigste Anwendung ist die Reduktion von Eisen(III)-oxid, wobei Temperaturen von über 2000 °C erreicht werden können:
Thermitschweißen im Gleisbau
Schienen wurden bei der Straßenbahn in Essen erstmals 1899 mit Thermit verschweißt. Bis in die 1920er Jahre hinein wurde ein weltweites Vertriebs- und Fertigungsnetzwerk aufgebaut. Im Jahr 1928 führte die Deutsche Reichsbahn das Thermitschweißen als Regelschweißverfahren ein. Fast alle weiteren Eisenbahngesellschaften der Welt folgten bis in die Zeit nach dem Zweiten Weltkrieg.[9][10]
An die mit etwa 2 cm Lücke fest ausgerichteten Schienen werden seitlich Gusshalbformen angesetzt, mit Halteblechen angepresst und mit Formsandmasse abgedichtet. Mit einer Gasflamme werden dann die Schienenenden samt Form getrocknet und vorgewärmt. Der Schmelztiegel (heute oft ein fertig gefüllter Einweg-Blechkübel) mit Schamotteauskleidung wird genau über dem Einguss positioniert. Sicherheitshalber wird erst dann ein Zünder, eine Zündkirsche mit Zündschnur oder ein schon angezündetes Zündstäbchen, hinzugefügt. Das Aufsetzen einer Tiegelkappe mit Mittelloch isoliert und schützt vor Spritzern, während sich die Pulvermischung rauchend umsetzt. Früher wurde der Guss manuell ausgelöst, heute in der Regel selbsttätig durch einen schmelzenden Verschlussstopfen. Der flüssige Stahl rinnt dabei in die Form, füllt sie und läuft an Steigkanälen über, wobei die Schienenenden etwas aufgeschmolzen werden. Nach drei Minuten ist die Schweißstelle so weit erstarrt, dass die Form entfernt und die Bearbeitung oben durch Abscheren beginnen kann.[11][2][1][12] Beim Erkalten wird die Schweißstelle grob geschliffen, das Entfernen der Steiger und der Feinschliff der Fahrfläche erfolgen nach dem Abkühlen. Zusatzstoffe wie Vanadium machen den Schweißstahl härter als den eigentlichen Schienenstahl.
Das aluminothermische Gießschmelzschweißen (Kürzel: AS) mit Kurzvorwärmung (…-SkV) eines Schienenstoßes hat mehrere Vorzüge: Es erfolgt mit relativ handlichem Gerät und es verbraucht nichts von der Länge etwa schon liegender Schienen, denn es bringt flüssiges Eisen in den Fügespalt ein. Auch ist es an Weichen sehr zweckmäßig. – In Schweißwerken ist allerdings die Alternative Abbrennstumpfschweißen (RA) effizienter.
Das Schweißen von Schienenstößen bewirkt eine stabilere Gleislage, damit reduziert sich der Überwachungs- und Unterhaltungsaufwand. Zusätzlich verringern lückenlos geschweißte Schienen das Rad-Schiene-Geräusch. Durch das stoßlose Aneinanderschweißen der Schienen ist eine Reduzierung des Schienenverkehrslärms um 6 dB(A) möglich.[13]
Thermitschweißen als Reparaturschweißverfahren
Thermitschweißen wurde mit großem Erfolg als Reparaturschweißverfahren eingesetzt, bis nach dem Ersten Weltkrieg effektivere Schweißverfahren entwickelt wurden.[4][14][15]
Waffen
Elektron-Thermitstäbe wurden in Kriegen als Brandbomben und Brandmittel verwendet.
In Zusammenarbeit mit der Schweizerischen Aluminium Industrie Aktiengesellschaft (A.I.A.G.) wurden Ende der 1940er Jahre durch die Schweizerische Armee spezielle Aluminotherm-Verfahren zur Unbrauchbarmachung verschiedenster Waffensysteme entwickelt.
Darstellung anderer Elemente
Die Redoxreaktion mit Aluminium (Aluminothermie) kann auch verwendet werden, um andere Metalloxide oder -erze, etwa Uranerz, Chrom(III)-oxid,[16] Siliciumdioxid oder Manganoxid zu den jeweiligen Metallen bzw. Halbmetallen zu reduzieren.[17]
Vorführungen
Wegen der beeindruckenden Reaktion mit Lichteffekten und umher sprühenden Eisentropfen wird Thermit in Schauexperimenten eingesetzt.[18] Die Thermitreaktion ist jedoch mit erheblichen Gefahren verbunden, insbesondere wenn Feuchtigkeit anwesend ist. Siehe hierzu Abschnitt Sicherheit.
Explosionsschutz
Eine Thermitreaktion kann auch durch heftigen mechanischen Kontakt erfolgen, wenn z. B. flugrostbehaftete Eisenteile auf Aluminium schlagen. Dabei können Funken geschlagen werden, die in der Lage sind, Methangasgemische zu zünden.[19][20]
Einzelnachweise
- Stephan Kallee: Thermitschweißen – Aluminothermisches Schweißen von Eisenbahnschienen.
- Gleisbau-Welt: Alu-Thermit Schweißen.
- Peter W. Atkins und Julio de Paula, übersetzt von Michael Bär: Physikalische Chemie 5. Auflage März 2013, Wiley-VCH, Weinheim, ISBN 978-3-527-33247-2.
- Stephan Kallee: Thermit-Prozess um 1910 – Eine der ersten unabhängigen Veröffentlichungen zum aluminothermischen Schweißen in Amerika.
- Richard N. Hart: The Thermit Process. In: Welding Theory, Practice, Apparatus and Tests. Electric, Thermit and Hot-Flame Processes. McGraw-Hill Book Company, London, 1910, S. 152–153 und 121–158.
- Stephan Kallee: Aluminothermie – Aluminothermisches Schweißen von Straßenbahnschienen.
- Hans Goldschmidt: Alumino-Thermics and Rail Welding. Abstract of lecture before the Columbia University Chemical Society, 13 November 1903.
- Paulinenaue als Wissenschaftsstandort. In: Paulinenaue. Abgerufen am 18. Dezember 2019 (deutsch).
- Daniel Liebthal: Schienenschweißen in Perfektion. In: Der Eisenbahningenieur. Band 71, Nr. 3, März 2020, ISSN 0013-2810, S. 39–42.
- Johannes Braun, Jörg Keichel und Andreas Peters: Aluminothermisches Schweißen: Tradition und Innovation im lückenlosen Gleis (Aluminothermic welding: tradition and innovation in continuously welded track). In: Infrastruktur Network ZEVrail, Nr. 139, 10. Oktober 2015, S. 382–389.
- Webseite Gleisbau-Welt (Memento vom 18. März 2004 im Internet Archive), Schweißverfahren, Matthias Müller, Thorsten Schaeffer, 2003–2012, abgerufen 20. April 2019.
- Lothar Fendrich (Hrsg.): Handbuch Eisenbahninfrastruktur. Band 10, Springer Berlin 2006, ISBN 3-540-29581-X, S. 317–319.
- Abgeordnetenhaus Berlin: Kleine Anfrage der Abgeordneten Claudia Hämmerling (Bündnis 90/Die Grünen) vom 19. November 2010 und Antwort Viel Lärm um nichts am Karower Kreuz und wie sicher ist die Stettiner Bahn? (Drucksache 16 / 14 932).
- Stephan Kallee: Thermit in der Praxis – Erste Anwendungen des aluminothermischen Schweißens in den USA bis 1905.
- Ernest Stütz: The Thermit Process in American Practice. Vorgetragen bei Meeting der American Society for Testing Materials im Juni 1905. In: The Iron and Steel Magazine, September 1905, S. 212–221.
- Patent US5092921.
- Patent US5152830.
- Versuch 69: Thermit-Verfahren. auf: lp.uni-goettingen.de.
- Rundverfügung des Landesoberbergamtes NRW Nr. 18.23.2-5-16, vom 16. Juni 1984 mit Anlagen.
- Technische Regeln für Betriebssicherheit, TRBS 2152 Teil 3. Gefährliche explosionsfähige Atmosphäre – Vermeidung der Entzündung gefährlicher explosionsfähiger Atmosphäre.