Tetrodotoxin
Das Tetrodotoxin (von altgriechisch τετρα- tetra- „vier“ und altgriechisch ὀδούς odoús, deutsch ‚Zahn‘‚ „Vierzähner“), kurz TTX, ist ein Nervengift, bei dem es sich um ein zwitterionisches Alkaloid aus der Imidazolin- und Pyrimidingruppe mit Guanidin-Teilstruktur handelt. 1964 wurde die Struktur des Tetrodotoxins von Robert B. Woodward aufgeklärt.[3] In Aceton ist es gut, in Wasser schlecht löslich. 4,9-Anhydro-TTX ist eine molekular geringfügig abweichende Variante dieses Giftes.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
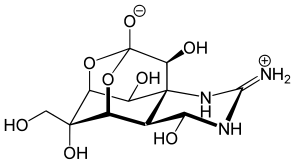 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Tetrodotoxin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C11H17N3O8 | |||||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 319,27 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Löslichkeit |
schwer in Wasser[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Giftträger
TTX und Anhydro-TTX kommen bei einigen, meist marinen, Gifttieren vor. Kugelfische, Igelfische und andere Familien der Tetraodontiformes, Westamerikanische Wassermolche, Stummelfußfrösche, einige Krebse, Schnecken, Seesterne und Blaugeringelte Kraken (Hapalochlaena) sind Träger dieses Gifts.[4] Zu den bekannten Landtieren, in denen TTX nachgewiesen werden konnte, gehören die Plattwurmarten Bipalium adventitium und Bipalium kewense.[5]
Tetrodotoxin konnte erstmals 1950 aus Ovarien von Kugelfischen isoliert werden, nachdem die Isolierungsversuche bereits 1909 begonnen hatten.
Bildung
Aufgrund der enormen Vielfalt von Tieren, welche TTX enthalten, wird angenommen, dass sie es nicht selbst bilden, sondern es aus ihrer Umwelt sequestrieren.
Es wurden Stämme aus vier Gattungen mariner Bakterien identifiziert, die TTX oder Anhydro-TTX produzieren und somit als Quellen dienen könnten: Pseudomonas (Pseudomonas spp.), Vibrio (Listonella pelagia oder Vibrio pelagius), Shewanella (Shewanella alga) und Alteromonas (Alteromonas tetraodoni und Pseudoalteromonas haloplanktis oder Alteromonas haloplanktis).[6] Als Fingerzeig galt, als an der Haut des Kugelfisches Takifugu poecilonotus Pseudomonas identifiziert wurde.[7]
Angehörige der Vibrionaceae stehen aber seither im Fokus der Untersuchungen,[8] nachdem weitere Angehörige von Vibrio als Quellen von TTX wahrscheinlich gemacht werden konnten. So wurden Vibrio fischeri (nun Aliivibrio fischeri) bei der Olivgrünen Steinkrabbe (Atergatis floridus) und Vibrio alginolyticus aus dem Magen des Kugelfisches Takifugu vermicularis isoliert.[9] Daher wird vermutet, dass TTX nicht von den Tieren produziert wird, sondern dass sie es durch Aufnahme von Vibrio-Bakterien oder durch eine Symbiose mit ihnen erhalten.[8]
Die Biosynthese des Tetrodotoxins ist nicht vollständig geklärt. Einer japanischen Arbeitsgruppe der Universität Nagoya um Tohru Fukuyama gelang eine Totalsynthese der Verbindung ausgehend von 1,4-Benzochinon über 31 Synthesestufen.[10][11]
Wirkung
Tetrodotoxin blockiert spannungsaktivierte Natriumkanäle, die auch in Neuronen vorkommen. Dabei ist zu unterscheiden zwischen den TTX-sensitiven (Nav 1.1 - Nav 1.7, mit Ausnahme Nav 1.5) und TTX-resistenten (Nav 1.5, Nav 1.8, Nav 1.9) Natriumkanälen[12]. Durch eine Blockade der Kanäle können keine Aktionspotentiale mehr ausgelöst werden, wodurch die Nerven- und Muskelerregung behindert oder unterbunden wird. Die Folge sind motorische und sensible Ausfälle. Tetrodotoxin zählt zu den stärksten Nicht-Protein-Giften und wird hinsichtlich seiner Toxizität nur von wenigen anderen Giften wie beispielsweise Maitotoxin übertroffen. Die tödliche Dosis von Tetrodotoxin beträgt etwa 10 Mikrogramm pro Kilogramm Körpergewicht.
Die Symptome der Vergiftung nach einer Aufnahme des Giftes (etwa beim Verzehr von Haut, Leber oder Eierstöcken des Fugu) beginnen innerhalb einer recht kurzen Zeit von etwa 45 Minuten. Der Patient zeigt diverse Lähmungserscheinungen, darunter die Lähmung der Skelettmuskulatur und somit auch der Atemmuskulatur; zudem fallen Koordinations- und Wahrnehmungsprobleme auf. Eine Beatmung und die orale Gabe medizinischer Kohle kann helfen. Wenn der Patient die ersten 24 Stunden nach Aufnahme des Giftes überlebt, ist die Prognose sehr gut.
Beispiel: Bei Konsum der letalen Dosis von 0,5 bis 1 Milligramm auf oralem Wege tritt die tödliche Wirkung erst nach einem gewissen Zeitraum ein, so dass eine Rettung der Opfer meist noch möglich ist. Wird das Gift jedoch intravenös injiziert, so wird infolge schneller Ausbreitung das gesamte Nervensystem lahmgelegt, und der Betroffene erliegt nach kurzer Zeit einer Atemlähmung.
Eine Tetrodotoxin-Vergiftung durch orale Aufnahme kann in vier Schweregrade unterteilt werden, die anhand der Symptomatik unterschieden werden:[13][14]
- Grad 1: Gefühlsstörungen im Mund- und Rachenbereich, eventuell Verdauungsbeschwerden
- Grad 2: ausgedehnte Parästhesien und Taubheitsgefühle, beginnende Lähmungserscheinungen, Koordinationsstörungen
- Grad 3: ausgedehnte schlaffe Lähmungen mit Ateminsuffizienz, Aphonie, autonome Ausfallerscheinungen (Hypotonie, Mydriasis)
- Grad 4: schwere Ateminsuffizienz, Kreislaufversagen, Bewusstseinsstörungen, Bradyarrhythmien
Nutzung
Da Tetrodotoxin in sehr geringen Mengen eine schmerzlindernde Wirkung zeigt, wird es auch für den Einsatz bei Krebstherapien in Betracht gezogen.[15]
Zudem ist es das Gegengift zum alkaloiden Toxin Batrachotoxin der Pfeilgiftfrösche.
In der biologischen und neurologischen Forschung wird TTX verwendet, um experimentell selektiv Natriumkanäle zu blockieren.
Filmische Erwähnung
- Gesetz der Rache
- Die Schlange im Regenbogen
- Das A-Team (2010)
- Die purpurnen Flüsse (Staffel 2, Folge 3)
- MacGyver (Staffel 7, Folge 6)
- Columbo (Staffel 7, Folge 2)
- Death in Paradise (Staffel 3, Folge 2)
- Alphateam – Die Lebensretter im OP (Staffel 8, Folge 1)
- Blindspot (Staffel 4, Folge 18)
- Akte X (Staffel 2, Folge 15)
- Miami Vice (Staffel 2, Folge 8)
- Ghost in the Shell (2017)
- Bones (Staffel 4, Folge 22)
- Alex Cross
Literatur
- Kyosuke Tsuda: Tetrodotoxin, Giftstoff der Bowlfische. In: Naturwissenschaften. 1966, 53 (7), S. 171–176.
- Gerhard G. Habermehl, Hans Chr. Krebs: Gifttiere und ihre Waffen. In: Naturwissenschaften. 1986, 73 (2), S. 459–470.
- D. F. Hwang, O. Arakawa u. a.: Tetrodotoxin-producing bacteria from the blue-ringed octopus Octopus maculosus. In: Marine Biology., 1989, 100 (39), S. 327–332.
- D. F. Hwang, K. P. Tai u. a.: Tetrodotoxin and derivatives in several species of the gastropod Naticidae. In: Toxicon, 1991, 29 (8), S. 1019–1024.
Weblinks
- Bernhard Peter: Tetrodotoxin
Einzelnachweise
- Datenblatt Tetrodotoxin (PDF) bei Carl Roth, abgerufen am 27. Januar 2019.
- Eintrag zu Tetrodotoxin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- R. B. Woodward, J. Zanos. Gougoutas: The Structure of Tetrodotoxin. In: Journal of the American Chemical Society. 86, 1964, S. 5030, doi:10.1021/ja01076a076.
- Becky L. Williams, Charles T. Hanifin, Edmund D. Brodie Jr., Roy L. Caldwell: Ontogeny of tetrodotoxin levels in blue-ringed octopuses: Maternal investment and apparent independent production in offspring of Hapalochlaena lunulata. In: Journal of Chemical Ecology, Band 37, Nr. 1, 2011, S. 10–17, doi:10.1007/s10886-010-9901-4.
- Amber N. Stokes et al.: Confirmation and Distribution of Tetrodotoxin for the First Time in Terrestrial Invertebrates: Two Terrestrial Flatworm Species (Bipalium adventitium and Bipalium kewense). PLoS ONE 9(6): e100718, 2014, doi:10.1371/journal.pone.0100718.
- Usio Simidu, Kumiko Kita-Tsukamoto, Takeshi Yasumoto, Mari Yotsu: Taxonomy of four marine bacterial strains that produce tetrodotoxin. In: International journal of systematic bacteriology. Band 40, Nummer 4, Oktober 1990, S. 331–336, doi:10.1099/00207713-40-4-331, PMID 2275851.
- Takeshi Yasumoto, Daisuke Yasumura, Mari Yotsu, Tooru Michishita, Amane Endo, Yuichi Kotaki: Bacterial production of tetrodotoxin and anhydrotetrodotoxin. In: Agricultural and Biological Chemistry, Band 50, Nr. 3, 1986, S. 793–795. doi:10.1080/00021369.1986.10867470 (freier Volltext)
- U. Simidu, T. Noguchi, D. F. Hwang, Y. Shida, K. Hashimoto: Marine bacteria which produce tetrodotoxin. In: Applied and Environmental Microbiology. Band 53, Nummer 7, Juli 1987, S. 1714–1715, PMID 3310884, PMC 203940 (freier Volltext).
- T. Noguchi, D. F. Hwang, O. Arakawa, H. Sugita, Y. Deguchi, Y. Shida, K. Hashimoto: Vibrio alginolyticus, a tetrodotoxin-producing bacterium, in the intestines of the fish Fugu vermicularis vermicularis. In: Marine Biology, Band 94, Nr. 4, 1987, S. 625–630, doi:10.1007/BF00431409.
- Tomoaki Maehara; Keisuke Motoyama; Tatsuya Toma; Satoshi Yokoshima; Tohru Fukuyama: Total Synthesis of (−)‐Tetrodotoxin and 11‐norTTX‐6(R)‐ol in Angew. Chem. 129 (2017) 1571–1574, doi:10.1002/ange.201611574.
- Keigo Murakami; Tatsuya Toma; Tohru Fukuyama; Satoshi Yokoshima: Total Synthesis of Tetrodotoxin in Angew. Chem. 132 (2020) 6312–6316, doi:10.1002/ange.201916611.
- Natriumkanäle. (spektrum.de [abgerufen am 6. Juli 2018]).
- Vaishali Bane, Mary Lehane, Madhurima Dikshit, Alan O'Riordan, Ambrose Furey: Tetrodotoxin: Chemistry, Toxicity, Source, Distribution and Detection. In: Toxins. 6, 2014, S. 693, doi:10.3390/toxins6020693.
- Jorge Lago, Laura Rodríguez, Lucía Blanco, Juan Vieites, Ana Cabado: Tetrodotoxin, an Extremely Potent Marine Neurotoxin: Distribution, Toxicity, Origin and Therapeutical Uses. In: Marine Drugs. 13, 2015, S. 6384, doi:10.3390/md13106384.
- N. A. Hagen, P. du Souich u. a.: Tetrodotoxin for moderate to severe cancer pain: a randomized, double blind, parallel design multicenter study. In: Journal of pain and symptom management. Band 35, Nummer 4, April 2008, S. 420–429, doi:10.1016/j.jpainsymman.2007.05.011. PMID 18243639.
