Aktionspotential
Als Aktionspotential, abgekürzt AP, wird in der Physiologie eine vorübergehende charakteristische Abweichung des Membranpotentials einer Zelle vom Ruhepotential bezeichnet. Ein Aktionspotential bildet sich selbsttätig mit zelltypischem Verlauf bei einer Erregung (Exzitation) der Zelle und breitet sich als elektrisches Signal über die Zellmembran aus. Umgangssprachlich werden die Aktionspotentiale von Nervenzellen auch „Nervenimpuls“ genannt.
Nur erregbare Zellen können auf Reize oder Signale hin Aktionspotentiale bilden, durch kurzfristige Änderungen der Membranleitfähigkeit infolge von Wechselwirkungen besonderer spannungsgesteuerter Ionenkanäle in ihrer Membran. Deren zeitabhängig unterschiedliche Aktivierung führt zu verschiedenen Ionenströmen mit entsprechend verschobenen Potentialdifferenzen. Daraus resultiert ein Aktionspotentialverlauf, bei dem auf die Phase der Depolarisation nach einem eventuellen Plateau die Phase der Repolarisation folgt, mit nachschwingender Hyperpolarisation. Dieser Vorgang läuft jeweils selbsttätig in typischer Form ab, wenn ein bestimmtes Schwellenpotential überschritten wird, und ist erst nach einer gewissen Refraktärzeit wieder auslösbar.
Zu den erregbaren Zellen gehören bei Tieren außer ihren Nervenzellen auch Muskelzellen und einige sekretorische Zellen. Nervenzellen nehmen Reize oder Signale von anderen Zellen auf, überführen sie in Membranpotentialveränderungen und können Aktionspotentiale bilden (Erregungsbildung) als zelleigenes Signal, das entlang dem Axon in einer Nervenfaser fortgeleitet (→ Erregungsleitung) und über Synapsen an andere Zellen übertragen wird (→ Erregungsübertragung). Über neuromuskuläre Synapsen werden Muskelzellen erreicht, die ebenfalls erregt werden können und dann Aktionspotentiale bilden, die geleitet über Membraneinstülpungen eine Kontraktion der Muskelfaser bewirken. Über neuroglanduläre Synapsen werden Drüsenzellen erreicht; besondere neuroendokrine Zellen können Aktionspotentiale bilden, denen eine Abgabe von Neurohormonen folgt.
Daneben kommen Aktionspotentiale auch in Einzellern vor – beispielsweise bei Pantoffeltierchen[1] und Kieselalgen[2] – sowie ebenfalls bei mehrzelligen Algen (Armleuchteralgen),[3] Gefäßpflanzen (Mimose)[4] und Pilzen.[5]
Geschichte
Das Phänomen von Muskelbewegungen infolge elektrischer Kräfte entdeckte der Bologneser Luigi Aloisio Galvani als Zuckung von Schenkeln sezierter Frösche.[7] Dessen 1791[6] veröffentlichen Erkenntnisse über eine „tierische elektrische Flüssigkeit“ in Nerven und Muskeln veranlassten Alessandro Volta zu seinen Untersuchungen über den Galvanismus, die 1799 zur Erfindung der ersten Batterie führten – Volta’sche Säule genannt. Volta nutzte diese auch dazu, die Auswirkung von Gleichspannung auf Lebewesen zu untersuchen.[8]
1952 legten Alan Lloyd Hodgkin und Andrew Fielding Huxley ein mathematisches Modell[9] vor, das die Entstehung des Aktionspotentials im Riesenaxon des Tintenfisches durch das Wechselspiel verschiedener Ionenkanäle erklärt und unter dem Namen Hodgkin-Huxley-Modell berühmt wurde. Für diese Entdeckung erhielten die beiden Forscher zusammen mit John Eccles 1963 den Nobelpreis für Medizin.
Grundlagen
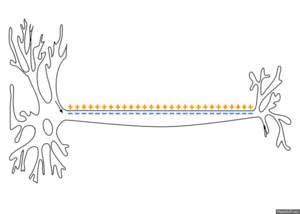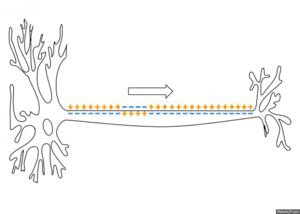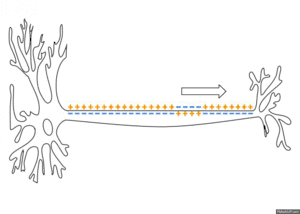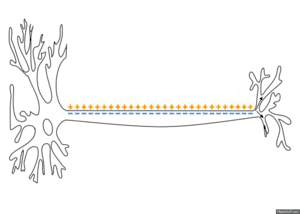
Ein Aktionspotential verläuft in einer für die Zellart typischen Form. Es dauert bei Nervenzellen oft nur etwa ein bis zwei Millisekunden, bei Skelettmuskelzellen kaum länger, bei Herzmuskelzellen meist über 200 ms. Reizabhängig stärkere oder schwächere Aktionspotentiale gibt es dabei nicht, vielmehr sind es Alles-oder-Nichts-Antworten. Die Signalstärke ergibt sich daher aus der Frequenz von Aktionspotentialen. Sie entstehen bei Nervenzellen typischerweise am Axonhügel und werden in Serien das Axon entlang fortgeleitet. Aktionspotentiale können sich auch rückwärts über den Zellkörper und die Dendriten ausbreiten; die Funktion dieser Weiterleitung wird noch untersucht. Die axonale Ausbreitung vom Zellkörper zum Endknöpfchen wird orthodrom genannt, die gegenläufige antidrom.[10]
Voraussetzung für die Ausbildung eines Aktionspotentials sind besondere Eigenschaften der Plasmamembran der Zelle. Die spezifische Ausstattung mit verschiedenen Gruppen von Ionenkanälen spiegelt sich in Kennzeichen der Verlaufsform wider. Zu einer Erregung kommt es, wenn sich das Membranpotential vom Ruhewert entfernt und in Richtung weniger negativer Werte verschiebt. Erreicht diese anfängliche Vordepolarisation eine bestimmte Schwelle, das sogenannte Schwellenpotential (etwa bei −55 mV), werden spannungsgesteuerte Ionenkanäle aktiviert, die sich in verketteter Abfolge öffnen, damit Ionenströme ermöglichen, und wieder inaktivieren.
Während dieser Kette von Öffnungs- und Schließungsvorgängen der Kanäle ändern sich also vorübergehend die Membranleitfähigkeiten für verschiedene Ionen. Die damit verbundenen kurzzeitig auftretenden Ionenströme führen gemeinsam zu einem charakteristischen Potentialverlauf. Dessen Form ist zellbezogen die gleiche, unabhängig von der Stärke des auslösenden überschwelligen Reizes. Die kurzzeitigen Änderungen des Potentials breiten sich nun (elektrotonisch) auf den benachbarten Membranbereich aus und können dann erregend auch hier wieder zum Aktionspotential führen, was die Grundlage der Erregungsleitung ist.
Potentialverlauf
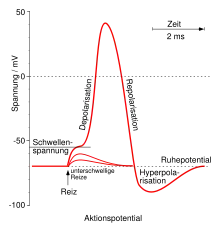
Ausgehend vom Ruhemembranpotential, das bei Neuronen je nach Zelltyp zwischen −90 und −70 mV liegt, werden vier Phasen des Aktionspotentials unterschieden:
- In der Initiationsphase treibt ein Reiz die negative Spannung in Richtung null (Depolarisation). Dies kann langsam oder schnell geschehen und ist unterhalb des Schwellenpotentials umkehrbar. Solch ein Reiz kann ein sich räumlich näherndes Aktionspotential sein oder ein postsynaptischer Ionenstrom.[11]
- Falls das Schwellenpotential überschritten wird, beschleunigt sich die Depolarisation stark (Aufstrich). Das Membranpotential wird sogar positiv (Overshoot).
- Auf das Maximum bei +20 bis +30 mV folgt die Rückkehr in Richtung Ruhepotential (Repolarisation).
- In vielen Neuronen wird das Ruhepotential zunächst unterschritten, bis z. B. −90 mV, und schließlich von tieferen negativen Werten her wieder erreicht. Dies wird als Hyperpolarisation oder hyperpolarisierendes Nachpotential bezeichnet. Während der Hyperpolarisation kann noch kein weiteres Aktionspotential ausgelöst werden.
Der zeitliche Verlauf eines Aktionspotentials kann sich über einige hundert Millisekunden hinziehen, beispielsweise in Herzmuskelzellen. Bei Nervenzellen hingegen dauert ein Aktionspotential nur etwa 1–2 ms. Danach kann ein weiteres Aktionspotential ausgelöst werden, allerdings nicht prompt, sondern erst nach einer gewissen Zeitspanne. Die Zelle befindet sich schon während der Repolarisation in dieser sogenannten Refraktärphase, bis sie wieder unter gleichen Bedingungen ein Aktionspotential bilden kann.
Man unterscheidet hierbei die absolute Refraktärzeit (ca. 0,5 ms bei Neuronen), in der gar kein Aktionspotential auslösbar ist, von der relativen Refraktärzeit (ca. 3,5 ms bei Neuronen), in der wegen des erhöhten Schwellenpotentials dafür stärkere Reizstärken nötig sind bzw. nur ein deformierter Potentialverlauf auszulösen ist. Von den Refraktärzeiten hängt die Maximalfrequenz ab, mit der ein Neuron Aktionspotentiale bilden und in Serie als Signale weiterleiten kann.
Ursachen
Das Verständnis des Aktionspotentials setzt das Verständnis des Gleichgewichtspotentials für einzelne Ionen voraus, wie es im Artikel Membranpotential beschrieben ist. Diese Spannung hängt vom Konzentrationsverhältnis außen/innen ab und kann mit der Nernst-Gleichung berechnet werden. Sind nur Kaliumkanäle geöffnet, stellt sich das Nernst-Potential von Kalium (−90 mV) ein, sind nur Natriumkanäle geöffnet, das Nernst-Potential von Natrium (+60 mV).
Ist die Membran sowohl für Kalium als auch für Natrium durchlässig, stellt sich diejenige Spannung ein, bei der die Summe beider Ströme null ist. Das Membranpotential liegt dabei umso näher am Nernst-Potential eines Ions, je größer die Permeabilität der Membran für dieses Ion ist; quantitativ wird dies durch die Goldman-Gleichung beschrieben. Bei dem Ruhemembranpotential sind vornehmlich die Kaliumkanäle geöffnet, woraus sich die niedrige Spannung von etwa −70 mV erklärt. Während eines Aktionspotentials überwiegt dagegen kurzzeitig die Permeabilität für Natrium. Sämtliche Potentiale, die im Verlauf eines Aktionspotentials auftreten, ergeben sich aus den Permeabilitäten zum jeweiligen Zeitpunkt.
Die Ströme, die im Verlauf eines Aktionspotentials auftreten, sind so klein, dass sie die Konzentrationen auf beiden Seiten der Membran nicht wesentlich verändern. Damit die Konzentrationsverhältnisse aber langfristig konstant bleiben, ist die Arbeit der Natrium-Kalium-Pumpe nötig, die unter ATP-Verbrauch drei Natriumionen im Austausch gegen zwei Kaliumionen aus der Zelle schafft.
Eigenschaften der Ionenkanäle
Wie im Artikel über das Ruhemembranpotential beschrieben, verfügen Zellen über eine Reihe von Ionenkanälen. Für das tierische Aktionspotential sind vor allem bestimmte für Natrium- bzw. Kalium-Ionen spezifische Ionenkanäle verantwortlich. Diese Kanäle öffnen sich in Abhängigkeit vom Membranpotential, sie sind somit spannungsaktiviert. In Ruhe ist das Membranpotential negativ.
So ist beispielsweise ein spannungsabhängiger Natriumkanal (Nav-Kanal) (aufgrund seiner Eigenschaft auch als schneller Natriumkanal bezeichnet) beim Ruhemembranpotential geschlossen und aktivierbar. Bei Depolarisation über einen kanalspezifischen Wert erfolgt eine Konformationsänderung der Transmembranproteine. Der Kanal wird dadurch durchlässig für Ionen und geht in den Zustand offen über. Doch bleibt der Kanal trotz anhaltender Depolarisation nicht offen, sondern wird innerhalb weniger Millisekunden wieder geschlossen, unabhängig vom Membranpotential. Das geschieht meist durch einen im Zytoplasma liegenden Teil des Kanalproteins, die Inaktivierungsdomäne, die sich gleich einem „Stöpsel“ in den Kanal setzt und diesen verstopft. Diesen Zustand bezeichnet man als geschlossen und inaktiviert.
Der anschließende Übergang in den Zustand geschlossen und aktivierbar ist nur nach einer Hyperpolarisation (oder vollständiger Repolarisation bei Herzmuskelzellen) möglich. So bleibt der Kanal zunächst geschlossen, wird nach einer Repolarisation bzw. Hyperpolarisation aktivierbar und kann erst danach wieder durch eine Depolarisation geöffnet werden. Nach einer Öffnung bleibt der Kanal nur kurzzeitig offen, da er von selbst rasch in die geschlossene Form übergeht und inaktiviert wird. Ein Übergang von inaktiviert nach offen jedoch ist bei depolarisierter Membran nicht möglich.
Nicht alle Kanäle öffnen sich gleichzeitig bei demselben Wert des Membranpotentials. Vielmehr ist die Wahrscheinlichkeit eines Kanals, in einen bestimmten Zustand überzugehen, spannungsabhängig. Aus der rein statistischen Verteilung stellt sich ein Gleichgewicht so ein, dass eine größere Zahl von Kanälen in der Summe das oben geschilderte Modell erfüllt.
Auch ist der Zeitaufwand, von einem Zustand in den anderen überzugehen, kanalspezifisch. Im geschilderten Natriumkanal läuft die Konformationsänderung von geschlossen nach offen in weniger als einer Millisekunde ab, während ein Kaliumkanal dafür rund 10 ms benötigt.
Abgesehen von der Spannung gibt es noch eine Reihe weiterer, oft chemischer Faktoren zum Öffnen bzw. Schließen der Kanäle. Für das Aktionspotential sind davon nur noch zwei von gewisser Bedeutung (siehe unten). Zum einen sind die einwärtsgleichrichtenden Kaliumkanäle (Kir) zwar an sich nicht regelbar. Es gibt jedoch niedermolekulare, positiv geladene Stoffe wie das Spermin, die bei ausreichender Depolarisation die Kanalporen verstopfen können (Kanalblock, Porenblock). Ein weiterer Mechanismus betrifft Kaliumkanäle, die öffnen, wenn intrazellulär Calciumionen (normalerweise intrazellulär in sehr niedriger Konzentration) an sie binden.
Ablauf
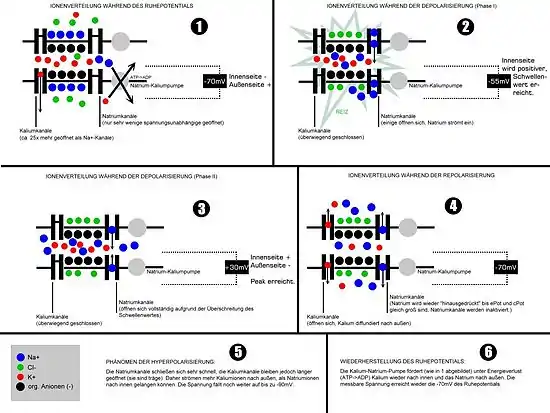
Ausgangslage
In der Ausgangslage befindet sich die Zelle in Ruhe und weist ihr Ruhemembranpotential auf. Die Natriumkanäle sind nahezu alle geschlossen, nur bestimmte Kaliumkanäle sind geöffnet. Die Kaliumionen bestimmen so im Wesentlichen das Ruhemembranpotential. Bei allen Ionenbewegungen werden Richtung und Stärke durch die elektrochemischen Triebkräfte für die jeweiligen Ionen bestimmt. Vor allem Natriumionen strömen infolge des herrschenden Konzentrationsgefälles schnell in die Zelle, sobald sich die Kanäle dafür öffnen.
Initiationsphase
Während der Initiationsphase wird das Membranpotential so verändert, dass es vom Ruhepotential abweicht in Richtung Null, bis die Verringerung des Ladungsgefälles ein gewisses Schwellenpotential erreicht. Diese Vor-Depolarisierung kann im Experiment durch eine Reizelektrode, am Axonhügel durch die Öffnung von postsynaptischen Ionenkanälen (Na+, Ca2+) oder an der Axonmembran durch ein elektrotonisch weitergeleitetes (Aktions)potential aus einer benachbarten Membranregion geschehen.
Bei derartigen vordepolarisierenden Veränderungen des Membranpotentials, beispielsweise von −70 auf −60 mV und darüber hinaus, können Kir-Kanäle durch Porenblocker wie Spermin versperrt werden. Damit wird ein in Richtung Ruhepotential gleichrichtend wirkender Kaliumstrom gedämpft. Dies erleichtert das Erreichen des Schwellenpotentials und beschleunigt die folgende Depolarisation bei Öffnung von Natriumkanälen.
Aufstrich und Overshoot
Bei ungefähr −55 mV fangen die spannungsabhängigen Natriumkanäle NaV an, in den offenen Zustand überzugehen. Natriumionen, die mit ihrer hohen Außenkonzentration weit von ihrem elektrochemischen Gleichgewicht entfernt sind, strömen ein, die Zelle depolarisiert. Dadurch werden weitere spannungsempfindliche Kanäle geöffnet, und noch mehr Ionen können einströmen: Der schnelle Aufstrich führt zum Overshoot (Umpolarisierung/Ladungsumkehr). Die „explosionsartige“ Depolarisierung nach Überschreiten des Schwellenpotentials kommt also durch eine positive Rückkopplung zustande.
Repolarisation
Noch bevor das Potentialmaximum im Overshoot erreicht ist, werden erste NaV-Kanäle inaktiv. Zugleich kommen nun die spannungsabhängigen Kaliumkanäle KV ins Spiel, K+-Ionen strömen aus der Zelle heraus. Diese Ionenkanäle haben zwar ihre Schwelle bei ähnlichen Werten, brauchen aber wesentlich länger für den Öffnungsvorgang. Während des Maximums der Na-Leitfähigkeit sind diese Kaliumkanäle erst zur Hälfte geöffnet; sie erreichen ihr Maximum, wenn fast alle Na-Kanäle schon inaktiviert sind. Daher liegt das Na-Leitfähigkeit-Maximum etwas vor dem Spannungsmaximum im Overshoot, das K-Leitfähigkeit-Maximum aber in der Phase der steilsten Repolarisation.
Während der Repolarisation nähert sich das Potential wieder dem Ruhepotential. Die KV-Kanäle schließen, und ein Porenblock der Kir wird aufgehoben, was für die Stabilisierung des Ruhepotentials wichtig ist. Die NaV-Kanäle werden langsam wieder aktivierbar. Die Repolarisation auf zum Beispiel −80 mV wird gelegentlich auch als Hyperpolarisation bezeichnet, wenn dieser Begriff als zunehmende Negativierung eines Membranpotentials definiert ist.
Nachhyperpolarisation
In vielen Zellen, vor allem Nervenzellen, ist noch eine über das Ruhepotential hinausgehende Hyperpolarisation zu beobachten. Sie erklärt sich aus einer weiterhin erhöhten Kaliumleitfähigkeit, wodurch das Potential noch näher am Kalium-Gleichgewichtspotential liegt. Die K-Leitfähigkeit ist erhöht, weil während des Aktionspotentials eingeströmte Calciumionen hier besondere Kaliumkanäle öffnen; sie normalisiert sich erst, wenn der intrazelluläre Calciumspiegel wieder absinkt. Bezeichnete man die Repolarisation bereits als Hyperpolarisation, wird dieser Vorgang einer zusätzlichen Absenkung dann Nachhyperpolarisation genannt.
Refraktärzeit
Nach dem Abklingen des Aktionspotentials ist eine Zelle für eine kurze Zeit nicht erregbar. Bei den Arbeitsmyokardzellen des Herzens ist diese Phase – hier auch „Plateauphase“ genannt – besonders lang anhaltend, was auf einen „langsamen Calcium-Einstrom“ zurückgeführt wird. Dieser Umstand ist bedeutend, denn so wird ein rückläufiger Wiedereintritt der Erregung verhindert (Unidirektionalität). Die Dauer dieser Zeitspanne, die Refraktärzeit, ist abhängig vom Zeitverlauf der Wiederaktivierung von NaV-Kanälen. Während der absoluten Refraktärphase kurz nach dem Overshoot, wenn die Repolarisation noch im Gange ist, können diese Kanäle überhaupt nicht wieder öffnen. Man sagt auch, der Schwellenwert liegt bei unendlich. Während der relativen Refraktärphase benötigt man stärkere Reize und erhält schwächere Aktionspotentiale. Hier bewegt sich der Schwellenwert von unendlich wieder auf seinen normalen Wert zu.
Schwellenpotential
Meist wird die Auslösung eines Aktionspotentials beschrieben als das Überschreiten eines bestimmten Schwellenpotentials, ab dem Natriumkanäle konzertiert geöffnet werden. Trotz aller Bemühungen eine solche exakte „Feuerschwelle“ zu finden, kann kein fixer Spannungswert angegeben werden als Bedingung für ein Aktionspotential. Stattdessen feuern Neurone auf einem relativen breiten Band auslösender Membranspannungen. Daher wird neurowissenschaftlich von der Vorstellung eines festen Wertes für das Schwellenpotential Abstand genommen. Systemtheoretisch lässt sich der Entstehungsprozess eines Aktionspotentials am ehesten durch eine Bifurkation wie beispielsweise beim Hodgkin-Huxley-Modell beschreiben. Dennoch ist es, auch in der Fachliteratur, durchaus üblich, weiterhin von einer Schwelle zu sprechen, um den „grauen Bereich zwischen Ruhe und Aktionspotential“ abgrenzend zu kennzeichnen.
Tierische Aktionspotentiale
Bei Purkinjezellen können Aktionspotentiale in ihrer Häufigkeit außer durch spannungsaktivierte Natriumkanäle auch durch spannungsaktivierte Calciumkanäle moduliert werden.[12][13]
Pflanzliche Aktionspotentiale
Prinzipiell sind Zellen von Pflanzen und Pilzen[5] auch elektrisch erregbar. Der Hauptunterschied zum tierischen Aktionspotential besteht darin, dass die Depolarisierung nicht durch Einstrom von (positiv geladenen) Natriumionen geschieht, sondern durch Ausstrom von (negativ geladenen) Chloridionen.[3][14][15] Zusammen mit dem darauffolgenden Austritt von (positiv geladenen) Kaliumionen – der gleichermaßen in tierischen wie in pflanzlichen Zellen die Repolarisierung bewirkt – bedeutet dies für Pflanzenzellen einen osmotischen Verlust an Kaliumchlorid; dagegen ist das tierische Aktionspotential durch gleiche Mengen von Natriumeinstrom und Kaliumausstrom in der Summe osmotisch neutral.
Die Kopplung von elektrischen und osmotischen Ereignissen beim pflanzlichen Aktionspotential[16] legt nahe, dass elektrische Erregbarkeit bei den gemeinsamen einzelligen Vorfahren von Tier- und Pflanzenzellen der Regulierung des Salzhaushalts unter veränderlichen Salinitätsbedingungen diente, während die osmotisch neutrale Fortleitung von Signalen durch tierische Vielzeller mit nahezu konstanter Salinität eine evolutionär jüngere Errungenschaft darstellt.[17] Demnach hat sich die Signalfunktion von Aktionspotentialen in einigen Gefäßpflanzen (beispielsweise Mimosa pudica) unabhängig von derjenigen in tierischen Zellen herausgebildet.
Literatur
- Stefan Silbernagl, Agamemnon Despopoulos: Taschenatlas der Physiologie. 6. Auflage. Thieme Verlagsgruppe, Stuttgart 2003, ISBN 3-13-567706-0.
Weblinks
- Aktionspotenzial Fortleitung – Flash-Animation in 4 Stufen bei informatik.uni-ulm.de
Einzelnachweise
- H. Machemer, A. Ogura: Ionic conductances of membranes in ciliated and deciliated Paramecium. In: The Journal of Physiology. Band 296, 1979, S. 49–60, PMID 529122.
- A. R. Taylor: A fast Na+/Ca2+-based action potential in a marine diatom. In: PLOS ONE. Band 4(3), 2009, Artikel e4966, PMID 19305505.
- M. J. Beilby: Action potentials in charophytes. In: Int. Rev. Cytol. Band 257, 2007, S. 43–82, doi:10.1016/S0074-7696(07)57002-6, PMID 17280895.
- T. Sibaoka: Excitable cells in Mimosa. In: Science. Band 137, 1962, S. 226, PMID 13912476.
- C. L. Slayman, W. S. Long, D. Gradmann: Action potentials in Neurospora crassa, a mycelial fungus. In: Biochimica et biophysica acta. Band 426, 1976, S. 737–744, PMID 130926.
- L. A. Galvani: De viribus electricitatis in motu musculari. („Über Kräfte der Electricität bei Muskelbewegung“). Bologna 1791. (online)
- M. Piccolino: Luigi Galvani and animal electricity: two centuries after the foundation of electrophysiology. In: Trends in Neuroscience. Band 20, Nr. 10, 1997, S. 443–448, doi:10.1016/S0166-2236(97)01101-6.
- M. Piccolino: The bicentennial of the Voltaic battery (1800–2000): the artificial electric organ. In: Trends in Neuroscience. Band 23, Nr. 4, 2000, S. 147–151, doi:10.1016/S0166-2236(99)01544-1.
- A. L. Hodgkin, A. F. Huxley: A quantitative description of membrane current and its application to conduction and excitation in nerve. In: J. Physiol. Band 117, 1952, S. 500–544, PMID 12991237.
- John P. J. Pinel, Paul Pauli: Biopsychologie. 6., aktualis. Auflage. Pearson Studium, 2007, ISBN 978-3-8273-7217-8, S. 110.
- Robert F. Schmidt: Physiologie des Menschen: Mit Pathophysiologie. Springer Verlag, 2007, ISBN 978-3-540-32908-4, S. 88.
- E. Hosy, C. Piochon, E. Teuling, L. Rinaldo, C. Hansel: SK2 channel expression and function in cerebellar Purkinje cells. In: The Journal of physiology. Band 589, Pt 14, Juli 2011, S. 3433–3440, ISSN 1469-7793. doi:10.1113/jphysiol.2011.205823. PMID 21521760. PMC 3167108 (freier Volltext).
- N. Zheng, I. M. Raman: Synaptic inhibition, excitation, and plasticity in neurons of the cerebellar nuclei. In: Cerebellum. Band 9, Nummer 1, März 2010, S. 56–66, ISSN 1473-4230. doi:10.1007/s12311-009-0140-6. PMID 19847585. PMC 2841711 (freier Volltext).
- H. Mummert, D. Gradmann: Action potentials in Acetabularia: measurement and simulation of voltage-gated fluxes. In: Journal of Membrane Biology. Band 124, 1991, S. 265–273, PMID 1664861.
- D. Gradmann: Models for oscillations in plants. In: Austr. J. Plant Physiol. Band 28, 2001, S. 577–590.
- D. Gradmann, J. Hoffstadt: Electrocoupling of ion transporters in plants: Interaction with internal ion concentrations. In: Journal of Membrane Biology. Band 166, 1998, S. 51–59, PMID 9784585.
- D. Gradmann, H. Mummert: Plant action potentials. In: R. M. Spanswick, W. J. Lucas, J. Dainty: Plant Membrane Transport: Current Conceptual Issues. Elsevier Biomedical Press, Amsterdam 1980, ISBN 0-444-80192-8, S. 333–344.