Skatol
Das Skatol (von altgriechisch σκῶρ skṓr [Genitiv σκατός skatós] „Kot“) ist eine sehr intensiv und unangenehm riechende Indolverbindung. Der Geruch von Fäkalien ist vor allem auf Skatol zurückzuführen.[4]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
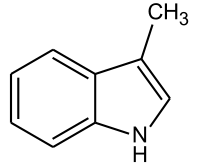 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Skatol | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C9H9N | |||||||||||||||
| Kurzbeschreibung |
weiße bis bräunliche Kristalle mit unangenehmem Geruch[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 131,17 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
265–266 °C[2] | |||||||||||||||
| Löslichkeit |
sehr schlecht in Wasser (450 mg·l−1 bei 20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vorkommen
Skatol kommt im menschlichen und tierischen Kot, im Mist (bis zu 0,1 %), im Sekret der Zibetkatze und in sehr vielen Pflanzen als Bestandteil des Blütenduftes vor. Auch das Fleisch unkastrierter Eber enthält Skatol.[5]
Entstehung
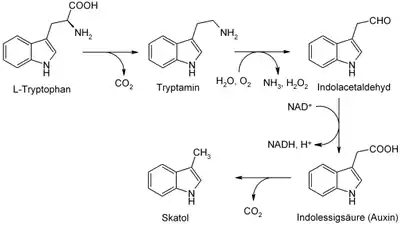
Fleisch besteht aus Eiweißen, die Bausteine der Eiweiße sind die Aminosäuren. Eine dieser Aminosäuren ist Tryptophan, eine essenzielle Aminosäure, die vom menschlichen Organismus nicht selbst gebildet werden kann, sondern mit der Nahrung aufgenommen werden muss. Die Umwandlung der Aminosäure beispielsweise bei der Verdauung in verschiedene Abbauprodukte, die teilweise vom Körper aufgenommen, teilweise ausgeschieden werden, besorgen Enzyme. Skatol ist neben Indol eines der Abbauprodukte von Tryptophan. Die Verwandtschaft von Tryptophan, Indol und Skatol ist an der allen drei gemeinsamen Ringstruktur zu erkennen. Da Tryptophan besonders häufig in tierischen Proteinen (also auch im Muskelfleisch) vorkommt, ist Skatol bei häufigem Fleischverzehr in entsprechend größerer Menge im Stuhl vorhanden.
Darstellung und Gewinnung
Skatol kann auf chemischem Wege aus Indol hergestellt werden. Da eine direkte Methylierung von Indol jedoch das 1-Methylindol (syn.: N-Methylindol) liefern würde, muss zunächst die N–H-Gruppe mit einer Schutzgruppe versehen werden. Es werden z. B. Trialkylsilyl-Schutzgruppen bevorzugt, da sie bei der nachfolgenden Deprotonierung (bzw. Lithiierung) mit Alkyllithium-Verbindungen resistent sind. Nach Umsetzung mit Methyliodid wird die Schutzgruppe wieder entfernt und man erhält Skatol.
Eigenschaften
Chemische Eigenschaften
Skatol bildet weiße Kristalle. Es reagiert heftig mit starken Oxidationsmitteln, starken Säuren, Säurechloriden und Säureanhydriden.
Physiologische Eigenschaften
Die Geruchsschwelle für Skatol in Luft ist beim Menschen außerordentlich niedrig. In der Literatur finden sich dafür Werte von 1,5 µg·m−3,[6] 0,0005 bis 6,4 µg·m−3,[7] und 0,0004 µg·m−3[8]. In Wasser beträgt der Geruchsschwellenwert 10 µg·l−1,[9] in Sonnenblumenöl 15,6 ppb.[10]
Verwendung
Skatol hat in hoher Verdünnung einen reinen, nebengeruchsarmen Geruch nach Rosen und wird in Spuren in der Parfümerie verwendet.[11]
Skatol zieht manche Insektenarten, darunter Mücken und manche Prachtbienen, an und wird daher in Labor- und Feldstudien als Lockmittel verwendet.[12][13]
Analytik
Der Nachweis von Skatol kann in einfachen Untersuchungsgütern mittels Headspace-Gaschromatographie erfolgen.[14] In komplexeren Untersuchungsmaterialien kann nach hinreichender Probenvorbereitung die qualitative und quantitative Bestimmung von Skatol durch Kopplung der Gaschromatographie mit der Massenspektrometrie vorgenommen werden.[15][16][17] Auch die Kopplung der UHPLC mit der Massenspektrometrie kommt zum Einsatz bei komplexerem Untersuchungsgut.[18]
Einzelnachweise
- Eintrag zu SKATOLE in der CosIng-Datenbank der EU-Kommission, abgerufen am 16. September 2021.
- Datenblatt Skatol (PDF) bei Carl Roth, abgerufen am 14. Dezember 2010.
- Datenblatt Skatole bei Sigma-Aldrich, abgerufen am 23. April 2011 (PDF).
- Hans Beyer, Wolfgang Walter: Organische Chemie. S. Hirzel Verlag, Stuttgart 1984, ISBN 3-7776-0406-2, S. 727.
- ValentinHarter: Vergleichende Verhaltensbeobachtung bei männlichen chirurgisch kastrierten, immunokastrierten und unkastrierten Mastschweinen. Dissertation, LMU München, 2017, S. 3–4.
- lebensministerium.at: Stand der Technik der Kompostierung - Grundlagenstudie. 29. September 2005, S. 68.
- Dorothea Lösel: Versuche zur Verbesserung der sensorischen Fleischqualität beim Schwein durch nutritive Hemmung der Skatolbildung Universität Hohenheim, Dissertation, 2006, S. 3.
Nach: J. A. Zahn, A. A. DiSpirito u. a.: Correlation of human olfactory responses to airborne concentrations of malodorous volatile organic compounds emitted from swine effluent. In: Journal of environmental quality. Band 30, Nummer 2, 2001 Mar-Apr, S. 624–634, PMID 11285926. - NIIR Board: Food Colours, Flavours and Additives Technology Handbook. Niir Project Consultancy Services, 2004, ISBN 978-8-186-62376-3, S. 287 (eingeschränkte Vorschau in der Google-Buchsuche).
- Hans-Dieter Belitz: Lehrbuch der Lebensmittelchemie. Springer-Verlag, 2013, ISBN 978-3-662-08308-6, S. 276 (eingeschränkte Vorschau in der Google-Buchsuche).
- Gerhard Eisenbrand: RÖMPP Lexikon Lebensmittelchemie, 2. Auflage, 2006. Georg Thieme Verlag, 2014, ISBN 978-3-131-79282-2, S. 1076 (eingeschränkte Vorschau in der Google-Buchsuche).
- Parfumo-Liste der Parfüms die Skatol enthalten, abgerufen am 27. April 2017.
- J. W. Beehler, J. G. Millar, M. S. Mulla: Field evaluation of synthetic compounds mediating oviposition inCulex mosquitoes (Diptera: Culicidae). In: Journal of Chemical Ecology. Band 20, Nr. 2, Februar 1994, ISSN 0098-0331, S. 281–291, doi:10.1007/BF02064436 (springer.com [abgerufen am 25. Januar 2021]).
- F. P. Schiestl, D. W. Roubik: Odor Compound Detection in Male Euglossine Bees. In: Springer (Hrsg.): Journal of Chemical Ecology. Band 29, Nr. 1, 2003, S. 253–257, doi:10.1023/A:1021932131526 (springer.com [abgerufen am 25. Januar 2021]).
- Franz von Bruchhausen: Hagers Handbuch der Pharmazeutischen Praxis. ISBN 3-540-52688-9, S. 182 (eingeschränkte Vorschau in der Google-Buchsuche).
- K. Verplanken, J. Wauters, J. Van Durme, D. Claus, J. Vercammen, S. De Saeger, L. Vanhaecke: Rapid method for the simultaneous detection of boar taint compounds by means of solid phase microextraction coupled to gas chromatography/mass spectrometry. In: J Chromatogr A. 1462, 2. Sep 2016, S. 124–133. PMID 27492596
- Y. Zhou, S. A. Hallis, T. Vitko, I. H. Suffet: Identification, quantification and treatment of fecal odors released into the air at two wastewater treatment plants. In: J Environ Manage. 180, 15. Sep 2016, S. 257–263. PMID 27235805
- M. A. Mahmoud, A. Buettner: Characterisation of aroma-active and off-odour compounds in German rainbow trout (Oncorhynchus mykiss). Part I: Case of aquaculture water from earthen-ponds farming. In: Food Chem. 210, 1. Nov 2016, S. 623–630. PMID 27211690
- K. Verplanken, J. Wauters, V. Vercruysse, M. Aluwé, L. Vanhaecke: Development and validation of a UHPLC-HR-Orbitrap-MS method for the simultaneous determination of androstenone, skatole and indole in porcine meat and meat products. In: Food Chem. 190, 1. Jan 2016, S. 944–951. PMID 26213060