Schleimsäure
Schleimsäure, auch Mucinsäure oder Galactarsäure genannt, zählt zu den Polyhydroxy-Dicarbonsäuren. Sie gehört zu den Zuckerdicarbonsäuren (Aldarsäuren). Sie zeigt keine optische Aktivität, die Schleimsäure ist epimer zur Glucarsäure. Ihre Salze und Ester werden als Galactarate oder Mucate bezeichnet.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
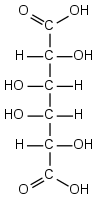 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Schleimsäure | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C6H10O8 | |||||||||||||||
| Kurzbeschreibung |
farblose, fast geruchlose Kristalle[4] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 210,14 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[4] | |||||||||||||||
| Dichte |
0,4 g·cm−3 (Schüttdichte)[4] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (3,3 g·l−1 bei 14 °C)[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Geschichte
Entdeckt wurde die Schleimsäure 1780 von Carl Wilhelm Scheele bei der Oxidation von Milchzucker durch Salpetersäure. Die Schleimsäure wurde später von Liebig und Pelouze genauer untersucht. Der Ursprung des Namens stammt von der Bezeichnung für Galactose (Schleimzucker) da dieser in Schleimhäuten vorkommt.
Gewinnung und Darstellung
Schleimsäure entsteht bei der Oxidation bestimmter Kohlenhydrate wie Lactose, Galactose oder der Galacturonsäure (Botrytissäure).
Zur Darstellung (beispielhaft) werden 25 g Galactose in 300 ml 25%iger Salpetersäure im Wasserbad auf ca. 50 ml eingedampft. Nach dem Erkalten wird die breiige Masse mit 50 ml Wasser aufgerührt. Nach einer Stunde kann man dann den Überstand absaugen und erhält so ca. 15 g Schleimsäure.[7]
Eigenschaften
Trockene Destillation (Pyrolyse) von Schleimsäure ergibt 2-Furancarbonsäure (Brenzschleimsäure).
Verwendung
Schleimsäure kann in Backpulver und Brausetabletten die Weinsäure ersetzen.
Biologische Bedeutung
Schleimsäure kann in Wein durch den Grauschimmelpilz Botrytis cinerea gebildet werden, wo sie als Calciumsalz einen Calciummucat genannten, weißen Niederschlag bildet.
Einzelnachweise
- Friedrich Albrecht Carl Gren, Christian Friedrich Bucholz: Grundriß der Chemie. Erster Theil, 4. Ausgabe, Hallisches Waisenhaus, 1818, S. 579.
- Gerhard Kempter: Studienbücherei: Organisch-chemisches Praktikum. 7. Auflage, Springer, 1978, ISBN 978-3-528-33540-3, S. 147.
- Eintrag zu GALACTARIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 30. Dezember 2021.
- Datenblatt Schleimsäure (PDF) bei Merck, abgerufen am 18. Januar 2011.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-280.
- Datenblatt Mucic acid, 97% bei Sigma-Aldrich, abgerufen am 26. Februar 2013 (PDF).
- Gattermann, Wieland: Die Praxis des organischen Chemikers. 43. Auflage, De Gruyter Verlag, 1982, ISBN 3-11-006654-8.
Literatur
- Eintrag zu Galactarsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. November 2017.