Fab-Fragment
Das Fab-Fragment, auch Fab-Antikörper (von engl. Fragment antigen binding), ist das Antigen-bindende Fragment eines Antikörpers, das durch Spaltung mit dem Enzym Papain gewonnen werden kann. Ein Fab-Fragment ist ein aus zwei Aminosäureketten aufgebautes Protein, wobei jede der beiden Ketten, die auch als leichte und schwere Kette bezeichnet werden, jeweils aus einer variablen und einer konstanten Antikörperdomäne besteht. Fab-Fragmente finden als Diagnostika und Therapeutika in der Medizin Anwendung. Darüber hinaus werden sie als wichtige Werkzeuge in der Forschung und Entwicklung eingesetzt.
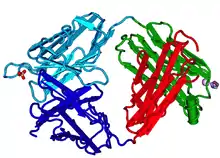
Eigenschaften
Im Gegensatz zu klassischen Antikörpern, wie dem Immunglobulin G (IgG), fehlen den Fab-Fragmenten die Fc-Einheiten. Daher fehlt Fab-Fragmenten auch die Fähigkeit, direkt zytotoxische Reaktionen durch Aktivierung des Komplementsystems auszulösen. Da die Molekülmasse von Fab-Fragmenten in der Regel unterhalb der Nierenschwelle liegt und aufgrund des Fehlens der Fc-Einheit keine aktiven Rückhaltemechanismen existieren, besitzen Fab nur eine kurze Plasmahalbwertzeit. Diese lässt sich jedoch durch Modifikation mit Polyethylenglycol verlängern (PEGylierung).[1]
Dank der um etwa Faktor drei geringeren Molekülmasse, besitzen Fab-Fragmente eine verbesserte Fähigkeit in das Gewebe einzudringen.[1]
Herstellung
Die klassische Herstellung von Fab-Fragmenten erfolgt aus monoklonalen oder polyklonalen Antikörpern mit Hilfe der enzymatischen Spaltung durch Papain. Eine effektive Möglichkeit der Produktion von Fab-Fragmenten ist die Expression in Zellkulturen wie z. B. CHO-Zellen.
Beispiele
Fab-Fragmente finden insbesondere in der Notfallmedizin als Antidote Anwendung. Dazu zählen die gegen die Herzglycoside Digoxin und Digitoxin gerichteten polyklonalen und monoklonalen Digitalis-Antidote. Die entwickelten, gegen Colchicin und gegen trizyklische Antidepressiva gerichteten Fab-Fragmente wurden zwar klinisch erprobt, sind jedoch nicht kommerziell verfügbar.[2] Ein gegen das Klapperschlangen-Gift gerichtetes polyklonales Fab-Fragment, CroFab, ist seit dem Jahr 2000 in den USA zu Behandlung von Klapperschlangenbissen zugelassen.[3]
Mit der Zunahme des Anteils der Biologicals auf dem Arzneimittelmarkt, konnten sich auch Fab-Fragmente in der Therapie etablieren. Einer der ersten monoklonalen Fab-Antikörper, der therapeutisch eingesetzt wurde, ist Abciximab. Dieses Fab-Fragment ist gegen das Glycoprotein GPIIb/IIIa auf Thrombozyten gerichtet und wird in der Prophylaxe Gefäßverschlusses nach einer perkutanen transluminalen koronaren Angioplastie eingesetzt. Ranibizumab ist ein humanisiertes, rekombinantes monoklonales, gegen VEGF-A gerichtetes Fab-Fragment, das für die Behandlung der feuchten altersbezogenen Makuladegeneration zugelassen ist.[4] Certolizumab ist ein Fab-Fragment eines rekombinanten, humanisierten monoklonalen Antikörpers, der an Polyethylenglycol konjugiert wurde. Der Arzneistoff wirkt als TNF-Blocker und wird zur Behandlung der entzündlichen Darmerkrankung Morbus Crohn eingesetzt.
Auch in der Diagnostik finden Fab-Fragmente einen Einsatz. Arcitumomab, ist ein Fab-Fragment eines murinen monoklonalen Antikörpers, der ein Epitop des carcinoembryonalen Antigens (CEA) erkennt. Dieses Protein wird besonders stark in der embryonalen Darmschleimhaut und in Karzinomen des Gastrointestinaltraktes synthetisiert. CEA ist als Erkennungsmolekül für die Darstellung metastasierender Karzinome geeignet.[5] Sulesomab, ist ebenfalls ein Fab-Fragment eines murinen monoklonalen Antikörpers, der ein Epitop auf der Oberfläche von Granulozyten erkennt. Es kann eingesetzt werden um Infektions- und Entzündungsherde, beispielsweise bei Patienten mit Osteomyelitis, darzustellen.
Einzelnachweise
- Hudson PJ, Souriau C: Engineered antibodies. In: Nat. Med.. 9, Nr. 1, Januar 2003, S. 129–134. doi:10.1038/nm0103-129. PMID 12514726.
- Flanagan RJ, Jones AL: Fab antibody fragments: some applications in clinical toxicology. In: Drug Saf. 27, Nr. 14, 2004, S. 1115–1133. PMID 15554746.
- Seger D, Kahn S, Krenzelok EP: Treatment of US crotalidae bites: comparisons of serum and globulin-based polyvalent and antigen-binding fragment antivenins. In: Toxicol Rev. 24, Nr. 4, 2005, S. 217–227. PMID 16499404.
- Fachinformation Lucentis®. Novartis Pharma. Stand 15. November 2007.
- W. J. Köstler, C. C. Zielinski: Diagnostische und therapeutische Antikörper in der Onkologie — State of the Art. In: Acta Chirurgica Austriaca. 32, Nr. 6, November 2000, S. 260–263.