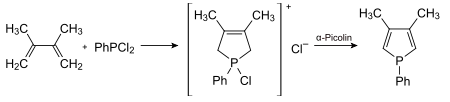
Phosphol
Phosphol ist eine organische Verbindung mit der Summenformel C4H5P; es handelt sich dabei um die phosphoranaloge Variante von Pyrrol.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||
| Allgemeines | ||||||||||
| Name | Phosphol | |||||||||
| Andere Namen |
1H-Phosphol | |||||||||
| Summenformel | C4H5P | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 84,06 g·mol−1 | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Geschichte
Erstmals wurde ein Phospholderivat 1953 entdeckt, Pentaphenylphosphol folgte 1959. Die Synthese der Titelverbindung wurde 1987 beschrieben.[2]
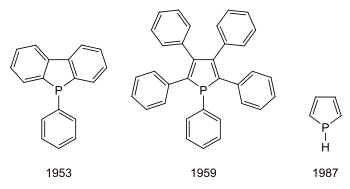
Darstellung
Allgemein werden Phosphole mittels McCormack-Reaktion[3] aus Butadienen und Dichlorphosphanen dargestellt.
Im gezeigten Beispiel kann der Phenylring anschließend mit Butyllithium abgespalten werden.
Die Protonierung von Phospholylanionen bei niedriger Temperatur ein P-unsubstituierte 1H-Phosphol. Zu den synthetisierbaren Produkten gehört das Stamm-Phosphol C4H4PH. Zwischen −70 °C und Raumtemperatur kommt es entsprechend dem Substitutionsmuster zu einer Umlagerung der 1H-Phosphole durch Protonenverschiebungen zu 2H-Phospholen um, die sofort dimerisieren.[4]
Eigenschaften
Im Gegensatz zu anderen Fünfringheterozyklen wie Pyrrol, Thiophen und Furan weist Phosphol keine Aromatizität auf, da der Phosphor sein freies Elektronenpaar nicht den π-Elektronenpaaren innerhalb des Ringes zwecks Delokalisierung zur Verfügung stellt.
Die mit im obigen Abschnitt erläuterter Darstellung erhaltenen Phospholidanionen dimerisieren bei Protonierung. Diese Dimerisierung lässt sich durch Erhitzen rückgängig machen und man erhält das thermodynamisch stabilere exo-Dimer in Analogie zu Cyclopentadienen.
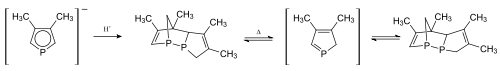 v. l.: Phospholidanion, [4+2]endo-Dimer, 2H-Phosphol, exo-Dimer
v. l.: Phospholidanion, [4+2]endo-Dimer, 2H-Phosphol, exo-Dimer
Die Charakterisierung des Phosphols kann wegen der Dimerisierung nur bei tiefen Temperaturen mittels 31P{1H}-NMR erfolgen.[5] Die chemische Verschiebung liegt für das Anion bei +76,6ppm, für das Phosphol bei −49,2ppm mit einer 1JPH Kopplungskonstanten von 234 Hz in THF.
Weitere physikalische Daten wie Siedepunkt, Schmelzpunkt etc. oder toxikologische Eigenschaften sind daher nicht bekannt.
Übergangsmetallkomplexe
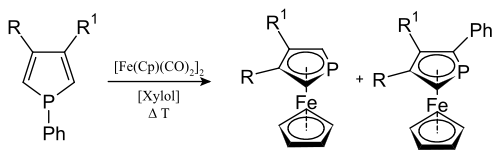 Metallocene mit Phosphol
Metallocene mit Phosphol
In Analogie zu anderen Metallocenen kann man aus Phospholen Phosphaferrocene herstellen.[6]
Vom Phospholylligand (phosphacyclopentadienyl) und dessen Derivaten sind viele andere Übergangsmetallkomplexe bekannt.[7][8] Die Liganden (L) treten hierbei als 2, 3, 4, 5 oder in anionischer Form auch als 6-Elektronendonatoren auf, von völliger Lokalisation der Ring-π-Elektronen bei endständigen Komplexen wie L-M(CO)n zum Beispiel [(CO)5W(PC4H2Me2){η5-W(CO)5}][9] über metallverbrückte 3-Elektronenliganden (µ-L)M2(CO)8 zum Beispiel (µ-PC4H2Me2)Mn2(CO)8[10] bis zu völliger Delokalisation als η5-Ligand in η5-(Me2C4H2P)W(CO)3I[11] oder im Phosphaferrocen.
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- P. J. Fagan, W. A. Nugent: 1-Phenyl-2,3,4,5-tetramethylphosphole In: Organic Syntheses. 70, 1992, S. 272, doi:10.15227/orgsyn.070.0272; Coll. Vol. 9, 1998, S. 653 (PDF).
- W. B. McCormack: U.S. Pat. 2.663.736 und 2.663.737. Volltext (Memento des Originals vom 24. September 2007 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- Claude Charrier, Hubert Bonnard, Guillaume De Lauzon, Francois Mathey: Proton [1,5] shifts in P-unsubstituted 1H-phospholes. Synthesis and chemistry of 2H-phosphole dimers. In: Journal of the American Chemical Society. Band 105, Nr. 23, 1983, ISSN 0002-7863, S. 6871–6877, doi:10.1021/ja00361a022.
- C. Charrier, H. Bonnard, G. de Lauzon, F. Mathey: Proton [1,5] shifts in P-unsubstituted 1H-phospholes. Synthesis and chemistry of 2H-phosphole dimers, in: J. Am. Chem. Soc., 1983, 105, 6871–6877; doi:10.1021/ja00361a022.
- F. Mathey, A. Mitschler, R. Weiss: Phosphaferrocene, in: J. Am. Chem. Soc., 1977, 99, 3537–3538; doi:10.1021/ja00452a076.
- E. W. Abel, N. Clark, C. Towers: η-Tetraphenylphospholyl and η-tetraphenylarsolyl derivatives of manganese, rhenium, and iron, in: J. Chem. Soc., Dalton Trans., 1979, 1552–1556; doi:10.1039/DT9790001552.
- S. Holand, F. Mathey, J. Fischer, A. Mitschler: Preparation of 3,3',4,4'-tetramethyl-1,1'-biphospholyl and its reactions with iron and cobalt carbonyls, in: Organomet., 1983, 2, 1234–1238; doi:10.1021/om50003a027.
- S. Holand, C. Charrier, F. Mathey, J. Fischer, A. Mitschler: Stabilization of 2H-phospholes by complexation. A phosphorus-carbon double bond acting as a four-electron donor, in: J. Am. Chem. Soc., 1984, 106, 826–828; doi:10.1021/ja00315a081.
- U. Flörke, O. Krampe, H.-J. Haupt: Bis(µ-3,4-dimethylphosphol-1-yl)bis(tetracarbonylmanganese), in: Act. Cryst. C, 1998, 54, 918–920; doi:10.1107/S0108270198001036.
- S. Holand, F. Mathey, J. Fischer: Synthesis and x-ray crystal structure analysis of (η5-3-4-dimethylphospholyl)tricarbonyl-iodotungsten, in: Polyhedron, 1986, 5, 1413–1421; doi:10.1016/S0277-5387(00)83502-0.
Weiterführende Literatur
- Louis D. Quin: A Guide to Organophosphorus Chemistry. John Wiley & Sons, 2000, ISBN 0-471-31824-8.