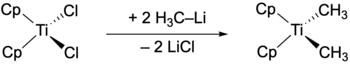Petasis-Reagenz
Bei dem Petasis-Reagenz handelt es sich um den Titankomplex Dimethyltitanocen. Es kann analog dem Tebbe-Reagenz zur Olefinierung von Ketonen, Aldehyden, Estern und Lactonen verwendet werden. Gegenüber dem Tebbe-Reagenz besitzt es den Vorteil der leichteren Herstellung und der höheren Stabilität. Des Weiteren erlaubt es auch die Einführung größerer Reste, während mit dem Tebbe-Reagenz nur eine Methenylierung möglich ist.[3]
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
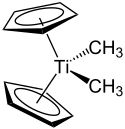 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Petasis-Reagenz | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C12H16Ti | ||||||||||||
| Kurzbeschreibung |
orangefarbener bis roter Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 208,13 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Löslichkeit | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Das Reagenz ist nach dem zyprisch-US-amerikanischen Chemiker Nicos A. Petasis (* 1954) benannt.
Herstellung
Die Herstellung des Petasis-Reagenz kann leicht aus Titanocendichlorid durch Substitution mit Methyllithium oder Methylmagnesiumchlorid bewerkstelligt werden.[4] Im Folgenden wird als Abkürzung für die Cyclopentadienyl-Liganden der auftretenden Komplexverbindungen die Abkürzung Cp verwendet.[5]
Reaktionsmechanismus
Das Petasis-Reagenz wird analog dem Tebbe-Reagenz verwendet. Wahrscheinlich wird auch als aktive Spezies das gleiche Schrock-Carben gebildet. Die Reaktion wird allerdings bei höherer Temperatur (60–80 °C) durchgeführt. Dies ist nötig um aus dem Titankomplex Methan abzuspalten und so einen Carbenkomplex zu bilden.[5]
Die Methylenierung verläuft analog der Reaktion mit der Tebbe-Reagenz: Das durch Methanabspaltung erhaltene Schrock-Carben addiert zunächst an die Carbonylkomponente unter Bildung eines Oxatitanacyclobutans. Nach Ringöffnung erhält man das methylenierte Produkt. Ähnlich wie im Falle des Phosphors bei der Wittig-Reaktion ist die Affinität von Titan zu Sauerstoff Triebkraft der Reaktion.
Verwendung
Verwendet wird das Petasis-Reagenz zur Methylenierung von Ketonen, Estern, Aldehyden und Lactonen. Besonders bei Carbonylfunktionen, die durch die Wittig-Reaktion nicht olefiniert werden können (z. B. Ester, Lactone), bietet das Petasis-Reagenz eine Alternative. Anders als beim Tebbe-Reagenz lassen sich auch in bedingtem Umfang größere Reste, wie zum Beispiel einen Benzylidenrest, einführen.
Einzelnachweise
- Datenblatt Petasis-Reagenz bei Acros, abgerufen am 26. Februar 2010.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Tanja Schirmeister; Carsten Schmuck; Peter Richard Wich: Beyer / Walter Organische Chemie. 25., völlig neu bearbeitete Auflage. Hirzel, Stuttgart 2016, ISBN 978-3-7776-1673-5, S. 700–701.
- Karl Clauss, Herbert Bestian: Über die Einwirkung von Wasserstoff auf einige metallorganische Verbindungen und Komplexe. In: Justus Liebigs Annalen der Chemie. Band 654, Nr. 1, 15. Juni 1962, S. 8–19, doi:10.1002/jlac.19626540103 (wiley.com [abgerufen am 29. Juli 2021]).
- Jie Jack Li: Name reactions: A collection of detailed mechanisms and synthetic applications. 5. edition Auflage. Springer, Cham 2014, ISBN 978-3-319-03979-4, S. 474–475, doi:10.1007/978-3-319-03979-4.