Natriumchlorat
Natriumchlorat (veraltet auch chlorsaures Natrium) NaClO3 ist das Natriumsalz der Chlorsäure (HClO3).
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
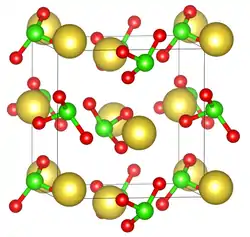 | |||||||||||||||||||
| _ Na+ _ Cl5+ _ O2− | |||||||||||||||||||
| Kristallsystem |
kubisch | ||||||||||||||||||
| Raumgruppe |
P213 (Nr. 198) | ||||||||||||||||||
| Gitterparameter |
a 6,57584 Å | ||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Natriumchlorat | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Verhältnisformel | NaClO3 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser, kristalliner, wasserlöslicher, Feststoff[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 106,44 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,49 g·cm−3 (15 °C)[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
Zersetzung ab 255 °C[2] | ||||||||||||||||||
| Löslichkeit |
gut in Wasser (916 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Brechungsindex |
1,5151[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Darstellung und Gewinnung
Natriumchlorat wird durch Elektrolyse von Natriumchloridlösung hergestellt. Das an der Anode gebildete Chlor (Cl2) reagiert zu Hypochlorit, das seinerseits durch anodische Oxidation in Chlorat übergeht.[5]
Es kann auch durch Einleiten von Chlorgas in eine warme NaOH-Lösung hergestellt werden. Mit anschließender Kristallisation erhält man das Natriumchlorat.
Eigenschaften
Natriumchlorat bildet farblose, wasserlösliche, kubische Kristalle. Es disproportioniert bei erhöhter Temperatur zunächst in Natriumperchlorat und Natriumchlorid,[5]
wobei Natriumperchlorat bei stärkerem Erhitzen weiter in Natriumchlorid und Sauerstoff zerfällt. Wässrige Lösungen reagieren schwach sauer.[2] Natriumchlorat kristallisiert kubisch, Raumgruppe P213 (Raumgruppen-Nr. 198) mit dem Gitterparameter a = 6,57584 Å.[6]
Verwendung

Natriumchlorat wird größtenteils als Bleichmittel in der Papierindustrie verwendet[7] und ist auch für die Textilindustrie geeignet.[8] Die Elementar-Chlor-Freie-Bleiche (ECF-Bleiche) bei der Zellstoffherstellung führte in den 1990er Jahren zu einer stark wachsenden Erzeugung von Natriumchlorat. Bereits um 1985 wurden fast 80 % der hergestellten Mengen zur Freisetzung von Chlordioxid verwendet.[9] Zurzeit werden etwa 90 % der Weltproduktion zu Chlordioxid weiterverarbeitet.[10] Weiterhin dient Natriumchlorat zur Herstellung von Natriumchlorit, Perchloraten sowie als Unkrautvernichtungsmittel.[5] Chlorate sind jedoch innerhalb der EU als Wirkstoffe in Pflanzenschutzmitteln nicht mehr zugelassen;[11] ein bekannter Handelsname der chlorathaltigen Herbizide war „UnkrautEx“. Die noch immer möglichen Höchstgehalte von Rückständen in Lebensmitteln/Erzeugnissen sind durch eine Verordnung (EU) geregelt[12].
Früher diente Natriumchlorat als Oxidans in einigen Explosivstoffen, doch diese werden wegen ihrer Handhabungsunsicherheit schon lange nicht mehr hergestellt. Seit 1. Februar 2021 zählt die EU es zu den beschränkten Ausgangsstoffen für Explosivstoffen mit der Folge, dass die Verwendung, der Besitz, die Verbringung und die Abgabe von Gemischen mit einem Gehalt von mehr als 40 % durch und an Personen verboten ist, die nicht zu beruflichen oder gewerblichen Zwecken handeln; die berufliche oder gewerbliche Zweckbestimmung ist bei Verkauf zu überprüfen und verdächtige Transaktionen sind meldepflichtig.[13]
Natriumchlorat ist in chemischen Sauerstoffgeneratoren enthalten, wie sie sich für Notfälle in Passagierflugzeugen über jedem Sitz befinden; sie sind über einen Schlauch mit einer Sauerstoffmaske verbunden. Bei Druckabfall im Flugzeug fallen diese Masken aus einer kleinen Kammer über dem Sitz. Der Sauerstoffgenerator wird durch das Heranziehen der Maske aktiviert. Dabei reagiert das Natriumchlorat mit Eisen zu Natriumchlorid, Eisen(II)-oxid und Sauerstoff.
Durch die bei dieser Reaktion freigesetzte Wärme wird der Generator bis zu 260 Grad Celsius heiß.[14][15]
Einzelnachweise
- Eintrag zu SODIUM CHLORATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- Eintrag zu Natriumchlorat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Index of Refraction of Inorganic Crystals, S. 10-247.
- Eintrag zu Sodium chlorate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 478–479.
- S.C. Abrahams, J.L. Bernstein: Remeasurement of optically active NaClO3 and NaBrO3. In: Acta Crystallographica. B33, 1977, S. 3601–3604, doi:10.1107/S0567740877011637 (Open Access).
- Arnold Willmes: Taschenbuch Chemische Substanzen. Harry Deutsch, Frankfurt am Main 2007, ISBN 978-3-8171-1787-1.
- Umweltbundesamt (Hrsg.): Integrierte Vermeidung und Verminderung der Umweltverschmutzung (IVU). Referenzdokument über die besten verfügbaren Techniken in der Textilindustrie. Juli 2003 (PDF (Memento vom 24. Januar 2011 im Internet Archive)).
- N. N. Greenwood, A. Earnshaw: Chemie der Elemente. VCH, 1988, ISBN 3-527-26169-9, S. 1115–1116.
- Bleaching. In: Ullmann’s Encyclopedia of Industrial Chemistry. 7. Auflage. Wiley-VCH, 2007 (Online Edition).
- Entscheidung 2008/865/EG der Kommission vom 10. November 2008 über die Nichtaufnahme von Chlorat in Anhang I der Richtlinie 91/414/EWG des Rates und die Aufhebung der Zulassungen für Pflanzenschutzmittel mit diesem Stoff
- VERORDNUNG (EU) 2020/749 DER KOMMISSION. 4. Juni 2020, abgerufen am 23. Juni 2020.
- Art. 5 der Verordnung (EU) 2019/1148 des Europäischen Parlaments und des Rates vom 20. Juni 2019 über die Vermarktung und Verwendung von Ausgangsstoffen für Explosivstoffe mit Anhang I, Inkrafttreten Art. 23, Prüfungs- und Meldepflichten der Wirtschaftsteilnehmer und Online-Marktplätze Art. 8 und 9. In Deutschland sind Verstöße gegen das Besitz-, Verwendungs- und Anwendungsverbot nach § 13 Ausgangsstoffgesetz strafbar
- Max Mahnken: Integration von Kabinensystemen in BWB-Flugzeugkonfigurationen. Hrsg.: Hochschule für Angewandte Wissenschaften Hamburg. 2006 (PDF (Memento vom 5. März 2016 im Internet Archive)).
- Jan Köhler: Aufarbeitung und Beschreibung ausgewählter Flugzeugkomponenten. Hrsg.: Hochschule für Angewandte Wissenschaften Hamburg. Abschnitt 7.3 (PDF (Memento vom 15. Januar 2014 im Internet Archive)).


