Methylaspartatzyklus
Der Methylaspartatzyklus ist ein Stoffwechselweg, der die Synthese von C4-Kohlenhydraten (wie Succinat) aus zwei Molekülen Acetyl-CoA ermöglicht. Er wurde bislang in Vertreter der Halobakterien gefunden. Alternative Stoffwechselwege zur Assimilation von Acetat sind der weit verbreitete Glyoxylatzyklus sowie der Ethylmalonyl-CoA-Weg.
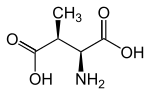
Der Stoffwechselweg verdankt seinen Namen dem Zwischenprodukt Methylaspartat.
Vorkommen
Der Methylaspartatzyklus wurde ursprünglich im Halobakterium Haloarcula marismortui nachgewiesen. Halobakterien sind halophile Archaeen, die unter hohen Salzkonzentrationen von 3 bis 5 Molar und hellen, mikroaerophilen und nährstoffreichen Bedingungen in Salzseen leben.
Im Genom einer Gruppe der Halobakterien (Stamm I) wurden Gene für den Zyklus gefunden (wie beispielsweise Natrialba magadii), während der andere Teil größtenteils auf den Glyoxylatzyklus zur Acetatassimilation zurückgreift. Manche Genome enthalten aber auch Gene für Enzyme beider Zyklen, so dass sie theoretisch beide betreiben können.
Biochemie

Der Methylaspartatzyklus beginnt mit der Kondensation von Acetyl-CoA mit Oxalacetat. Dabei entsteht Citrat, das durch Enzyme des Citratzyklus über Isocitrat zu α-Ketoglutarat umgesetzt wird. Durch eine NADP-abhängige Glutamatdehydrogenase reagiert dieses mit Ammonium (NH4+) zu L-Glutamat, das eine Glutamatmutase (EC 5.4.99.1) zu der ungewöhnlichen Aminosäure Methylaspartat umsetzt.
Methylaspartat wird durch eine Methylaspartat-Ammoniumlyase (EC 4.3.1.2) zu Mesaconat desaminiert, das durch eine Transferase zu Mesaconyl-CoA reagiert. Hierbei wird als Coenzym A-Donor Succinyl-CoA genutzt. An Mesaconyl-CoA kondensiert Wasser, dabei entsteht β-Methylmalyl-CoA. Diese Reaktion katalysiert eine Mesaconyl-CoA-Hydratase. Schließlich wird das Intermediat zu Glyoxylat und Propionyl-CoA durch die β-Methylmalyl-Lyase gespaltet.
Propionyl-CoA wird zunächst mit Bicarbonat (HCO3−) carboxyliert, was eine biotinabhängige Carboxylase katalysiert. Anschließend wird das Reaktionsprodukt zu Succinyl-CoA umgesetzt. Nach Hydrolyse entsteht daraus Succinat. Glyoxylat reagiert mit einem weiteren Molekül Acetyl-CoA zu Malat, diese Reaktion ist typisch für den Glyoxylatzyklus und wird durch die Malatsynthase katalysiert. Nach Oxidation zu Oxalacetat schließt sich der Kreis.
In der Bilanz wird aus zwei Molekülen Acetyl-CoA ein Molekül Succinat gebildet.
Biologische Bedeutung
Zur Assimilation von Acetat sind zwei Stoffwechselwege bekannt, der Glyoxylatzyklus und der lineare Ethylmalonyl-CoA-Weg. Unter aeroben Bedingungen nutzen manche Halobakterien den Glyoxylatzyklus, wie beispielsweise Haloferax volcanii. Unter strikt anaeroben Bedingungen können Halobakterien Pyruvat aus Acetyl-CoA aufbauen. Manchen aerob lebenden Halobakterien fehlt aber die Isocitratlyase (EC 4.1.3.1), ein Schlüsselenzym des Glyoxylatzyklus, sowie Enzyme für den alternativen Ethylmalonyl-CoA-Weg. Dennoch können sie auf Acetat wachsen, indem sie auf den Methylaspartatzyklus zurückgreifen, um Acetat zum Aufbau von Zellsubstanz zu nutzen.
Für die Lebensweise der Halobakterien in Salzseen kann der Methylaspartatzyklus lebensnotwendig werden. Wenn kurzfristig nährstoffreiche Bedingungen im Salzsee vorliegen, legen diese Halobakterien den Speicherstoff Polyhydroxyalkanoat an. Unter schlechteren Bedingungen bauen sie dann diesen Speicherstoff zu Acetat-CoA ab, und nutzen das Acetat im Methylaspartatzyklus. Alternativ können jene Archaeen Acetat aus dem Abbau organischer Verbindungen wie Fettsäuren, Alkoholen oder einfachen Aminosäuren (z. B. L-Lysin) gewinnen.
Für das Betreiben des Zyklus sind hohe Glutamatkonzentrationen notwendig. In H. marismortui wurde dies tatsächlich nachgewiesen, während Halobakterien, die den Glyoxylatzyklus nutzen, wesentlich geringere Mengen an Glutamat aufweisen. Glutamat ist ein Osmolyt, Vorläufer für γ-Glutamylcystein (ein Antioxidans) und γ-Polyglutamat. Letzteres ist ein extrazelluläres Polymer, dass den Halobakterien als Speicherstoff und als Schutzmantel gegenüber harschen Umweltbedingungen dient.
Der Zyklus koppelt den Stickstoffmetabolismus mit der Acetatassimilation und bildet die namensgebende, nicht-proteinogene Aminosäure Methylaspartat als Intermediat. Es sind neun Reaktionen nötig, um aus Isocitrat Succinat zu machen, im Glyoxylatzyklus ist es vergleichsweise nur eine einzige Reaktion.
Evolution
Durch Genomanalysen vermutet man, dass die Gene für den Methylaspartatzyklus wahrscheinlich durch horizontalen Gentransfer aus Bakterien in Halobakterien gelangt sind. In Bakterien dienten sie zunächst ganz anderen Aufgaben im Stoffwechsel und wurden in einigen Halobakterien im Laufe der Zeit zur Acetatassimilation umfunktioniert. Durch Beteiligung anderer Enzyme entstand schließlich ein neuer Weg zur Assimilation von Acetat. Vermutlich erfolgte diese Anpassung infolge der harschen Umweltbedingungen mit hohen Stickstoff- und Salzgehalt.
Literatur
- Khomyakova, M., Bükmez, Ö., Thomas, LK., Erb, TJ. und Berg, IA. (2011): A methylaspartate cycle in haloarchaea. In: Science 331(6015); 334–337; PMID 21252347; doi:10.1126/science.1196544
- Ensign, SA. (2011): Another microbial pathway for acetate assimilation. In: Science 331(6015); 294–295; PMID 21252338; doi:10.1126/science.1201252
Weblinks
- Das Salz in der Suppe der Evolution Pressemitteilung der Universität Freiburg vom 21. Januar 2011
- Wie man im Toten Meer überlebt. Marianne Diehl, Bild der Wissenschaft vom 21. Januar 2011 (abgerufen am 15. September 2014)