Hexachlorethan
Hexachlorethan ist eine organische chemische Verbindung des Chlors, die vielfältigen Einsatz erlangt hat.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
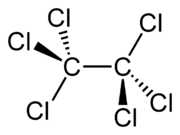 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Hexachlorethan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C2Cl6 | ||||||||||||||||||
| Kurzbeschreibung |
weißes Pulver mit campherähnlichem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 236,74 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,09 g·cm−3[1] | ||||||||||||||||||
| Sublimationspunkt | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK | |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−202,8 kJ/mol[5] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Vorkommen
Hexachlorethan gehört zu den chlorierten Kohlenwasserstoffen und wird durch Chloraddition aus Tetrachlorethen hergestellt.
Physikalische Eigenschaften
Hexachlorethan besitzt zwei kristalline Modifikationen: rhombisch bis 46 °C und triklin zwischen 46 und 71 °C.
Verwendung
Hexachlorethan wurde hauptsächlich auf zwei Gebieten verwendet.
Militärische Verwendung
Im militärischen Bereich diente die Verbindung noch bis in die zweite Hälfte des 20. Jahrhunderts der Erzeugung von künstlichem Nebel, auch als Berger-Nebel bezeichnet. Der französische Chemiker Berger stellte ein Gemenge aus Hexachlorethan und Zink-, auch Magnesium- oder Aluminiumpulver her und brachte es zur Entzündung. Für Jahrzehnte war es das militärisch meistgenutzte Mittel zur raschen Hervorbringung künstlichen Nebels, sei es aus Kartuschen, Nebeltöpfen, Artilleriegeschossen oder Wurfgranaten. Als sich um 1970 bei Bundeswehrübungen mehrfach Unfälle ereigneten, weil der Nebel in zu hoher Konzentration eingeatmet wurde, stellte man diese Art von Nebelerzeugung ein. Vorhandene Vorräte wurden delaboriert und einer bereits um 1935 bekannt gewordenen Verwendung in der Aluminiumindustrie zugeführt.
Nichteisen-Metallurgie
Beim Schmelzen und Vergießen von Aluminium und seinen Legierungen zeigte sich, dass die Herstellung wachsenden Ansprüchen gerecht werdender Gussteile (auch hier spielte die Rüstung eine Rolle) wegen der Neigung der Aluminiumschmelzen zu Oxidation und Wasserstoffaufnahme schwierig war. Die Wasserstofflöslichkeit in der Schmelze ist 15fach höher als im Festzustand, es kommt daher bei der Erstarrung der Schmelze zur Ausscheidung unter Blasenbildung im Gussstück. Es wurde gefunden, dass eine Spülung der Schmelzen mit einem geeigneten Spülgas – inert oder besser in geeigneter Form reaktiv – den Wasserstoffgehalt senkt und die Probleme verringert. Als Konsequenz wurde 1928 erstmals Chlorgas als Spülmittel eingesetzt. Chlor reagiert mit Aluminium zu Aluminiumchlorid und weil dieses bei ca. 180 °C unter Aufwallung die Schmelze verlässt, eignete es sich als Spülmittel/Entgasungsmittel (siehe auch Schmelzebehandlung).
Ein Deutsches Reichspatent (DRP) aus dem Jahr 1931, das auch vorübergehend in die Betriebspraxis einging, sieht Kartuschen vor, gefüllt mit in Kieselgur aufgesaugtem Tetrachlorkohlenstoff als Chlorträger. Die bekannt giftige Substanz setzte sich aber nicht durch. Auf der Suche nach einem ungefährlicheren Stoff fand man um 1935 erstmals Hexachlorethan in Gießereien; nach damaliger Erkenntnis ein ungefährlicher Feststoff, der kristallin oder zu Briketts verpresst, rein oder in Zubereitungen (vgl. DRP 733616) bald allgemeine Verwendung fand und bis gegen Ende des zwanzigsten Jahrhunderts in großen Mengen von der chlorchemischen Industrie erzeugt und in Aluminiumhütten und -gießereien verbraucht wurde. Das Sevesounglück, obwohl mit Herstellung und Verwendung von Hexachlorethan in keiner Verbindung, lenkte die Aufmerksamkeit aber doch auf die Chlorkohlenwasserstoffe insgesamt, eine mögliche Bildung von Hexachlorbenzol konnte schließlich nachgewiesen werden. Zwar kann durch oxidative Steuerung des Hexachlorethanzerfalls in der Schmelze diese Möglichkeit bis unter die Bedenklichkeitsschwelle gesenkt werden (DP 36 30 711.4), aber das „Aus“ für Hexachlorethan wurde damit auch für diesen zweiten großen Verwendungsbereich nur um einige Jahre hinausgeschoben.
Die Verwendung beschränkt sich heute zumindest im EU-Raum auf einige medizinische Erzeugnisse und technische Spezialprozesse mit der Folge stark rückläufiger Produktionsmengen.
Sicherheitshinweise
Hexachlorethan ist bei oraler Einnahme leberschädigend, in hoher Konzentration eingeatmet wirkt es leicht narkotisierend. Inwieweit es krebserregend sein könnte, wird seit längerem untersucht, biologisch ist es als Festsubstanz nicht gefährlich, da es in Wasser unlöslich ist. Bei Raumtemperatur sublimiert es langsam unter Camphergeruch. Bei thermischer Zersetzung in einer Metallschmelze können auch polychlorierte Dibenzodioxine und Dibenzofurane entstehen.
Einzelnachweise
- Eintrag zu Hexachlorethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 4. November 2021. (JavaScript erforderlich)
- Eintrag zu Hexachloroethan. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. November 2014.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 67-72-1 bzw. Hexachlorethan), abgerufen am 2. November 2015.
- Datenblatt Hexachlorethan bei AlfaAesar, abgerufen am 9. Dezember 2007 (PDF) (JavaScript erforderlich).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-21.
Weblinks
- Stoffangaben (englisch)
- US EPA: Factsheet (Memento vom 7. Juli 2001 im Internet Archive)
- Profil bei Scorecard.org

