Guanfacin
Guanfacin ist ein Arzneistoff aus der Gruppe der Antisympathotonika. Es senkt in niedrigen Dosen anhaltend den Blutdruck. Außer in der Behandlung des Bluthochdrucks wird Guanfacin auch in der Behandlung der Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) eingesetzt. Es ist oral wirksam.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
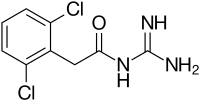 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Guanfacin | |||||||||||||||||||||
| Andere Namen |
N-(Diaminomethyliden)-2-(2,6-dichlorphenyl)acetamid | |||||||||||||||||||||
| Summenformel | C9H9Cl2N3O | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
C02AC02 | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 246,09 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Bei ADHS zeigt es eine größere Effektstärke als Atomoxetin, aber eine kleinere als Stimulanzien.[2]
Anwendungsgebiete
Guanfacin ist ein Abkömmling des Clonidins und wurde ursprünglich zur Behandlung des Bluthochdrucks eingesetzt.[3] Es bewirkte eine Senkung des Blutdrucks um etwa 16 %,[4] konnte sich aber als Blutdrucksenker nicht dauerhaft am Markt behaupten, nachdem modernere Antihypertonika mit günstigerem Nutzen-Risiko-Verhältnis entwickelt worden waren.[3]
Seit September 2015 ist Guanfacin in der Europäischen Union zur Behandlung von ADHS bei 6- bis 17-Jährigen, für die eine Behandlung mit Stimulanzien nicht in Frage kommt, nicht vertragen wird oder unwirksam war, zugelassen.[5] Guanfacin wird meistens in retardierter Form verabreicht und darf nur im Rahmen einer therapeutischen Gesamtstrategie angewendet werden, die in der Regel auch psychologische, pädagogische und soziale Maßnahmen umfasst.
In Studien hat sich Guanfacin auch bei 2 und 3 Jahre alten Kindern als wirksam erwiesen.[6]
In einer 2020 veröffentlichten klinischen Phase-III Studie erwies sich Guanfacin auch bei Erwachsenen mit ADHS als wirksam.[7]
Pharmakologie
Biochemie
Die Verbindung wirkt als sehr selektiver Agonist am α2-Adrenozeptor.[8][9] Daneben bindet es auch als selektiver Agonist an den 5-HT2B-Rezeptor.[10] In Ratten führt Guanfacin zu einem verbesserten Kurzzeitgedächtnis durch die Hemmung der Bildung des sekundären Botenstoffs cAMP im präfrontalen Cortex.[11]
Wirkungsmechanismus
Für die blutdrucksenkende Wirkung ist einerseits die Stimulierung der α2-Adrenozeptoren mit der Folge einer verminderten Noradrenalinfreisetzung als auch die agonistische Wirkung an den Imidazolinrezeptoren ursächlich. Es resultiert eine Abnahme des peripheren Gefäßwiderstandes, der Herzfrequenz und des Herzzeitvolumens.[12]
Der Wirkmechanismus von Guanfacin in der Behandlung von ADHS ist nicht vollständig geklärt. Bei Ratten zeigte sich ein dosisabhängiger Rückgang von Impulsivität, der einer angenommenen Unterstützung von Funktionen im präfrontalen Cortex zugeordnet wurde.[13]
Pharmakokinetik
Die orale Bioverfügbarkeit liegt bei 80 %. Es gibt keine Hinweise auf einen First-Pass-Effekt. Die biologische Halbwertszeit beträgt 17 Stunden. Guanfacin wird über die Niere ausgeschieden. Im Zuge der Biotransformation wird 3-Hydroxy-Guanfacin gebildet.[14]
Geschichte
Guanfacin wurde zuerst 1974 unter dem Codenamen „BS 100-141“ im Rahmen der Frühjahrstagung der Deutschen Pharmakologischen Gesellschaft in Mainz als eine neue pharmakologisch wirksame Substanz vorgestellt.[15] Es wurde 1979 zur Behandlung des Bluthochdrucks unter dem Markennamen Estulic vom damaligen Sandoz-Tochterunternehmen Wander eingeführt.[3] Seit der Zulassung des Wirkstoffs durch die US-amerikanische Food and Drug Administration im Jahr 1986, ist Guanfacin auch in den USA zur Behandlung des Bluthochdrucks auf dem Markt. Im September 2009 wurde Guanfacin unter dem Handelsnamen Intuniv zunächst in den USA zur Behandlung des ADHS zugelassen.[16] Im September 2015 folgte die arzneimittelrechtliche Zulassung in der EU durch die Europäische Arzneimittel-Agentur.[5] Im Juni 2019 erfolgte die erstmalige Zulassung von Guanfacin für ADHS bei Erwachsenen in Japan.[17]
Einzelnachweise
- Eintrag zu Guanfacin-Hydrochlorid bei TCI Europe, abgerufen am 2. Februar 2016.
- N. T. Bello: Clinical utility of guanfacine extended release in the treatment of ADHD in children and adolescents. In: Patient preference and adherence. Band 9, 2015, S. 877–885. doi:10.2147/PPA.S73167. PMID 26170637, PMC 4494608 (freier Volltext) (Review).
- K. Neumann: Zweite Chance für Guanfacin, 6. Oktober 2015.
- P. Jerie: Clinical experience with guanfacine in long-term treatment of hypertension. In: British journal of clinical pharmacology. Band 10, Suppl 1, 1980, S. 37S–47S. PMID 6994777, PMC 1430120 (freier Volltext).
- Europäische Arzneimittel-Agentur (EMA): Intuniv / guanfacine, abgerufen am 3. Februar 2016.
- Bernard J. Lee: Clinical experience with guanfacine in 2- and 3-year-old children with Attention Deficit Hyperactivity Disorder. In: Infant Mental Health Journal. Band 18, Nr. 3, September 1997, S. 300–305, doi:10.1002/(SICI)1097-0355(199723)18:33.0.CO;2-Q.
- Akira Iwanami, Kazuhiko Saito, Masakazu Fujiwara, Daiki Okutsu, Hironobu Ichikawa: Efficacy and Safety of Guanfacine Extended-Release in the Treatment of Attention-Deficit/Hyperactivity Disorder in Adults: Results of a Randomized, Double-Blind, Placebo-Controlled Study. In: The Journal of Clinical Psychiatry. Band 81, Nr. 3, 14. April 2020, ISSN 1555-2101, S. 19m12979, doi:10.4088/JCP.19m12979, PMID 32297719.
- Amy FT Arnsten: The use of α-2A adrenergic agonists for the treatment of attention-deficit/hyperactivity disorder. In: Expert Review of Neurotherapeutics. Nr. 10, Oktober 2010, S. 1595–1605, doi:10.1586/ern.10.133, PMC 3143019 (freier Volltext).
- B. L. Roth, J. Driscol: PDSP Ki Database. University of North Carolina at Chapel Hill and the United States National Institute of Mental Health.
- X.-P. Huang, V. Setola, P. N. Yadav, J. A. Allen, S. C. Rogan, B. J. Hanson, C. Revankar, M. Robers, C. Doucette, B. L. Roth: Parallel Functional Activity Profiling Reveals Valvulopathogens Are Potent 5-Hydroxytryptamine2B Receptor Agonists: Implications for Drug Safety Assessment. In: Molecular Pharmacology. 76, 2009, S. 710. doi:10.1124/mol.109.058057. PMC 2769050 (freier Volltext).
- B. P. Ramos, D. Stark, L. Verduzco, C. H. van Dyck, A. F. Arnsten: Alpha2A-adrenoceptor stimulation improves prefrontal cortical regulation of behavior through inhibition of cAMP signaling in aging animals. In: Learning & memory. Band 13, Nummer 6, Nov-Dez 2006, S. 770–776. doi:10.1101/lm.298006. PMID 17101879, PMC 1783631 (freier Volltext).
- Ernst Mutschler, Monika Schäfer-Korting: Arzneimittelwirkungen. Lehrbuch der Pharmakologie und Toxikologie. 7. Auflage. Wissenschaftliche Verlagsgesellschaft, Stuttgart 1996, S. 294.
- A. B. Fernando, D. Economidou, D. E. Theobald, M. F. Zou, A. H. Newman, M. Spoelder, D. Caprioli, M. Moreno, L. Hipólito, A. T. Aspinall, T. W. Robbins, J. W. Dalley: Modulation of high impulsivity and attentional performance in rats by selective direct and indirect dopaminergic and noradrenergic receptor agonists. In: Psychopharmacology. Band 219, Nummer 2, Januar 2012, S. 341–352. doi:10.1007/s00213-011-2408-z. PMID 21761147, PMC 3249163 (freier Volltext).
- J. R. Kiechel: Pharmacokinetics and metabolism of guanfacine in man: a review. In: British journal of clinical pharmacology. Band 10, Suppl 1, 1980, S. 25S–32S. PMID 6994775, PMC 1430131 (freier Volltext).
- G. Scholtysik: Inhibition of effects of accelerator nerve stimulation in cats and rabbits by BS 100-141 and guanabenz. In: Naunyn Schmiedebergs Arch. Pharmacol. Band 282, (Suppl), 1974, S. R86. PMID 4276642
- Drugs.com: Shire Announces FDA Approval of Once-Daily Intuniv (guanfacine) Extended Release Tablets for the Treatment of ADHD in Children and Adolescents Aged 6 to 17, abgerufen am 17. Februar 2017.
- Shionogi Got Approval of Additional Indication of INTUNIV in Japan for Treatment of Adult ADHD - CMOCRO. Abgerufen am 19. November 2021 (englisch).