Droperidol
Droperidol (Dehydrobenzperidol, DHB, DHBP) ist ein Neuroleptikum, welches zur Vorbeugung und Behandlung von Übelkeit und Erbrechen nach Operationen eingesetzt wird.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
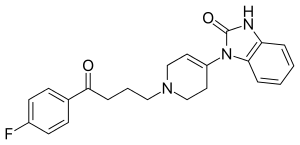 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Droperidol | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C22H22FN3O2 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes bis fast weißes, polymorphes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus |
Hemmung von dopaminergen Rezeptoren in der Area postrema | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 379,44 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| pKS-Wert |
7,46[2] | |||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Wirkmechanismus
Droperidol hat eine starke Affinität zum D2-Rezeptor (siehe Dopamin-Rezeptor) in der Area postrema, einem Teil des Brechzentrums, wo die Substanz hemmend wirkt,[4] sowie geringere Affinität zu D3-, 5-HT2- und α1-Rezeptoren.
Gegenanzeigen
Droperidol darf nicht angewendet werden bei Patienten mit:[5]
- Überempfindlichkeit/Allergie gegen Droperidol oder einen der sonstigen Bestandteile;
- Überempfindlichkeit/Allergie gegen Butyrophenone;
- bekannter oder vermuteter verlängerter QT-Zeit (QTc >450 ms bei Frauen und >440 ms bei Männern). Dies gilt auch für Patienten mit angeborener verlängerter QT-Zeit, Patienten mit angeborener verlängerter QT-Zeit in der Familiengeschichte und Patienten unter Behandlung mit Arzneimitteln, die bekanntermaßen die QT-Zeit verlängern;
- Hypokaliämie oder Hypomagnesiämie;
- Bradykardie (weniger als 55 Herzschläge pro Minute);
- Bekannter Begleitmedikation, die zu Bradykardie führen kann;
- Phäochromozytom;
- Komatösen Zuständen;
- Parkinson-Krankheit;
- Schwerer Depression.
Nebenwirkungen und Wechselwirkungen
Bis in die 1980er Jahre hinein wurde zur Prämedikation vor operativen Eingriffen das Medikament Thalamonal gegeben. Dabei handelt es sich um eine Kombination der beiden Wirkstoffe Fentanyl und Droperidol. Ziel war es, den Patienten die Angst vor dem operativen Eingriff zu nehmen und sie gleichzeitig zu sedieren. Viele Patienten äußerten nach der Operation jedoch den Wunsch, dieses Medikament in Zukunft auf keinen Fall wieder verabreicht zu bekommen. Viele von ihnen klagten auch unter dem Einfluss der beiden Wirkstoffe über innere Aufgewühltheit, depressive Episoden, sogar Panik, das Ganze bei gleichzeitig äußerer Müdigkeit. Mehrere von Ihnen zogen sogar ihr Einverständnis zum Eingriff in letzter Minute zurück oder verweigerten diesen, wegen der kurzfristigen und drastischen Verschlechterung ihres psychischen Befindens. Seit dieser Zeit setzen Anästhesisten nur noch in Ausnahmefällen die Wirkstoffkombination ein. Mittlerweile ist es Standard, zur Prämedikation Benzodiazepine zu verwenden, die von den meisten Patienten als angenehm und angstlindernd empfunden werden. Außerdem bewirken sie eine anterograde Amnesie, so dass die unangenehmen Aspekte der Operation dem Kranken nicht mehr in Erinnerung sind.[6] Weitere potenzielle Nebenwirkungen von Dehydroxybenzperidol sind Schwindel, extrapyramidale Symptome und Angst.[7]
Geschichte der Marktrücknahme und Wiederzulassung
Die Marktrücknahme der peroralen Darreichungsformen erfolgte durch den Hersteller (Janssen) im Jahr 2001, da bei der hochdosierten oralen Langzeittherapie kardiale Nebenwirkungen (QT-Syndrom) aufgetreten waren. Die parenterale Applikationsform, wo diese Nebenwirkung kein Problem darstellte, wurde aus kommerziellen und markttaktischen Gründen eingestellt.[4] Droperidol war weiterhin in Deutschland für den Gebrauch zugelassen und über ausländische Hersteller bzw. Vertreiber (z. B. Abbott, USA) zu beziehen.
Nachdem Janssen-Cilag angekündigt hatte, den Vertrieb von Droperidol Ende Juni 2001 weltweit einzustellen, wurde von der damaligen Schweizer Heilmittelbehörde (IKS) der Verkauf der Substanz Ende September 2001 verboten. Droperidol wird in der Schweiz von der Firma Sintetica wieder produziert und ist im Schweizer Handel auch legal wieder erhältlich.
Nach der angekündigten Einstellung der Produktion wurde die Lizenz von der Firma Arzneimittel ProStrakan vom früheren Lizenzinhaber Janssen-Cilag gekauft, was nach einem neu durchgeführten Zulassungsverfahren 2007 zu Zulassungen in verschiedenen europäischen Ländern führte (u. a. am 27. März 2008 in Deutschland).[8]
Bedeutung und Einsatzgebiete
Alte Zulassung
Droperidol erlangte nie eine Bedeutung in der Psychiatrie, stattdessen wird es in der Anästhesie verwendet. Zusammen mit einem hochpotenten Analgetikum (meist Fentanyl) ist es ein Bestandteil der Neuroleptanalgesie, deren Anwendung und Bedeutung im Bereich der klinischen Anästhesiologie seit etwa 1980 an Bedeutung verloren hat (Zunahme der Verfügbarkeit alternativer Verfahren wie etwa der TIVA). Zum anderen ist Droperidol ein wichtiges und eines der am besten untersuchten Medikamente bei postoperativer Übelkeit und Erbrechen (PONV). Bei PONV können erwachsenen Menschen 0,5 mg – 1,25 mg (bzw. 0,625-5 mg)[9] Droperidol langsam i.v. appliziert werden.[10] Zur Neuroleptanalgesie werden überwiegend höhere Dosierungen verwendet. Im Jahr 2001 wurde Dehydrobenzperidol vom deutschen Markt[11] genommen.
Neue Zulassung
Nach der neuen Zulassung steht das Fertigarzneimittel Xomolix in der Anästhesie zur Verfügung:[5]
- Prophylaxe und Therapie der postoperativen Übelkeit und Erbrechen (PONV) bei Erwachsenen und Kindern über zwei Jahre
- Prophylaxe von Übelkeit und Erbrechen durch Opioide bei der postoperativen Patienten-kontrollierten Analgesie (PCA).
Siehe auch
Weblinks
Einzelnachweise
- Europäische Arzneibuch-Kommission (Hrsg.): EUROPÄISCHE PHARMAKOPÖE 5. AUSGABE. Band 5.0–5.8, 2006.
- Eintrag zu Droperidol in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Datenblatt Droperidol bei Sigma-Aldrich, abgerufen am 29. März 2011 (PDF).
- Pharmazeutische Zeitung Nr. 27, S. 25 f.
- Fachinformation Xomolix 2,5 mg/ml Injektionslösung (ProStrakan Limited). Stand: Oktober 2009, abgerufen 24. Januar 2016.
- (Höfling S, Dworzak H, Butollo W, Neeef W,: Der Angstprozess unter verschieden hohen Thalamonaldosen zur Prämedikation, Anästhesist 1983;32;512-518).
- J. Wallenborn und andere: Metoclopramid und Dexamethason zur Prophylaxe von postoperativer Übelkeit und Erbrechen nach balancierter Anästhesie. In: AINS. Band 38, Nr. 11, November 2003, S. 695–704, hier: S. 702.
- Xomolix Receives Additional Key European Approvals, ProStakan Pressemitteilung vom 2. April 2008 auf der Webseite www.cmocro.com.
- J. Wallenborn und andere: Metoclopramid und Dexamethason zur Prophylaxe von postoperativer Übelkeit und Erbrechen nach balancierter Anästhesie. In: AINS. Band 38, Nr. 11, November 2003, S. 695–704, hier: S. 702 (zu Dehydrobenzperidol, Stand Januar 2003).
- Fachinformation Droperidol® Sintetica des Arzneimittel-Kompendiums® der Schweiz.
- J. Wallenborn und andere: Metoclopramid und Dexamethason zur Prophylaxe von postoperativer Übelkeit und Erbrechen nach balancierter Anästhesie. In: AINS. Band 38, Nr. 11, November 2003, S. 695–704, hier: S. 702.
- Rote Liste Service GmbH (Hrsg.): Rote Liste 2017 – Arzneimittelverzeichnis für Deutschland (einschließlich EU-Zulassungen und bestimmter Medizinprodukte), Rote Liste Service GmbH, Frankfurt/Main, 2017, Aufl. 57, ISBN 978-3-946057-10-9, S. 397.
- Larsen Anästhesie (5. Auflage)
- E. Burgius, Intensivkurs Allgemeine und spezielle Pharmakologie