Diisobutylaluminiumhydrid
Diisobutylaluminiumhydrid (Abk. DIBAL, DIBAL-H, DIBALH, DIBAH) ist ein Reduktionsmittel mit der chemischen Formel (i-Bu)2AlH (i-Bu = Isobutyl). DIBAL wird vor allem in der organischen Synthese für verschiedene Reduktionen verwendet (siehe: Hydroaluminierung) und liegt in der Reaktivität zwischen Lithiumaluminiumhydrid (LiAlH4) und Natriumborhydrid (NaBH4).
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
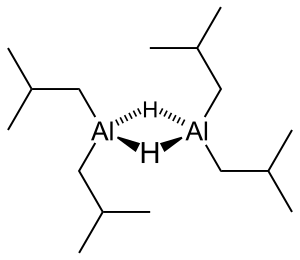 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Diisobutylaluminiumhydrid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H19Al | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 142,22 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Ein typisches Einsatzgebiet von DIBAL ist die direkte Reduktion von Estern zu Aldehyden. Um eine konsekutive Reduktion der gebildeten Aldehyde zu Alkoholen zu verhindern wird die Reaktion bei −78 °C durchgeführt. Bei der Verwendung von LiAlH4 beispielsweise werden die Ester stets zu Alkoholen weiterreduziert, während NaBH4 kaum Reaktivität (substituentenabhängig) gegenüber Estern besitzt.
Auch zur Reduktion von Nitrilen zu Aldehyden wird DIBAL häufig eingesetzt. Damit lässt sich die Reaktion so steuern, dass ein Molekül DIBAL-H immer nur ein Hydrid-Ion überträgt. Wegen der sperrigen iso-Butyl-Gruppen werden sterisch leicht zugängliche, elektrophile Zentren bevorzugt angegriffen.
DIBAL ist ein elektrophiles Reduktionsmittel, das gut mit elektronenreichen Verbindungen reagiert, während die Reaktivität gegenüber elektronenarmen Substraten eher gering ist.
DIBAL ist sowohl in Substanz, komfortabler jedoch in Lösung (z. B. in Toluol) kommerziell erhältlich. Es kann durch β-Hydrideliminierung aus Triisobutylaluminium synthetisiert werden. DIBAL ist luft- und feuchtigkeitsempfindlich und reagiert heftig mit Wasser.[2]
Einzelnachweise
- Eintrag zu DIBAL. In: Römpp Online. Georg Thieme Verlag, abgerufen am 2. Mai 2014.
- Product Data Sheet Nouryon (Memento vom 25. Juli 2019 im Internet Archive).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- Datenblatt Diisobutylaluminum hydride bei Sigma-Aldrich, abgerufen am 3. November 2021 (PDF).

